
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кінетична і агрегативна стійкість колоїдних розчинів
|
|
|
|
Для колоїдних розчинів характерним є рух частинок дисперсної фази, який спричиняється хаотичними ударами з боку молекул середовища, які перебувають в тепловому русі. Його вперше спостерігав шотландський ботанік Броун. Саме тому рух частинок дисперсної фази в дисперсійному середовищі золю називають броунівським.
Наслідком кінетичних властивостей колоїдних розчинів є їх кінетична стійкість, яка полягає в тому, що концентрація колоїдних розчинів однакова в усьому об’ємі системи і при правильному зберіганні не змінюється в часі.
Здатність подрібнених систем зберігати властивий їм ступінь дисперсності називають агрегативною стійкістю. Якісна особливість колоїдних розчинів – їх агрегативна нестійкість: в колоїдних розчинах самовільно відбуваються процеси в напрямку зменшення сумарної поверхні, які призводять до зменшення дисперсності, тобто до збільшення частинок. Внаслідок цього колоїдні системи термодинамічно нестійкі.
Поняття кінетичної і агрегативної стійкості ввів в науку про колоїдні системи М.Пєсков (1922 р.).
Будь-яка міцела являє собою агрегат простих молекул, характерний для взятого золю тільки в даний момент і для певних умов. Зміна умов може призвести до зміни його розмірів, до випадання осаду.
Отже, можна говорити тільки про відносну стійкість колоїдних систем. Основними чинниками, які зумовлюють відносну стійкість колоїдних систем, є малі розміри частинок, їх розвинута поверхня, броунівський рух і однойменні заряди, які спричиняють їх взаємне відштовхування.
Наявність електричного заряду у частинок дисперсної фази призводить до їх значної гідратації: полярні молекули води певним чином орієнтуються відносно заряджених частинок і взаємодіють з ними. Гідратна оболонка помітно знижує поверхневу енергію дисперсної фази і тим самим зменшує намагання частинок до укрупнення.
За теорією ДЛФО (Б.В.Дерягіна (1937 р.), Л.Д.Ландау і голландських вчених Фервея і Овербека (1948 р.)) потенціальна енергія взаємодії (U) між колоїдними частинками є алгебраїчною сумою потенціальної енергії електростатичного відштовхування (UЕ) і потенціальної енергії дисперсійного притягання (UД) між ними:
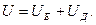
Якщо UЕ > UД, то відштовхування превалює над притяганням, і дисперсна система стійка. Якщо UЕ < UД, то відбувається злипання колоїдних частинок, а потім випадання в осад.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1237; Нарушение авторских прав?; Мы поможем в написании вашей работы!