
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота №5
|
|
|
|
ОДНО- Й БАГАТОАТОМНІ СПИРТИ. ФЕНОЛИ. ЕТЕРИ
1. Виявлення води у спирті
Реактиви: етиловий спирт, безводний CuSO4.
До білого порошку безводного сульфату міді - CuSO4 долити етиловий спирт. Якщо спирт містить воду, то сульфат міді синішає. Зробити висновок про аналізований спирт.
2. Розчинність спиртів у воді
Реактиви: метиловий, етиловий, аміловий спирти, гліцерин, синій лакмусовий папір.
В окремі пробірки помістити по 1,0 мл метилового, етилового, амілового спиртів і гліцерину. Долити надлишок води, струснути і спостерігати розчинність. Зробити висновок про розчинність спиртів в залежності від їхньої молекулярної маси й атомності. Водяні розчини спиртів випробуйте синім лакмусовим папером. Яке середовище водних розчинів спиртів?
3. Утворення алкоголяту і його гідроліз
Реактиви: етиловий, метиловий, аміловий спирти, металевий натрій, розчин фенолфталеїну.
У 3 сухі пробірки внести по 1,0 мл спиртів: етилового (абсолютного), метилового, амілового. У кожну пробірку внести по шматочку очищеного металевого натрію. Відзначити, у якій пробірці реакція йде найбільше інтенсивно й у який повільно. Чому?
Реакцію доведіть до кінця. У першу пробірку додайте надлишок води і 1 краплю фенолфталеїну. Спостереження. Навести хімізм реакції спирту з натрієм. Як розщеплюється s- зв'язок О-Н у цій реакції? Які властивості спиртів виявляються в реакції з натрієм? Напишіть рівняння реакції етилату натрію з водою. Поясніть чому з'являється забарвлення з фенолфталеїном.
4. Окиснення спиртів
Реактиви: етиловий і метиловий спирти, хромова суміш, розчин сірчаної кислоти, мідна спіраль.
а) окислювання спиртів хромовою сумішшю
Внести в пробірку 1,0 мл етилового спирту, додати 1,0 мл розведеної H2SO4 і 2 мл 5% K2Cr2O7. Отриманий розчин обережно нагріти. Спостерігати зміну забарвлення і появу характерного запаху “прілих яблук” - оцтового альдегіду. Одну краплю отриманого розчину перенести в пробірку з 3 краплями розчину фуксинсірчистої кислоти. Поява фіолетового забарвлення свідчить про присутність альдегіду. Реакція може бути використана для відкриття етилового спирту. Представити механізм реакції.
б) окиснення і дегідрування етилового спирту
1,0 мл етилового спирту помістити в пробірку. Розжарити мідну спіраль до червоного кольору і внести в пробірку зі спиртом. Звернути увагу на зміни, що відбуваються зі спіраллю і на появу характерного запаху. Вийняти спіраль, додати у пробірку дві краплі фуксинсірчистої кислоти. З'являється характерне забарвлення, що свідчить про присутність альдегіду. Представити хімізм окиснення і дегідрування спирту.
5. Виявлення домішки метилового спирту в етиловому спирті
Реактиви: етиловий спирт, що містить домішку метилового спирту, фуксинсірчиста кислота, розведена H2SO4, розчин KMnO4, середній або кислий сульфат натрію або калію (у порошку або розчині).
Дослід проводять із звичайним етиловим спиртом і паралельно зі спиртом, що містить домішку метилового спирту. У дві окремі пробірки доливають по 1,0 мл випробуваних спиртів. До них доливають по 1 мл розчину H2SO4 і 3 мл розчину KMnO4. Через кілька хвилин добавляють ще 2мл H2SO4. Розчин повинний бути безбарвним. Якщо забарвлення KMnO4 не зникнуло, вносять трішечки сульфіту натрію до повного знебарвлення. Потім доливають до отриманої рідини рівний обсяг розчину фуксинсірчистої кислоти. Через 3-5 хвилин порівняти колір розчину, що містить метиловий спирт та без нього. У пробірці з домішкою метилового спирту виникає синьо-фіолетове забарвлення. Цей метод дозволяє виявити домішку метилового спирту в кількості 0,5%. Навести хімізм реакції.
6. Відкриття сивушної олії
Реактиви: сивушне масло або аміловий спирт, хлоргідрат метилового фіолетового.
Внести в пробірку 1,0 мл сивушного масла або амілового спирту, додати 3-4 краплі зеленого розчину хлоргідрату метилового фіолетового, добре збовтати. Верхній шар, що складається із сивушного масла, забарвлюється у фіолетовий колір, тому що сивушне масло витягає з водного розчину основу метилового фіолетового, що утворюється при гідролізі хлоргідрату.
7. Якісна реакція на багатоатомні спирти
Реактиви: 0,2н розчин CuSO4, концентрований розчин NaOH, гліцерин.
Помістити в пробірку 1,0 мл розчину CuSO4 і 1,0 мл концентрованого розчину лугу. До отриманого студенистого осаду долити по стінках пробірки гліцерин. Струснути. На основі спостереження явищ, напишіть рівняння реакцій, що відбуваються. Які властивості гліцерину виявляються в реакції з гідроксидом міді?
8. Розчинність, кислотний характер фенолів і нафтолів
Реактиви: одноатомний фенол, двоатомні феноли, a- і b-нафтоли, універсальний індикаторний папір.
До досліджуваних фенолів у кількості 0,1 - 0,3 г додати надлишок води і струснути. Якщо цілком розчинення не спостерігається, суміш нагріти до кипіння, потім остудити. Відмітити, які досліджувані сполуки добре розчинні у воді, які - погано. За допомогою універсального індикаторного паперу визначити рН розчинів. Звернути увагу на найбільше виражений кислотний характер у нафтолів і їх погану розчинність у воді.
9. Бромування фенолів
Реактиви: бромна вода, водний розчин фенолу (карболова вода).
Внести у пробірку 1,0 мл водного розчину фенолу і при постійному струшуванні поступово додати бромну воду до одержання пластівчастого осадку. Що доводить дана реакція? Навести хімізм.
10. Кольорові реакції фенолів
Реактиви: розчини одноатомного і багатоатомного фенолів, 1% розчин FeCl3.
До розчинів досліджуваних фенолів додати 3-5 крапель FeCl3. Спостерігати різноманітні забарвлення. Так як феноли і сполуки, що містять фенольну групу, дають із FeCl3 комплексні феноляти.
Завдання для самостійної роботи
1. Напишіть ізомери спирту складу С5Н11ОН. Складіть схеми реакцій окиснення кожного спирту дихроматом калію в сульфатнокислому середовищі. Назвіть вихідні й одержані речовини.
2. Напишіть формули: а) етиленгліколю; б) гліцерину; в) метилбутилкарбінолу.
3. Дайте назву нищенаведеним сполукам:
а) СН3 – СН – СН – СН – СН3
ç ç ç
С2Н5 СН3 СН2 – ОН
б) СН3 – СН – О – СН2 – СН3
ç
СН3
в) СН2 – СН2 – СН2
ç ç
ОН ОН
 г)
г) 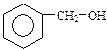 д)
д) 
е) 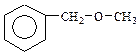 є)
є) 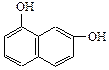
4. Напишіть рівняння реакцій:
а) каталітичного дегідрування пропанолу-2;
б) взаємодії 1-бутанолу з концентрованою сульфатною кислотою при нагріванні;
в) внутрішньомолекулярної дегідратації спиртів: 3-метил-2-бутанолу; 3-гексанолу
5. Напишіть для амілового спирту рівняння реакцій:
а) взаємодії з металічним натрієм;
б) окиснення спиртової групи;
в) окиснення за місцем подвійного зв’язку (реакція Вагнера).
6. Наведіть формули спиртів і простих ефірів складу С4Н10О. Назвіть їх.
7. Здійсніть ряд перетвореннь: бензол → ізопропілбензол →фенол → фенолят натрію → дифеніловий ефір.
8. Напишіть схеми реакцій взаємодії фенолу:
а) з їдким калієм;
б) з нітратною кислотою;
в) з бромом.
Назвіть одержані сполуки.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1745; Нарушение авторских прав?; Мы поможем в написании вашей работы!