
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
OH OH Br Br
|
|
|
|
ОН
НO–С–С–OН+2KMnO4+3H2SO4→K2SO4+2MnSO4+10CO2+8H2O
|| ||
O О
4.Розклад мурашиної кислоти
Реактиви: мурашина кислота.
У пробірку з газовідвідною трубкою з відтягнутим у капіляр кінцем налийте 1 – 1,5 мл мурашиної кислоти і обережно нагрійте. Мурашина кислота при цьому розкладається з виділенням оксиду вуглецю (СО) (обережно, отруйний!), який при запалюванні горить синім полум’ям.
 H- С = О → CO + H2O
H- С = О → CO + H2O
ОН
Якщо реакція не закінчилася, запаліть газ біля отвору газовідвідної трубки, щоб запобігти накопиченню чадного газу (СО) в приміщенні.
5. Розклад щавлевої кислоти
Реактиви: щавлева кислота, вапняна або баритова вода.
 У суху пробірку з газовідвідною трубкою покладіть 1-2 г щавлевої кислоти. Газовідвідну трубку занурте в пробірку з вапняною або баритовою водою. Пробірку з щавлевою кислотою нагрійте. При цьому виділяються гази. Вуглекислий газ реагує з вапняною водою і утворює осад. Потім трубку вийміть з рідини і запаліть біля її отвору газ, що виділяється. CO2
У суху пробірку з газовідвідною трубкою покладіть 1-2 г щавлевої кислоти. Газовідвідну трубку занурте в пробірку з вапняною або баритовою водою. Пробірку з щавлевою кислотою нагрійте. При цьому виділяються гази. Вуглекислий газ реагує з вапняною водою і утворює осад. Потім трубку вийміть з рідини і запаліть біля її отвору газ, що виділяється. CO2

 НO – С – С – OН t CO2 + H- С = О
НO – С – С – OН t CO2 + H- С = О
|| || ОН H2O
O О
Ca (OH)2 + CO2 → CaCO3 ¯ + H2O
Як розкладаються при нагріванні інші карбонові кислоти? Що таке реакція декарбоксилювання? Які продукти утворюються при декарбоксилюванні одноосновних карбонових кислот?
6. Проба на ненасиченість олеїнової кислоти
Реактиви: олеїнова кислота (або рослинна олія), бромна вода, розчин KMnO4, розчин лугу.
В одну пробірку налийте бромної води, а в другу – лужний розчин KMnO4. В обидві пробірки додайте по краплі олеїнової кислоти. Суміш у пробірках збовтайте. Бромна вода знебарвлюється, а в пробірці з KMnO4 випадає бурий осад диоксиду марганцю.
Що доводять проведені реакції?
a)CH3–(CH2)7–CH=CH–(CH2)7–COOH+Br2→CH3–(CH2)7–CH–CH–CH2–COOH
| |
Br Br
б)CH3–(CH2)7–CH=CH–(CH2)7–COOH+[О]+Н2О KmnO4CH3–(CH2)7–CH–CH–CH2-COOH
| | → | |
7. Ізомеризація олеїнової кислоти в елаїдинову
Реактиви: олеїнова кислота, концентрована нітратна кислота, мідний дріт.
У пробірку налийте 0,5 – 1 мл олеїнової кислоти і киньте коротеньку зім’яту дротинку вагою 0,1 – 0,2 г По стінках пробірки налийте 1 мл. концентрованої нітратної кислоти, суміш обережно перемішайте. Коли спінювання суміші припиниться і гази перестануть виділятися, пробірку закрийте пробкою і залиште на 0,5 –1 год.
При цьому рідка олеїнова кислота перетворюється у тверду елаїдинову.
H – C – (CH2)7 – CH3 H – C – (CH2)7 – CH3
| | → | |
H – C – (CH2)7 – CООН НООС–(CH2)7 – C – H
Олеїнова кислота Елаїдинова кислота
Оксиди азоту, що утворюються при взаємодії міді з концентрованою нітратною кислотою, каналізують ізомеризацію олеїнової кислоти (цис-ізомер) в більш стійкий транс-ізомер – тверду елаїдинову кислоту.
8. Дія хлориду заліза (ІІІ) на оцтову кислоту (якісна реакція)
Реактиви: ацетат натрію, розчин FeCl3.
У пробірку налийте 1-2 мл розчину ацетату натрію та кілька крапель FeCl3. Розчин забарвлюється у темно-червоний колір, оскільки утворюється комплексна сполука, розчинна у воді. При нагріванні темно-червоне забарвлення зникає і випадає бурий осад ацетату гідроксозаліза (ІІІ).
При взаємодії хлориду заліза з ацетатом натрію спочатку утворюється ацетат заліза [ Fe3(OH)2(CH3COO)6]+Cl-
Аналогічний дослід проведіть з бензойною кислотою. Зробіть висновки.
Завдання для самостійної роботи
1. Виведіть формули всіх ізомерних карбонових кислот складу С5Н10О2. Назвіть їх за замісниковою номенклатурою (IUPAC) та раціональною номенклатурою.
2. Напишіть схему перетворень: СН3СООН 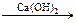 А
А  Б
Б 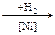

 В
В 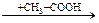 Г
Г
Дайте назви одержаним сполукам.
3. Напишіть схеми одержання кислот:
а) з метилоцтового альдегіду;
б) з 1,1,1- три хлор – 3-метилбутану;
в) з бромистого етилу реакцією вітрильного синтезу.
4. Напишіть рівняння реакцій естерифікації, при яких одержують:
а) неповний мурашинокислий естер 1,3 –пропадіолу;
б) диетилоксалат;
в) ізопропіло-фталат.
5. Напишіть формули ізомерних ароматичних кислот складу С8Н8О4. Назвіть їх.
6. Закінчіть рівняння реакцій:
а) СН2 =CH – СООН + НBr →
б) 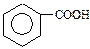
| + HNO3 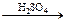
|
в) 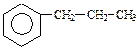
| + KMnO4 + H2SO4 
|
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 649; Нарушение авторских прав?; Мы поможем в написании вашей работы!