
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторна робота № 10
|
|
|
|
ВУГЛЕВОДИ (моносахариди,дисахариди, полісахариди)
1. Загальна реакція на вуглеводи з a- нафтолом
(реакція Моліша)
Реактиви: 15% спиртовий розчин нафтолу, концентрована сульфатна кислота, різні вуглеводи (глюкоза, фруктоза, сахароза, крохмальний клейстер).
У пробірки налити по 0,5 мл води і внести дуже невеличку кількість вуглеводів: глюкози,фруктози, сахарози і крохмалю. Потім у кожну з пробірок додати 1-2 краплі спиртового розчину a–нафтолу і нахиливши пробірку, по стінках за допомогою піпетки обережно долити 1мл концентрованої сульфатної кислоти. Утвориться два шари: нижній -сульфатна кислота, верхній - водний шар. На межі двох шарів з'являється забарвлене кільце. Цю кольорову реакцію дають як моносахариди, так і полісахариди, причому кетози дають більш інтенсивне забарвлення чим альдози. При взаємодії концентрованої сульфатної кислоти вуглеводи розкладаються. Серед продуктів розкладання присутні фурфурол і його похідні. Вони конденсуються з нафтолом з утворенням забарвлених продуктів.
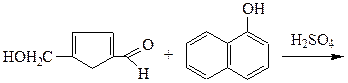
фурфурол α-нафтол
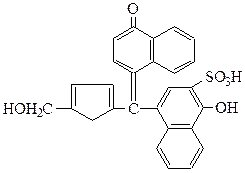
2.Осмолення моносахаридів
Реактиви: 10% розчин глюкози, 30-40% розчинNaOH, 10% розчин сульфатної кислоти.
У пробірці змішати 1,0 мл 10% розчину глюкози і 1,0 мл концентрованого розчину NaOH, внести в суміш кип'ятильні камінці і кип'ятити 2-3 хвилини. Рідина в пробірці набуває жовтого, а потім бурого кольору. Після охолодження її підкисліть 10% розчином сульфатної кислоти. Забарвлення блідне і з'являється запах паленого цукру.
При нагріванні з концентрованим розчином лугу моносахариди осмолюються і окиснюється. Утворюється складна суміш речовин. У ній містяться також продукти полімеризації і конденсації сполук, що утворяться при розпаді моноз, а також виявлені молочна, мурашина кислоти.
3. Окислення моносахаридів реактивом Фелінга
Реактиви: 1% розчин глюкози, 1% розчин фруктози, реактив Фелінга.
В одну пробірку помістити 1,0 мл розчину глюкози, у другу - стільки ж розчину фруктози. Потім у кожну пробірку додати рівний об'єм розчину Фелінга. Вміст пробірок перемішати і нагріти. Звернути увагу на появу жовто-червоного осадку CuO. Які вуглеводи визначаються цією реакцією?
4. Окислення моносахаридів аміачним розчином оксиду срібла (реакція срібного дзеркала)
Реактиви: аміачний розчин гідроксиду срібла, 1% розчин глюкози.
До 10 мл глюкози додати 1,0 мл аміачного розчину гідроксиду срібла. Нагріти. Спостерігати виділення або чорного осаду, або, якщо стінки пробірки були чисті, наліт срібла на стінках пробірки. (Під час нагрівання пробірку не можна струшувати, тому що срібло виділиться не на стінках пробірки, а у вигляді осаду).
При окисненні моносахаридів у лужному середовищі утвориться суміш продуктів в наслідок руйнації моносахарида. Але також утвориться в невеличкій кількості альдонова кислота (одноосновна). У даному випадку також утвориться глюконова кислота. Навести окислення глюкози до глюконової кислоти.
5.Реакція Селіванова на фруктозу
Реактиви: реактив Селіванова (розчин резорцину в розведеній соляній кислоті), 1% розчин фруктози, 5% розчин меду.
У пробірку внести декілька крапель реактиву Селіванова і додати 1,0 мл розчину фруктози. Нагріти до початку кипіння. Поступово рідина набуває червоне забарвлення, обумовлене утворенням оксиметилфурфуролу.
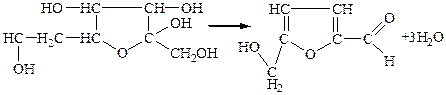
Такий же дослід проробити з розчином меду. Зробити висновок.
6. Доведення наявності гідроксогруп у моносахаридах і дисахаридах
Реактиви: 1% розчин глюкози і сахарози, 2н розчин NaOH, 0,2н розчин CuSO4 .
Одержати у двох пробірках блакитний осад гідроксиду міді, змішавши 0,5 мл сульфату міді з 1,0 мл гідроксиду натрію. До отриманого осаду долити надлишок розчину глюкози і сахарози. Вміст пробірок струснути. Чому відбувається розчинення осаду? Навести хімізм процесу.
7. Розпізнавання дисахаридів, що відновлюють (редукують) і не відновлюють (не редукують)
Реактиви: 1% розчини сахарози, лактози і мальтози, реактив Фелінга.
У три пробірки наливають по 1,0 мл сахарози, мальтози і лактози. Потім у кожну пробірку додають у рівному об'ємі реактив Фелінга, нагрівають до початку кипіння. У якій із пробірок випадає червоно-жовтий осад міді (I)? Поясніть результати досліду. Поясніть хімізм взаємодії відповідного дисахариду з реактивом Фелінга.
8.Гідроліз сахарози
Реактиви: 1% розчин сахарози, 2н розчин HCl, розчин Фелінга, реактив Селіванова.
У пробірку налити 1 мл сахарози, декілька крапель розведеної соляної кислоти і прокип'ятити 4-5 хвилин. Частину отриманого розчину нейтралізувати розчином гідроксиду натрію до слаболужної реакції і додати розчин Фелінга. Нагріти. Чому виділяється червоно-жовтий осад оксиду міді (I)? До другої частини розчину долити реактив Селіванова, нагріти. Про що свідчить поява червоного забарвлення розчину? Навести рівняння гідролізу сахарози.
9.Виявлення лактози у молоці
Реактиви: молоко, оцтова кислота, 10% розчин гідроксиду натрію, фенолфталеїновий папірець, реактив Фелінга.
У хімічний стакан внести 3-4 мл молока, розведеного водою (1:1), додати декілька крапель оцтової кислоти. Добре перемішати суміш скляною паличкою. У кислому середовищі білки молока випадають в осад у вигляді пластівців. Осад відфільтрувати. Фільтрат нейтралізувати 10% розчином гідроксиду натрію до слаболужної реакції по індикаторному фенолфталеїновому папірці. Відлити частину отриманого розчину, додати до нього стільки ж розчину Фелінга, нагріти до кипіння. Чи змінюється забарвлення розчину. Поясніть дослід і напишіть рівняння реакції.
10. Кольорові реакції на сахарозу.
Реактиви: 10% розчин сахарози, 5% розчин сульфату кобальту, 5% розчин сульфату нікелю, 5% розчин гідроксиду натрію.
У дві пробірки наливають по 1,0 мл розчину сахарози і по 1,0 мл розчину гідроксиду натрію. Потім в одну пробірку додають декілька крапель розчину сульфату кобальту, у другу – декілька крапель розчину сульфату нікелю. У пробірці із сіллю кобальту з'являється фіолетове забарвлення, а із сіллю нікелю - зелене.
11.Карамелізація сахарози
Реактиви: сахароза кристалічна.
У пробірку насипати невеличку кількість кристалів сахарози й обережно нагріти доти, поки сахароза не розплавиться і не побуріє. Темний продукт, що утворився, є карамеллю.
12. Реакція крохмалю з йодом
Реактиви: крохмальний клейстер, розчин йоду.
У пробірку помістити 1,0 мл крохмального клейстеру і 1-2 краплі розведеного розчину йоду. Звернути увагу на колір розчину крохмалю. Нагріти розчин, а потім остудити. Пояснити явища, що спостерігаються.
13. Кислотний гідроліз крохмалю
Реактиви: крохмальний клейстер, 2н Н2SO4, розчин I2 у KI, 10% р-н NaOH, р-н Фелінга.
У пробірку наливають 1,5-2 мл крохмального клейстеру і декілька крапель 10% H2SO4. У 7-8 пробірок поміщають по декілька крапель розчину йоду в йодиді калію. У першу пробірку внести 1-2 краплі підготовленого для досліду розчину крохмалю. Потім пробірку з крохмальним клейстером нагріти. Через 30 сек. після початку кипіння відібрати піпеткою пробу розчину і внести в другу пробірку з розчином йоду. Надалі відбирати проби через кожні 30 сек. і вносити в наступні пробірки з розчином йоду. Відзначити поступову зміну забарвлення розчинів при реакції з йодом. Після того як реакційна суміш перестане давати забарвлення з йодом, суміш кип'ятять ще 2-3 хвилини, охолоджують і нейтралізують 10% розчином гідроксиду натрію. До отриманого розчину доливають рівний об'єм розчину Фелінга і нагрівають. Який можна зробити висновок на підставі реакції з реактивом Фелінга? Навести схему гідролізу крохмалю.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3013; Нарушение авторских прав?; Мы поможем в написании вашей работы!