
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Білет 3 питання 1
|
|
|
|
Білет 3
Вн́утрішня ене́ргія тіла (позначається як E або U) — повна енергія термодинамічної системи за винятком її кінетичної енергії як цілого і потенціальної енергії тіла в полі зовнішніх сил. Внутрішня енергія складається з кінетичної енергії хаотичного руху молекул, потенціальної енергії взаємодії між ними і внутрішньомолекулярної енергії.
Зміна внутрішньої енергії при переході з одного стану в інший буде завжди дорівнювати різниці значень в цих станах, незалежно від шляху, по якому здійснювався перехід. Внутрішню енергію тіла не можна виміряти напряму. Можна визначити тільки зміну внутрішньої енергії: 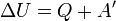
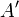 — робота, виконана над термодинамічною системою[1] або:
— робота, виконана над термодинамічною системою[1] або:
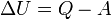 ,
,
де 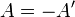 , робота виконана термодинамічною системою.
, робота виконана термодинамічною системою.
Внутрішня енергія, як термодинамічний потенціал
Оскільки внутрішня енергія є функцією стану, то її можна визначити як термодинамічний потенціал, залежний від об'єму, числа частинок у системі, та ентропії: U(V,S,N).
Для квазістатичних процесів виконується співвідношення: 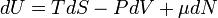
де T — температура, S — ентропія, P — тиск, μ — хімічний потенціал, N — кількість частинок в системі.
Ві́льна ене́ргія Гельмго́льца — термодинамічний потенціал, який визначає рівноважні термодинамічні характеристики системи в залежності від об'єму й температури.
Рівновжний стан системи багатьох часток при визначеному об'ємі й сталій температурі визначається мінімумом вільної енергії.
Дослідження показали, що нагрітий газ при охолодженні, що не роби, не віддає всю свою енергію. Ту частку енергії газу, яку можна було відібрати й перетворити в корисну роботу, стали називати вільною енергією.
Вільна енергія F визначається, як 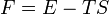 ,
,
Зміна вільної енергії дорівнює роботі, виконаній над тілом при ізотермічному процесі
Диференціал вільної енергії дорівнює 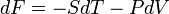 .
.
У випадку системи із змінним числом часток, диференціал вільної енергії отримує додатковий член 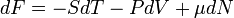 ,
,
де μ — хімічний потенціал, N — число часток.
Вирази для вільної енергії деяких термодинамічних систем
Для класичного ідеального одноатомного газу вільна енергія дорівнює
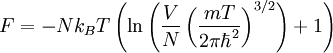
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 404; Нарушение авторских прав?; Мы поможем в написании вашей работы!