
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ентропія та ентальпія. Вільна енергія Гіббса
|
|
|
|
Ентроп́ія S — в термодинаміці міра енергії у термодинамічній системі, яка не може бути використана для виконання роботи. Вона також є мірою безладдя, присутнього в системі.
Поняття ентропії було вперше введено у 1865 році Рудольфом Клаузіусом. Він визначив зміну ентропії термодинамічної системи при оборотному процесі як відношення загальної кількості теплоти ΔQ, отриманої або втраченої системою, до величини абсолютної температури T:
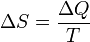
Рудольф Клаузіус дав величині S назву «ентропія», утворивши її від грецького слова τρoπή, «зміна» (зміна, перетворення).
Рівність відноситься саме до зміни ентропії. У термодинаміці ентропія визначається лише з точністю до сталої.
Зв'язок між теплоємністю та ентропією дається формулою
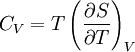
Властивості ентропії: Ентропія є екстенсивною величиною(залежить від маси і об'єму системи), тому сумарна ентропія двох систем
S = S 1 + S 2
Ентропія є функцією стану системи, її зміна не залежить від способу переходу з кінцевого стану у початковий: Δ S = Sf − Si. В самочинних поцесах, які протікають в ізольованій системі, ентропія зростає(ΔS>0), а в оборотних рівноважних — вона незмінна (ΔS=0).
Ізоентропійність — незмінність ентропії; ізоентропійні п р о ц е с и — зміна стану фізичної системи, коли не змінюється її ентропія.
Ентальпі́я (або теплова функція, від грец. enthálpo — «нагріваю») — термодинамічний потенціал, що характеризує стан термодинамічної системи при виборі як основних незалежних змінних ентропії (S) і тиску (P). Позначається H (S, P, N, xi) або W (S, P, N, xi), де N — число частинок системи, xi — інші макроскопічні параметри системи. Ентальпія — адитивна функція, тобто ентальпія всієї системи дорівнює сумі ентальпій її складових частин. Із внутрішньою енергією E системи ентальпія зв'язана співвідношенням:
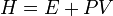 ,
,
де E - внутрішня енергія, P - тиск, V - об'єм.
Таким чином ентальпія дорівнює сумі внутрішньої енергії і добутку тиску на об'єм.
Ентальпія залежить від тиску й ентропії системи, тобто при незмінних N і xi її повний диференціал дорівнює:
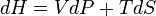 .
.
Ентальпія використовується для опису ізобарних процесів, тобто процесів, які відбуваються при сталому тиску. Якщо процес проходить при сталому тиску, то приріст ентальпії дорівнює переданій тілу теплоті dQ = TdS.
Тож,
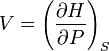 ,
,
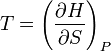 .
.
Вільна енергія Гіббса (або просто енергія Гіббса, або потенціал Гіббса, або термодинамічний потенціал у вузькому значенні) - це термодинамічний потенціал такого вигляду:
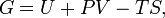
Енергію Гіббса можна розуміти як повну хімічну енергію системи (кристала, рідини і т.п.)
Поняття енергії Гіббса широко використовується в термодинаміці та хімії.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3149; Нарушение авторских прав?; Мы поможем в написании вашей работы!