
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ферум(iii) гідроксид
|
|
|
|
Ферум(ii) гідроксид
Ферум(iii) оксид
Ферум(ii) оксид FeO
Чорний порошок, який легко окиснюється. У воді практично нерозчинний.
Добування: 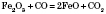
Хімічні властивості. Основний оксид, характерна взаємодія з кислотами:
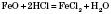 .
.
Найстійкіша природна оксигеновмісна сполука Феруму. У воді практично нерозчинний.
Добування. Розкладання ферум(III) гідроксиду під час нагрівання:
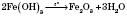
Хімічні властивості. Слабко амфотерний оксид.
Осад білого кольору. На повітрі окиснюється до ферум(III) гідроксиду, забарвлення стає зеленуватим, а потім бурим:

Добування. Дія розчинів лугів на розчини солей феруму(II):

Хімічні властивості. Слабкий амфотерний гідроксид. Характерна взаємодія з кислотами:
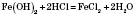
Осад червоно-бурого кольору.
Добування. Дія розчинів лугів на розчини солей феруму(III):
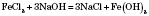
Хімічні властивості. Основний гідроксид. Характерна взаємодія з кислотами:
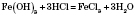
Металу́ргія (рос. металлургия, англ. metallurgy, нім. Metallurgie f, Hüttenwesen n, Hüttenkunde f) — наука, техніка і галузь промисловості, пов'язана з одержанням металів з руд або металовмісних речовин з наданням їм необхідних властивостей. У прикладному плані — сукупність зв'язаних між собою галузей і стадій виробничого процесу від видобутку сировини до випуску готової продукції — чорних і кольорових металів і їх сплавів (стопів).
До чорних металів відносять залізо, марганець і хром. Решта — кольорові. За фізичними властивостями і призначенню кольорові метали умовно ділять на важкі (мідь, свинець, цинк, олово, нікель) і легкі (алюміній, титан, магній).
Властивості металів та методи їхньої модифікації вивчає металознавство.
Сплав (стоп [1]) — тверда або рідка однорідна речовина, утворена сплавленням (стопленням) кількох металів або металів з неметалами.[2]
Однорідні стопи (сплави) утворюються в тих випадках, коли атоми одного металу можуть заміщатися атомами іншого металу у вузла кристалічних ґраток. За такого заміщення творяться кристали зі структурою, що схожа на структуру вихідних металів, проте з атомами різного ґатунку, чим і зумовлена однорідність стопу (сплаву). Такі стопи звуть твердими розчинами. Тверді розчини утворює Аурум з Арґентумом, Нікол з Купрумом, тощо.
Неоднорідні сплави є механічною сумішшю кристалітів металів. До того ж кожний з металів зберігає свою кристалічну ґратку. Наприклад, структура стопів Стануму з Плюмбумом, які використовують як м'які припої, складається з кристалітів чистого Стануму та кристалітів чистого Плюмбуму.
У вільному стані в природі зустрічаються тільки неактивні метали. Так у вигляді самородків зустрічаються золото й платина, іноді – срібло й мідь. Добування цих металів пов’язане лише з механічним відокремленням їх від домішок. Більшість металічних елементів легко окиснюються й існують в природі тільки у сполуках: оксидах (Fe3O4, Cr2O3), сульфідах (FeS2, ZnS), солях (NaCl, CaCO3). Саме з таких природних сполук і добувають метали шляхом їх хімічної переробки.
Природні мінеральні сполуки, з яких економічно доцільно видобувати метал у виробничих умовах називають рудами. Найважливішими рудами є оксиди, сульфіди і карбонати металічних елементів. Першим етапом переробки руд є видалення пустої породи — збагачення руди. Добування металів із руд ґрунтується на їх відновленні різними способами.
Найважливіший спосіб одержання металів із руд — відновлення оксидів відповідних металічних елементів вугіллям (коксом) при нагріванні:
SnO2 + C = Sn + CO2.
Досить часто оксидні руди відновлюють карбон(ІІ) оксидом, а інколи — воднем:
Fe2O3 + 3CO = 2Fe + 3CO2
WO3 + 3H2 = W + 3H2O.
Сульфідні руди спочатку випалюють, а потім відновлюють одержаний оксид:
2PbS + 3O2 = 2PbO + 2SO2
PbO + C = Pb + CO.
Важливим методом добування металів є відновлення менш активних металів активнішими металами і деякими неметалами при нагріванні. Відновлення алюмінієм називають алюмінотермією, відновлення магнієм — магнієтермією, силіцієм — силікотермією:
Fe2O3 + 2Al = 2Fe + Al2O3.
Органі́чні сполу́ки — клас сполук, в склад яких входить сполука Карбон (за винятком карбідів, карбонатної кислоти, карбонатів, оксидів Карбону і ціанідів). Окрім Карбону, вони майже завжди містять Гідроген, досить часто — Оксиген, Нітроген та галогени, рідше Фосфор, Сульфур та інші елементи. В органічних сполуках Карбон завжди виявляє валентність IV.
До органічних сполук належать не тільки природні речовини, які отримуються при розвитку рослин, або в результаті життєдіяльності тварин, але і багато штучно отриманих в лабораторії речовин.
До складу органічних молекул органічних речовин поруч з вуглецем входять деякі хімічні елементи. Це насамперед водень, кисень, азот, сірка, галогени і фосфор. Інші елементи рідко зустрічаються в органічних сполуках; органічні речовини, які містять благородні гази, невідомі.
Не дивлячись на значну кількість елементів, які входять до складу неорганічних сполук, кількість органічних сполук набагато переважає кількість неорганічних. Сьогодні відомо понад сім мільйонів органічних речовин.
Однією з важливих особливостей органічних сполук, яка накладає відбиток на всю хімічну поведінку, є характер зв’язків між атомами в їх молекулах. У переважній більшості випадків ці зв’язки мають яскраво виражений ковалентний характер. Тому органічні сполуки, як правило, не дисоціюють на іони і порівняно повільно взаємодіють один з одним. Тоді як реакції між електролітами в розчинах протікають майже миттєво, час, необхідний для завершення тієї або іншої реакції між органічними речовинами, звичайно вимірюється годинами, а іноді і днями. От чому в органічній хімії велике значення має застосування різних каталізаторів.
Інша характерна риса органічних сполук полягає в їхній схильності піддаватися при нагріванні без доступу повітря глибоким змінам, в результаті котрих утворюються нові речовини, які мають абсолютно інші властивості. Якщо ж вести нагрівання при доступі повітря або у присутності окисників, то органічні речовини згорають, причому вуглець і водень що входять до їх складу цілком перетворюються на двоокис вуглецю і воду, а азот звичайно виділяється у вільному стані. На цьому заснований елементний аналіз органічних речовин: вміст вуглецю і водню в згорілій речовині визначають за кількістю двоокису вуглецю і води, які утворилися, азот, що виділився, вимірюють безпосередньо, а вміст кисню встановлюють за різницею між вагою згорілої речовини і вагою решти елементів, що містилися в ньому. Дані аналізу і визначення молекулярної ваги дозволяють вивести молекулярну формулу органічної речовини. Проте на відміну від неорганічних сполук молекулярна формула органічної речовини ще не дає уявлення ні про його характер, ні про його властивості. Річ у тому, що відомо дуже багато органічних сполук, які мають однаковий склад і однакову молекулярною вагу, але абсолютно різні фізичні і навіть хімічні властивості.
Це явище, широко поширене серед органічних сполук, одержало назву ізомерії, а речовини, що відповідають одній і тій же молекулярній формулі, але відрізняються за своїми властивостями, називаються ізомерами.
Пояснення різних випадків ізомерії дає теорія будови органічних сполук, створена в шестидесятих роках позаминулого сторіччя Бутлеровим, згідно з якою властивості речовин визначаються не тільки їх якісним і кількісним складом, як вважали раніше, але і внутрішньою будовою молекул, певним порядком з’єднаних між собою атомів, утворюючих молекулу. Цей внутрішній устрій Бутлеров назвав «хімічною будовою».
Особливо важливою була ідея Бутлерова про те, що атоми, з’єднуючись хімічно в певній послідовності відповідно до їх валентності, взаємно впливають один на одного таким чином, що частково змінюється їх власна природа, їх «хімічний зміст». Вчення Бутлерова про хімічну будову молекул складають теоретичну основу органічної хімії.
Теорія хімічної будови. Поняття «хімічна будова» вперше ввів О. М. Бутлеров у 1861 р. Він зауважував, що властивості речовин визначаються не тільки їхнім складом (якісним і кількісним), як вважалося раніше, а й внутрішньою структурою молекул, тобто порядком з'єднання атомів один з одним, які входять до складу молекули. Цей порядок і є хімічною будовою молекули. У поняття «хімічна будова» О. М. Бутлеров включав також характер зв'язку атомів, їхній взаємний вплив один на одного. Наприклад, водень і кисень, утворивши воду, настільки змінилися від взаємного впливу, що вода вже не має властивостей ні водню, ні кисню, хоча й містить Гідроген і Оксиген, що входили до складу відповідно водню і кисню. У молекулі фенолу С6Н5ОН бензольне ядро впливає на властивості гідроксильної групи, посилюючи її кислотність (аналогія зі спиртами):
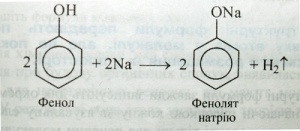
Гідроксильна група, у свою чергу, впливає на властивості бензольного ядра і полегшує заміщення в ньому атомів Гідрогену:

Так, на прикладах з неорганічної та органічної хімії ми спостерігаємо взаємний вплив атомів. Хімічну будову молекул виражають за допомогою структурних формул.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 4456; Нарушение авторских прав?; Мы поможем в написании вашей работы!