
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методи добування. У промисловості алкени вилучають із природних джерел (газоподібні – частково із природного газу, а рідкі – з нафти)
|
|
|
|
У промисловості алкени вилучають із природних джерел (газоподібні – частково із природного газу, а рідкі – з нафти).
Лабораторні методи. Дегідратація (внутрішньомолекулярна дегідратація одноатомних спиртів під дією зневоднюючих агентів – каталізаторів):
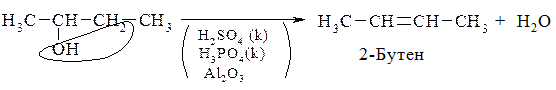
Локант, що позначає функціональну групу, виноситься перед назвою основного ланцюга: 2-бутен.
Відщеплення води йде відповідно правилу Зайцева:
При відщепленні бінарних сполук (води, галогеноводнів від відповідних похідних – спиртів, галогенопохідних) атом Гідрогену відщеплюється від менш гідрогенізованого атома Гідрогену, сусіднього до того, з яким сполучена функціональна група (в даному випадку гідроксил або галоген).
1. Відщеплення галогеноводнів від галогенопохідних алканів під дією спиртового розчину лугу (NaOH, KOH). Також іде відповідно до правила Зайцева.
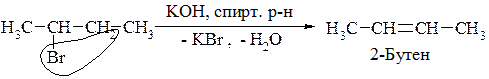
2. Відщеплення дигалогеніду цинку при дії цинкового пилу на віцинальні дигалогенопохідні:
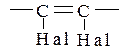
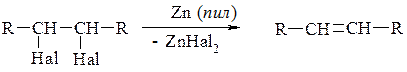
Віцинальні дигалогенопохідні – це такі, що мають атоми галогену при сусідніх атомах Карбону.
Гемінальні – мають обидві функціональні групи при одному атомі Карбону.
6.4. Хімічні властивості
Загальна характеристика. Оскільки в молекулах алкенів, крім міцних
σ-зв’язків наявний ще один малоактивний (слабкий) π-зв’язок, який легко рветься, то реакційна здатність алкенів зумовлена практично повністю саме реакціями з розривом π-зв’язку. До них належать такі групи реакцій, як:
· Приєднання по місцю розриву π-зв’язку;
· Деякі реакції окиснення;
· Полімеризація і співполімеризація;
· Крім того, є ряд реакцій, в яких розривається σ-зв’язок:
· Дія дуже сильних окисників (озон, HNO3, CrO3 тощо);
· Заміщення в насиченій частині ланцюга алкена за жорстких умов.
І. Реакції приєднання:
1. Гідрогенізація (гідрування) – приєднання Гідрогену:

2. Галогенування (хлорування, бромування, приєднання галогенів).
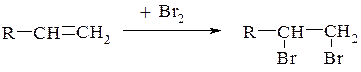
Якісна реакція на ненасичений зв’язок – знебарвлення бромної води (жовтого кольору) до алкену.
3. Гідрогалогенування – приєднання галогеноводнів, відбувається за правилом Марковнікова:
При приєднанні бінарних агентів HCl, HOCl до ненасиченого зв’язку позитивна частка прямує до більш гідрогенізованого атома Карбону. Причина напрямку реакції полягає у сумісній дії мезомерного і індукційного ефектів в молекулі алкенів.
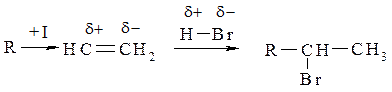
4. Гідратація – приєднання води, також іде відповідно до правила Марковнікова:
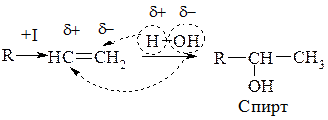
5. Гіпохлорування:
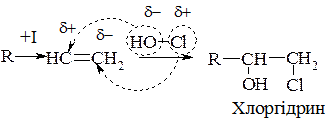
ІІ. Реакції окиснення.
1. Реакція Вагнера – дія холодного розведеного розчину калійперманганату на алкен; відбувається знебарвлення рожевого розчину. Якісна реакція на ненасичений зв’язок у молекулах алкенів.
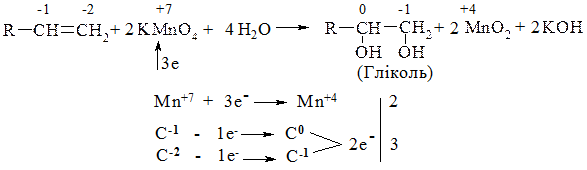
Дія кисню повітря в присутності срібного каталізатора:
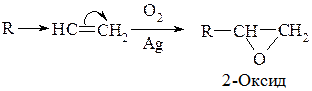
2. Озонування:
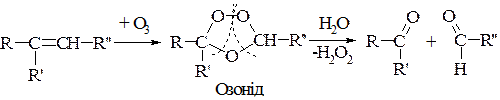
З того боку подвійного зв’язку, де не було атомів Гідрогену, утворюється кетон, а з того, де був атом Гідрогену – альдегід.
3. Дія сильних окисників приводить до повного розриву π- та σ-зв’язків:
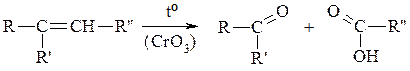
Доповнення до реакцій приєднання:
4. Приєднання за Харашем – приєднання галогеноводнів (у присутності пероксидів) до несиметричного подвійного зв’язку, іде проти правила Марковнікова (не за іонним, а за радикальним механізмом), при цьому Гідроген із молекули галогеноводнів прямує до менш гідрогенізованого атома Карбону при подвійному зв’язку:
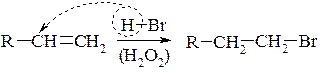
Реакцію каталізують органічні пероксиди, рідше пероксид водню:
ІІІ. Реакції полімеризації відбуваються з розривом π-зв’язку в низькомолекулярних алкенах і утворенням макромолекулярних полімерів, що складаються з великої кількості елементарних ланок.
Полімеризація – це процес утворення полімеру із мономерів без виділення побічних низькомолекулярних продуктів:

Співполімеризація (кополімеризація) – процес утворення полімеру із двох мономерів без виділення побічних низькомолекулярних продуктів.
Поліконденсація – процес утворення полімеру із мономерів, але він супроводжується виділенням низькомолекулярних, термодинамічно стійких побічних продуктів (наприклад, води).
IV. Ізомеризація.
Як правило, ізомеризація положення подвійного зв’язку відбувається за високих температур і проходить за радикальним механізмом.
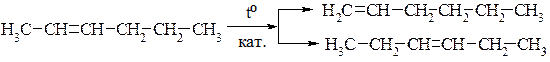
Практично такий процес використовується дуже рідко.
Примітка! При розв’язуванні задач на добування одного ізомеру з іншого треба використовувати перетворення, які однозначно приводять від одного ізомеру до іншого, а не до суміші можливих ізомерів.
Приклад: Від бутену-1 перейти до бутену-2.
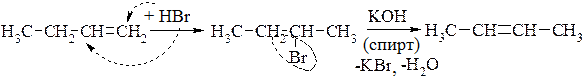
V. Високотемпературне галогенування гомологів етилену.
У разі галогенування за температур порядку 500 – 550°С реакція іде не за іонним механізмом приєднання, а за радикальним механізмом заміщення. При цьому заміщення відбувається в α-положенні до подвійного зв’язку.
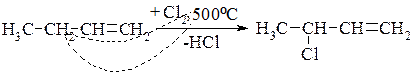
6.5. Просторова будова (стереохімія) алкенів (гомологів етену)
Заміщені етилени можуть існувати у вигляді цис- або транс- ізомерів:
1. Якщо два однакові замісники при двох атомах Карбону, що складають подвійний зв’язок, розташовані по один бік від площини подвійного зв’язку, то це цис-ізомер.
2. Якщо два однакові замісники при двох атомах Карбону, що складають подвійний зв’язок, розташовані по різні боки від площини подвійного зв’язку, то це транс-ізомери.

Але розглянутий вид просторової (геометричної) ізомерії є лише окремим випадком загального типу ізомерії, що називається E/Z – ізомерією (від двох німецьких слів – entgegen – навпроти; zusammen – разом).
В термінах E/Z – ізомерії можна розглядати гомологи етену, що мають чотири (або три) зовсім різні замісники біля подвійного зв’язку. Для цього спершу розглядається старший із замісників. Старшість замісників визначається тим, який атомний номер має атом замісника, що сполучається з атомом Карбону подвійного зв’язку.
Z-ізомер – має старші замісники біля атомів Карбону подвійного зв’язку знаходяться по один бік від площини подвійного зв’язку.
Е-ізомер – має старші замісники по різні боки подвійного зв’язку.
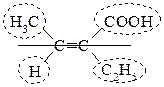
6.6. Окремі представники
Етен (етилен) – безбарвний, майже нерозчинний у воді газ. Горить світлим кіптявим полум’ям, утворює з повітрям вибухові суміші.
Етен міститься в значній кількості у коксових газах очистки нафтопереробних установок, з яких він добувається.
Етен використовують здебільшого для виробництва поліетилену, а також для добування етанолу, ацетальдегіду, вінілхлориду і стирену. Слід згадати про використання етену для прискорення дозрівання фруктів. Це дає змогу транспортувати недозрілі плоди до місця призначення, де вони дозрівають в атмосфері етену.
Пропен виділяють з газів нафтопереробки й у великій кількості використовують для синтезу ізопропанолу, поліпропілену і алілхлориду.
Бутени добувають у промислових масштабах з газів крекінгу або переробки нафти. 1-Бутен і ізомерні 2-бутени використовують для виробництва 1,3-бутадієну і 2-бутанолу. [1], c. 145-146; [2], с. 229-252.
Контрольні запитання та завдання
1. Напишіть структурні формули ізомерів (крім стереоізомерів) пентену, назвіть їх за номенклатурою IUPAC і (якщо можна) дайте їм альтернативні назви. Напишіть структурні формули продуктів, які утворюються під час озонолізу кожного з них.
2. Напишіть форми геометричних ізомерів: н- пентенів; монобромопропенів; ізопентенів.
3. Які алкени утворюються з наведених сполук? Напишіть рівняння відповідних реакцій:
(СН3)3ССl; (СН3)2С(ОН)С(СН3)3
4. Який алкен у кожній парі активніший у реакції приєднання Н2О? Дайте пояснення: а) етен або пропен; б) етен або вінілбромід; в) пропен або 2-бутен; г) 2-бутен або ізобутен;
д) 1-пентен або 2-метил-1-бутен.
5. Наведіть механізм реакцій:
СН3СН=СН2 + НОВr  ?
?
ССl3СН=СН2 + НОВr  ?
?
6. Напишіть структурні формули алкенів, у яких в під час озонолізу утворюються такі продукти: а) СН3СН2СН2СНО та НСНО; б) СН3СН(СН3)СНО та СН3СНО; в) тільки СН3СОСН3. Що дає кожний із цих алкенів у реакції з калійперманганатом?
7. Алкіни
Це вуглеводні, що містять один потрійний зв’язок. Загальна формула: CnH2n-2.
Ізомерія, як і в ряду алкенів, зумовлена:
а) ізомерією будови карбонового ланцюга;
б) ізомерією положення потрійного зв’язку в ланцюзі.
Номенклатура: раціональна (за основу беруть назву першого члена гомологічного ряду – ацетилен); систематична: 
Приклад:

|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3326; Нарушение авторских прав?; Мы поможем в написании вашей работы!