
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методи добування. Відщеплення галогеноводнів від віцинальних та гемінальних дигалогенопохідних:
|
|
|
|
Відщеплення галогеноводнів від віцинальних та гемінальних дигалогенопохідних:
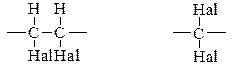
а) із віцинальних
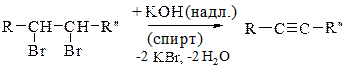
б) із гемінальних
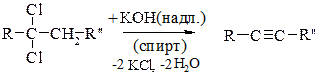
Як і у випадку алкенів, при відщепленні тут діє правило Зайцева, але можливе утворення ізомерних кумульованих дієнів:
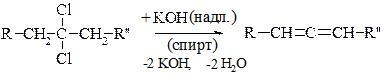
Алкілювання ацетилену галоїдними алкілами (галогеналканами). Метод добування гомологів етину буде розглянутий у хімічних властивостях алкінів.
7.2. Хімічні властивості
Потрійний зв’язок складається із σ-зв’язку, утвореного sp-гібридними орбіталями сусідніх атомів Карбону, а також двох π-зв’язків, утворених негібридизованими р -орбіталями і розташованих у двох взаємно перпендикулярних площинах.
Здавалося б, що маючи два π-зв’язки, алкіни повинні були б швидше, ніж алкени, вступати в реакції приєднання. В дійсності ж алкіни в цих реакціях є інертнішими за алкени. Наприклад, вони повільніше знебарвлюють жовтий розчин бромної води і рожевий розчин калійперманганату.
Це пояснюється тим, що електронна густина трьох із чотирьох орбіталей кожного атома Карбону в молекулах алкінів зосереджена в між’ядерному просторі.
Тому подвійний зв’язок є більш доступним для атакуючого агенту.
 .
.
Друга особливість реакційної здатності алкінів порівняно з алкенами полягає в тому, що для алкінів, на відміну від алкенів, характерні реакції заміщення атомів Гідрогену при ненасиченому зв’язку.
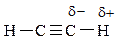
Внаслідок концентрації електронної густини в між’ядерному просторі відбувається поляризація зв’язків С–Н, тому атом Гідрогену легко вступає в реакції заміщення на інші атоми і групи.
Зокрема, ця здатність використовується для якісного виявлення кінцевого потрійного зв’язку, а також для добування гомологів ацетилену.
І. Реакції приєднання алкінів.
Алкіни вступають практично в усі ті реакції, що і алкени, але приєднання іде в дві стадії: спочатку з розривом одного π-зв’язку, а потім другого.
1. Гідрогенізація:
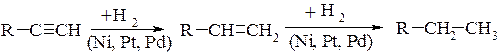
2. Галогенування:

3. Гідрогалогенування – іде за правилом Марковнікова, як у алкенів:
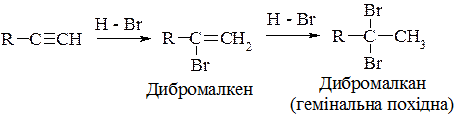
4. Приєднання води (гідратація) відрізняється від гідратації алкенів.
Гідратація алкінів за Кучеровим:

Правило Ельтекова: Гідроксил та аміногрупа не можуть існувати біля атома Карбону з подвійним зв’язком; такі сполуки вже в момент утворення підлягають перегрупуванню з переходом атома Гідрогену на інший кінець подвійного зв’язку.

В реакції Кучерова із ацетилену утворюється оцтовий альдегід, а з інших алкінів – кетони:
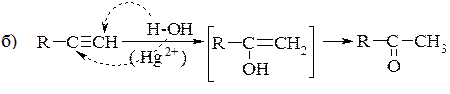
в) алкін, що має потрійний зв’язок в середині ланцюга, утворює два ізомерних кетони:

ІІ. Реакції окиснення.
Реакції окиснення дещо відрізняються від окиснення алкенів. Дія розведеного розчину перманганату приводить до утворення α-дикарбонільних сполук (порівняти з реакцією Вагнера).

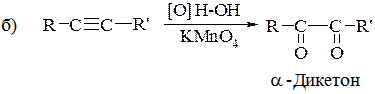
ІІІ. Реакції подовження ланцюга.
Димеризація ацетилену:

При приєднанні молекул водню до вінілацетилену переважно утворюється бутадієн-1,3. Оскільки така система стабілізована кон’югацією (тобто при її утворенні виділяється додаткова порція енергії – статичний ефект кон’югації), порівняно з іншим можливим ізомером – етилацетиленом.
IV. Реакції заміщення атома Гідрогену біля потрійного зв’язку.
1. Алкілювання ацетилену галоїдними алкілами:
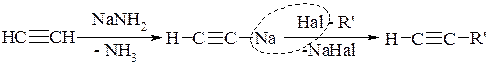
2. Якісна реакція на кінцевий потрійний зв’язок (якісна реакція на атом Гідрогену біля потрійного зв’язку) – утворення осадів ацетиленідів одновалентного Купруму або Аргентуму (Cu або Ag):

3. Реакція Фаворського-Шостаковського – взаємодія алкінів з органічними кислотами і спиртами:
а) взаємодія зі спиртами:
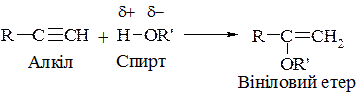

б) взаємодія з карбоновими кислотами:

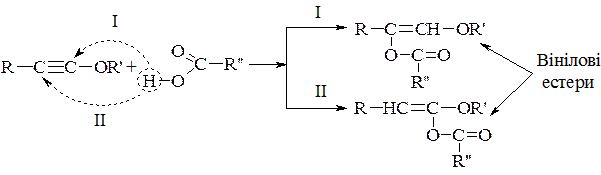
4. Реакція Фаворського-Назарова – реакція взаємодії алкінів, що мають потрійний зв’язок, з оксосполуками (альдегідами чи кетонами).
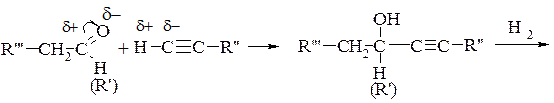

7.3. Окремі представники
Ацетилен – безбарвний газ з ефірним запахом, виявляє наркотичну дію, слабко розчиняється у воді, дещо краще – в ацетоні. Вперше був добутий
Ф. Велером (1862 р.) гідролізом кальцій карбіду.
З повітрям ацетилен утворює вибухові суміші. Під час спалювання ацетилену в чистому кисні температура підвищується до 2700°С, тому ацетилен використовується для автогенного зварювання. Крім того, ацетилен є вихідною сполукою для виробництва пластичних мас і синтетичного каучуку.
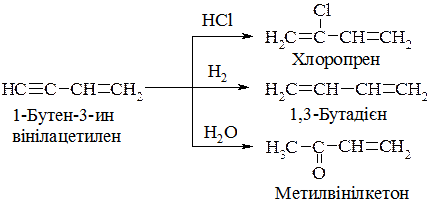
Вінілацетилен (1- бутен -3- ін) – газоподібний вуглеводень (Ткип = -5°С), утворюється під час димеризації ацетилену. Під дією хлороводню перетворюється на хлоропрен (2-хлоро-1,3-бутадієн), полімеризація якого дає малостійкі хлоропренові каучуки. Під час гідратації вінілацетилену утворюється також важлива сполука – метилвінілкетон; неповне гідрування дає 1,3-бутадієн:
[1], c. 167-176; [2], с. 268-280.
Контрольні запитання та завдання
1. Напишіть структури ізомерів гексину та вкажіть їх назви за номенклатурою IUPAC.
2. Опишіть прості хімічні реакції, за допомогою яких можна розрізнити етан, етилен, ацетилен.
3. Яка геометрія молекул 1-бутину; 2-бутину; 2-гептен-5-іну?
4. Напишіть схеми синтезу з ацетилену наведених нижче сполук, використовуючи будь-які органічні та неорганічні реагенти: а) 1,1-дибромоетану; б) ацетальдегіду; в) пропіну; г) 2-бутину; д) транс -2-бутену.
5. Закінчте наведені нижче рівняння, прокоментуйте їх та вкажіть назви усіх органічних сполук:

8. Алкадієни
Це вуглеводні, що мають в молекулах два подвійні зв’язки. Загальна формула: CnH2n-2.
Цей клас ізомерний класу алкінів, що мають таку саму загальну формулу.
8.1. Ізомерія алкадієнів
Ізомерія карбонового скелету – ізомерія взаємного розташування подвійних зв’язків.
8.2. Класифікація
За взаємним розташуванням подвійних зв’язків у молекулі алкадієни поділяються на три групи:
o кумульовані – такі, де обидва подвійні зв’язки знаходяться при тому самому атому Карбону:

o ізольовані – такі, де між двома подвійними зв’язками (етиленовими зв’язками) знаходиться одна або декілька метиленових або заміщених метиленових груп:
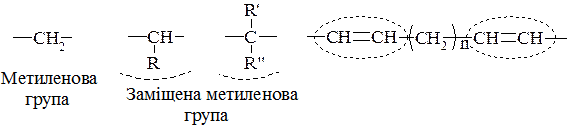
o кон’юговані – такі, що містять угруповання:

ця група є найцікавішою з теоретичної точки зору і найкориснішою з практичної точки зору, зокрема для добування каучуків.
Пі (π) – кон’югація
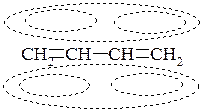
Не існує окремих електронних хмаринок кожного з π-зв’язків. Ці хмаринки (не маючи жорсткої матеріальної межі) взаємо проникають одна в одну, тобто кон’югуються (зчіплюються), утворюючи єдину молекулярну π-електронну хмаринку, у якої кожен з π-електронів не належить якомусь окремому «своєму» атому, а належить усій кон’югованій системі. Таким чином, електронна густина кожного з електронів цієї системи делокалізована. Це дає змогу в такій системі здійснюватися мезомерному ефекту.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 1659; Нарушение авторских прав?; Мы поможем в написании вашей работы!