
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Циклоалкани
|
|
|
|
Це вуглеводні, в молекулах яких присутні циклічні карбонові ланцюжки і наявні лише прості зв’язки.Загальна формула CnH2n.
Циклоалкани, або циклани, ізомерні алкенам.
9.1. Номенклатура. Ізомерія
Номенклатура практично така ж сама, як в алканів, але з додаванням префіксу цикло- перед назвою замкненого карбонового ланцюга. Нумерація циклу починається від замісника, ближчого до початку алфавіту.
1. Ізомерія циклів.
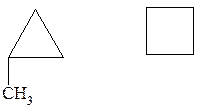
2. Ізомерія взаємного розташування замісників у циклі.
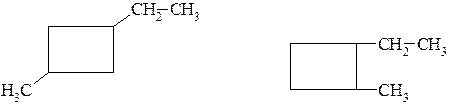
3. Ізомерія будови бічного ланцюга.

9.2. Будова циклоалканів
Першою теорією, яка намагалася пояснити стабільність циклоалканів та їх реакційну здатність, була теорія А. Байєра. В своїй теорії він виходив з того, що валентні кути в молекулах циклоалканів відхиляються від нормального кута між валентними напрямками sp3-гібридизованого атома Карбону. Кут між валентними напрямками в молекулі циклопропану за Байєром дорівнює внутрішньому куту трикутника і становить 60°. 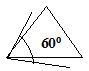 Напруження циклу – α — визначається половиною різниці між нормальним кутом 109° і внутрішнім кутом відповідного багатокутника.
Напруження циклу – α — визначається половиною різниці між нормальним кутом 109° і внутрішнім кутом відповідного багатокутника.
Для циклопропану 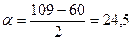 .
.
Для циклобутану  ,
, 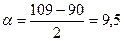 .
.
Дійсно, циклопропан та циклобутан поводять себе у хімічних реакціях так, ніби їх зв’язки напружені і намагаються якнайшвидше розірватись.
З гіпотези А. Байєра випливає, що найстабільнішим циклоалканом є циклопентан, внутрішній кут якого (108°) практично співпадає з нормальним валентним кутом sp3-гібридизованого атома Карбону. Проте, гіпотеза А. Байєра більш-менш задовільно пояснюючи властивості малих циклів, не може пояснити властивості циклогексану. За Байєром циклогексан повинен мати негативне значення напруги циклу 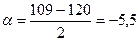 .
.
В дійсності ж циклогексан є найстабільнішим із циклів, стабільнішим ніж циклопентан.
Основними причинами хибності гіпотези А. Байєра є такі:
1. Хибною була вихідна установка гіпотези на деформацію валентних кутів, таких деформацій не відбувається, оскільки вони вимагали б надзвичайно високих енергій.
2. А. Байєр не враховував і не міг врахувати електронну будову циклоалканів, тому що за його часів не були розвинені квантово-хімічні уявлення про будову хімічних зв’язків.
3. Нарешті, А. Байєр вважав молекули циклоалканів плоскими багатокутниками, тобто зовсім не враховував можливого просторового взаємного розташування атомів у циклах.
9.3. Сучасні уявлення про будову малих циклів
В малих циклах – циклопропані і циклобутані – існує особливий тип зв’язків – «бананові зв’язки».

При цьому sp3-гібридні орбіталі перекриваються під кутом, тому зона перекривання менша, ніж в σ-зв’язках, що послаблює цей зв’язок порівняно з σ-зв’язком. До того ж притягання іде по дотичній (подібно до
π-зв’язку), що також послаблює цей зв’язок порівняно з σ-зв’язком. За міцністю такий зв'язок знаходиться між σ- та π-зв’язком, наближаючись до π-зв’язку (легко рветься). Тому циклоалкани за реакційною здатністю нагадують алкени: вступають в реакції приєднання з розривом зв’язку, а значить і розривом циклу.
9.4. Стереохімія циклоалканів
Всупереч твердженню А. Байєра, жоден з циклоалканів не є плоскою структурою. Найбільш плоским з усіх є циклопропан, але навіть в ньому відбуваються коливання атомів Карбону з виходом із площини.
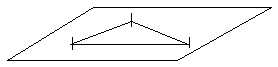
Циклобутан не є плоским квадратом, а в його молекулі відбувається коливання «крилець».

Циклопентан існує у вигляді «конверта», в якому почергово піднімаються і опускаються кожна з п’яти вершин.
Найцікавішою і найскладнішою є просторова будова циклогексану і його похідних.
Конформації молекули циклогексану. Циклогексан може існувати у вигляді трьох конформерів:

В конформації «крісло» кожна пара атомів Карбону, якщо дивитись вздовж зв’язку, знаходиться у загальмованій конформації.
В конформації «човника» дві пари атомів Карбону знаходяться в заслоненій конформації, тому човник менш імовірний, ніж крісло.
Молекула в конформації «крісло» підвержена осциляції:

Як собі уявити утворення крісла із плоского шестикутника?
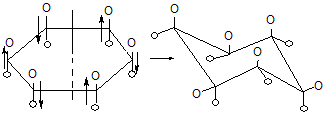
Молекула циклогексану може приймати дві кріслоподібні конформації. При переході від однієї конформації до другої атоми Гідрогену стають екваторіальними або аксіальними.
Енергія переходу невелика і такі переходи відбуваються у звичайних умовах (20°С):

9.5. Окремі представники
Циклопропан – безбарвний газ, використовується як нешкідливий дихальний наркотичний засіб. Цілий ряд природних сполук містять кільце циклопропану (наприклад, терпени).
Циклобутан – газоподібна речовина. Біциклічні монотерпенові вуглеводні (α- і β-пінен), деякі алкалоїди містять кільце циклобутану.
Циклопентан, циклогексан виділяють із нафти. Циклогексан є безбарвною рідиною з приємним запахом. Використовується як розчинник і як вихідна сировина для виробництва поліамідів. У природних сполуках міститься значна кількість похідних циклогексану. [1], c. 176-183; [2], c. 567-580.
10. Арени (Ароматичні вуглеводні)
Арени – це вуглеводні, в молекулах яких наявний циклічний ланцюг атомів Карбону i особливий тип зв’язку (ароматичний зв’язок). Розглянемо основні принципи виникнення i характеристики ароматичного зв’язку на прикладі найпростішої ароматичної сполуки – молекули бензену C6H6.
При переході від циклогексану до циклогексадієну, що мають один і два подвійних зв’язки відповідно, і далі до циклогексатрієну (бензену) відбувається якісний стрибок, оскільки ароматичні сполуки принципово відрізняються за своїми властивостями від циклогексенових і циклогексадієнових похідних.
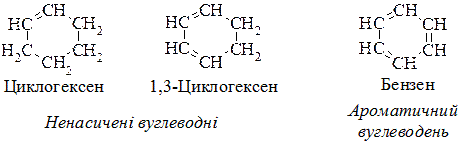
Назва «ароматичні вуглеводні» виникла на початку розвитку органічної хімії. До групи ароматичних вуглеводнів відносяться речовини, які добували з природних смол, бальзамів і ефірних масел, що мали приємний запах (аромат).
Але в дійсності далеко не всі ароматичні вуглеводні мають запах.
10. 1. Класифікація ароматичних сполук
Класифікація ароматичних сполук відбувається за такими ознаками׃
І. За кількістю ароматичних кілець׃
а) одноядерні (бензен і його гомологи);
б) двохядерні та багатоядерні, які в свою чергу поділяються на:
- багатоядерні з неконденсованими циклами;
- багатоядерні з конденсованими циклами.
Наприклад׃



Багатоядерних арени з конденсованими ядрами часто мають сильні канцерогенні властивості. Особливо багато таких сполук у нафтовому пеку (залишок після перегонки нафти), який використовується для асфальтування вулиць.
10.2. Ароматичні вуглеводні з одним бензеновим ядром
Загальна формула групи вуглеводнів з одним ядром СnН2n-6. Найпростішим представником ароматичних вуглеводнів з одним ядром є бензен. За даними якісного та кiлькiсного елементного аналізу, бензен має брутто-формулу — C6H6. Його відкрив М.Фарадей (1825 р.) у світильному газі (продукт переробки кам’яного вугілля). Пізніше (1845 р.) бензен був виявлений Гофманом у кам’яновугільній смолі.
|
|
|
|
|
Дата добавления: 2015-05-24; Просмотров: 3186; Нарушение авторских прав?; Мы поможем в написании вашей работы!