
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химическое равновесие в гетерогенной среде
|
|
|
|
Гетерогенной называется такая система, в которой есть поверхности разделамежду частями или фазами ее. Такие системы наряду с газовой могутсодержать конденсированные фазы — жидкие или твердые.
Рассмотрим возможность применения закона действующих масс к подобным системам. Для примера возьмем реакцию диссоциации углекислого кальция. Ее гетерогенный характер подтверждается тем, что в ней одновременно присутствуют два твердых и одно газообразное
вещество:

Наличие в этой реакции веществ в конденсированном, в частности в твердом, состоянии определяет особенности рассматриваемого процесса.
Над поверхностью любого из них образуется насыщенный пар, давление или упругость которого в условиях неизменности состава твердых фаз определяется только температурой процесса. Так как упругость паров Рсасо3 и Рсао для данной температуры постоянна и весьма мала, их величина не входит в уравнение равновесия и тогда
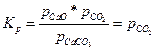
Соответственно, для таких реакций применение закона действующих масс достаточно просто: в этом случае константа равновесия реакции определяется парциальным давлением газа.
В подобных процессах при известных условиях реакция может практически дойти до конца, если, например, образующуюся газообразную углекислоту С02 непрерывно удалять из зоны реакции.
При расчете констант равновесия, например гетерогенных жидких систем или крепких растворов, часто возникают серьезные трудности. Кроме состояния равновесия, иногда требуется найти скорость протекания реакции на различных стадиях процесса. Эта величина зависит от таких физических параметров, как вязкость, скорость диффузии, дисперсность и пр. Скорость большинства реакций, с которыми мы сталкиваемся при сварке, современными методами расчета определить затруднительно, и потому скорость реакций физико-химических процессов оценивается качественно.
|
|
|
|
|
Дата добавления: 2015-06-26; Просмотров: 447; Нарушение авторских прав?; Мы поможем в написании вашей работы!