
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термод. потен-лы идеального газа
|
|
|
|
Мех-е и калор-кие урав-я сост-ния.
Запишем термод. потенциалы
dU = TdS – pdV
dH = TdS + VdP
dF = -SdT – pdV
dG = Vdp – SdT
Как и термодинам. потенциалы, так и их произ-ные имеют физич. смысл. Найдем произ-ные всех потен-лов по мех. переменным (V,p):
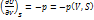
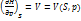 (1)
(1)
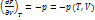
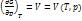
Система (1) дает нам знач-я p и V, как функция Т и одной из мех. перем-ой или как ф-я S и мех. переменной. Уравнения в системе (1) наз-ся механическими уравнениями состояния.
Теперь возьмем произ-ные по термич. переменным (S, T):

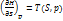 (2)
(2)

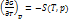
Уравнения входящ. в сист. (2) яв-ся КАЛОРИЧЕСКИМИ уравнениями состояния.
Св-ва ид. газа будут выражаться след. соотношениями:
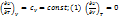
pV = RT (ур-ние состояния)
Найдем энтропию идеаль. газа
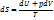
Поскольку для идеаль. газа
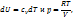
изменение энтропии м.б. записано в след. виде
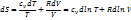
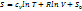 (2)
(2)
Интегрируя первое ур-ние, получим
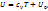 (3)
(3)
где U0 – пост-ная интегрирования
Фор-лы (2) и (3) позволяют найти новые соотношения для термод. потенциалов:
1) 
2)Для своб. эн-гии Гельмгольца:

3)Для эн-гии Гиббса
 )
)
4) Для энтропии:
 )
)
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 312; Нарушение авторских прав?; Мы поможем в написании вашей работы!