
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лабораторная работа. Определение основано на том, что при пропускании раствора соли через колонку с катионитом в Н-форме катионы соли обмениваются на ионы водорода
|
|
|
|
ЛАБОРАТОРНАЯ РАБОТА
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СОЛИ (CuSO4, NiSO4, KCl, NaCl) В РАСТВОРЕ С ПРИМЕНЕНИЕМ КАТИОНИТА
Определение основано на том, что при пропускании раствора соли через колонку с катионитом в Н-форме катионы соли обмениваются на ионы водорода, при этом выделяется кислота в количестве, эквивалентном содержанию соли в растворе. Количество выделившейся кислоты определяют титрованием щелочи.
Процесс катионного обмена можно представить следующим уравнением:
2R-H + CuSO4 → R2-Cu + H2SO4
В большинстве случаев ионный обмен проводят в водной среде, при этом можно определить содержание в растворе любой соли, если соль и соответствующая кислота хорошо растворимы в воде.
Для определения гидролизующихся солей применяют ионный обмен в неводных средах. В качестве сильнокислотных катионитов в этом случае можно использовать катиониты марки СДВ-3, КУ-2 и др. в Н-форме.
Методика определения. Отбирают пипеткой 10 мл анализируемого (~0,1н) раствора соли из мерной колбы и помещают в колонку (диаметр 20 мм, высота 300 мм), содержащую 15 г сильнокислотного катионита в Н-форме. Раствор пропускают через катионит со скоростью 10 мл/мин (примерно 2 капли в 1 с). Вытекающий из колонки раствор собирают в коническую колбу емкостью 300 мл. Затем через катионит пропускают 60 – 100 мл дистиллированной воды, наливая, её из промывалки отдельными порциями по 10 – 15 мл. Новую порцию воды наливают тогда, когда уровень жидкости в колонке достигнет поверхности катионита.
Полноту вымывания выделившейся кислоты проверяют по метиловому оранжевому; для этого отбирают на часовое стекло каплю вытекающего из колонки раствора и прибавляют индикатор. Если при этом окраска раствора станет оранжевой, то считают, что кислота полностью вымыта из катионита. Промывные воды тщательно собирают в ту же коническую колбу. Всё содержимое конической колбы оттитровывают стандартным 0,1 н раствором NaOH в присутствии метилового оранжевого. Определение проводят 2 – 3 раза, пропуская раствор соли через ту же колонку.
Расчет. Содержание соли (m) вычисляют (в мг) по формуле:
m = MЭсолиVNaOH CNaOH(VK/VA)
где VK – общий объем исследуемого раствора, мл;
VA – объем анализируемого раствора, мл
После окончания определения катионит регенерируют, т.е. снова переводят в Н-форму. Для этого через колонку с катионитом пропускают 200 мл 2 н раствора HCl для извлечения поглощенных катионитов, затем отмывают катионит от кислоты дистиллированной водой и до следующего определения катионит сохраняют в колонке, заполненной водой.
Определение содержания соли (NaCl, KCl) в растворе с применением анионита
Определение основано на том, что при пропускании раствора соли NaCl ( KCl) через колонку с сильноосновными анионитом в ОН-форме анионы соли (Cl-) обмениваются на ОН—ионы, при этом образуются щелочь в количестве, эквивалентном содержанию соли в растворе. Анионный обмен можно представить следующим уравнением:
R-OH + NaCl → R-Cl + NaOH
Методика определения. Отбирают пипеткой 10 мл анализируемого (~0,1н) раствора соли из мерной колбы и помещают в колонку (диаметр 20 мм, высота 300 мм), содержащую 15 г сильноосновного анионита АВ-17 в ОН-форме, подготовленного, как указано в предыдущей методике. Раствор пропускают через анионит со скоростью 1 капля в 1с. Вытекающий из колонки раствор собирают в коническую колбу емкостью 300 мл. Затем через анионит пропускают дистиллированную воду, наливая её в колонку из промывалки отдельными порциями по 10 – 15 мл. Промывные воды тщательно собирают в ту же коническую колбу. Новую порцию воды наливают тогда, когда уровень жидкости в колонке достигнет поверхности анионита.
Для вымывания щелочи пропускают через колонку около 100 мл воды, полноту вымывания проверяют по фенолфталеину (отбирают каплю фильтрата на часовое стекло). Всё содержимое конической колбы оттитровывают стандартным 0,1 н раствором НСl в присутствии фенолфталеина.
На одной колонке проводят 2 – 3 измерения.
Расчет. Содержание соли (m) вычисляют (в мг) по формуле:
m = MЭсолиVHCl CHCl(VK/VA)
где VK – общий объем исследуемого раствора,мл;
VA – объем анализируемого раствора,мл
Для последующих определений анионит регенерируют, т.е. переводят в ОН-форму. Для этого через колонку с анионитом пропускают 300 мл 1 н раствора NaOH. Затем анионит отмывают от избытка щелочи дистиллированной воды.
ЛАБОРАТОРНАЯ РАБОТА
ОПРЕДЕЛЕНИЕ ХЛОРОВОДОРОДНОЙ И УКСУСНОЙ КИСЛОТ
МЕТОДОМ КОНДУКТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
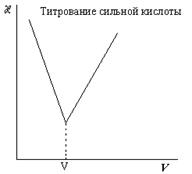
Краткое теоретическое вступление: Определение основано на последовательном взаимодействии с раствором сильного основания NaOH кислот, отличающихся друг от друга степенью ионизации. В первую очередь взаимодействует сильная кислота, что вызывает резкое понижение электролитической проводимости раствора вследствие связывания высокоподвижных ионов водорода: Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
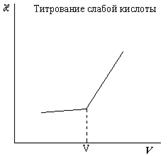
При титровании слабой кислоты проводимость обычно возрастает, так как вместо слабого электролита образуется хорошо диссоциирующая соль: Na+ + OH- + СН3СООН = Na+ СН3СОО- + H2O.
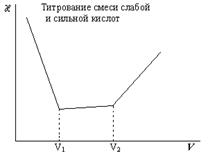
И, наконец, после точки эквивалентности проводимость резко возрастает благодаря появлению в растворе гидроксильных ионов, обладающих высокой подвижностью. V1 – объем щелочи, пошедший на титрование соляной кислоты; V2 – объем щелочи, пошедший на титрование суммы соляной и уксусной кислот.
Цель работы: ознакомление с принципом работы кондуктометра;
определение содержания в исследуемом растворе уксусной и хлороводородной кислот
Ход выполнения:
1.Стандартизация раствора NaOH по HCl. В стакан помещают 10 мл стандартного раствора соляной кислоты, добавляют дистиллированную воду до полного погружения ячейки (электродное отверстие должно быть полностью погружено в раствор); включают магнитную мешалку. При титровании приливают раствор NaOH порциями по 0,5 мл и каждый раз записывают значение удельной электропроводности и объем титранта, пока не обнаружат точку эквивалентности (излом на кривой титрования), соответствующую данной реакции. После этого снимают показания еще в 4 – 5 точках. По полученным данным строят кривую титрования в координатах удельной электропроводности – объем титранта, мл. Находят объем титранта в точке эквивалентности, Vэкв, и рассчитывают концентрацию раствора NaOH.
2. Анализ исследуемого раствора. Исследуемый раствор, содержащий смесь HCl и СН3СООН, доводят до метки, отбирают 10 мл, полученного раствора и переносят в стакан, добавляют воду до полного погружения ячейки и включают мешалку. Титруют раствором NaOH, приливая его порциями по 0,5 мл и в каждой точке записывая сопротивление раствора. Титрование прекращают после того, как будут обнаружены два излома на кривой титрования. Строят кривую титрования, по которым находят V1 и V2.
Обработка результатов:
Таблица 1. Значения удельной электропроводности при стандартизации гидроксида натрия
| Объем NaOH, V, мл | Показание прибора, χ |
| 0,5 | |
| ... |

Таблица 2. Значения удельной электропроводности при титровании смеси кислот
| Объем NaOH, V, мл | Показание прибора, χ |
| 0.5 | |
| … |
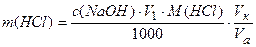
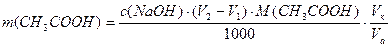
Выводы:
|
|
|
|
|
Дата добавления: 2015-06-04; Просмотров: 2268; Нарушение авторских прав?; Мы поможем в написании вашей работы!