
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методика решения типовых заданий. Задание.Почему кислород в соединениях всегда двухвалентен, а элемент его подгруппы сера способен проявлять валентности II
|
|
|
|
Задание. Почему кислород в соединениях всегда двухвалентен, а элемент его подгруппы сера способен проявлять валентности II, IV и VI?
Решение:
Электронная формула атома кислорода:
8O 1s22s22p4.
Электронно-графическая схема распределения электронов по квантовым ячейкам внешнего (валентного) уровня имеет вид:
s p
| n = 3 | ↑↓ | ↑↓ | ↑ | ↑ |
Исходим из определения, что количественной мерой валентности является число неспаренных электронов у атома в основном или возбуждённом состоянии.
Число неспаренных электронов на внешнем уровне равно двум. На данном (втором) энергетическом уровне отсутствуют вакантные орбитали. Возбуждённые состояния с переходом в более высокую валентность энергетически целесообразны при распаривании электронов в рамках одного уровня и не могут в этом случае измениться. Поэтому кислород во всех соединениях двухвалентен.
Электронная формула атома серы:
16S 1s22s22p63s23p4.
Электронно-графическая схема распределения электронов по квантовым ячейкам внешнего (валентного) уровня имеет вид:
s p d
| n = 3 | ↑↓ | ↑↓ | ↑ | ↑ |
Число неспаренных электронов на внешнем уровне, а значит и валентность, равно двум.
В отличие от атома кислорода у атома серы имеются вакантные орбитали на внешнем энергетическом уровне. Поэтому для него возможен переход в возбуждённые состояния с распариванием электронов:
s p d
| n = 3 | ↑↓ | ↑ | ↑ | ↑ | ↑ |
Число неспаренных электронов на внешнем уровне, а значит и валентность, равно четырём.
s p d
| n = 3 | ↑ | ↑ | ↑ | ↑ | ↑ | ↑ |
Число неспаренных электронов на внешнем уровне, а значит и валентность, равно шести.
Задания к самостоятельной работе
11. Какие валентности могут проявлять в соединениях: а) Be; б) F; в) Cl? Почему?
12. Какие валентности могут проявлять в соединениях: а) Al; б) C; в) Ca? Почему?
13. Используя метод валентных связей, опишите образование и пространственную форму молекулы BF3 и иона BF 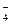 .
.
14. Используя метод валентных связей, опишите образование и пространственную форму молекулы CF4.
15. Используя метод валентных связей, опишите образование и пространственную форму молекулы NH3 и иона NH4+.
16. В чём сущность явления гибридизации электронных орбиталей? Какие формы имеют основные виды гибридных орбиталей? Каково их взаимное раположение?
17. На основе метода валентных связей и молекулярных орбиталей объясните почему энергия диссоциации O2 выше, чем F2.
18. Какие типы кристаллических решёток имеют NaCl, HCl, N2, C? Расположите эти вещества в ряд по возрастанию температуры плавления.
19. Какая химическая связь называется водородной? Приведите примеры. На какие виды подразделяется межмолекулярное взаимодействие?
20. Объясните аномально высокие значения температур плавления и кипения H2O и HF.
|
|
|
|
|
Дата добавления: 2015-07-02; Просмотров: 1450; Нарушение авторских прав?; Мы поможем в написании вашей работы!