
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Методика решения типовых заданий. Задание. Определить величину электродного потенциала никеля, опущенного в раствор NiSO4 c концентрацией 0,1 М при 25 0С
|
|
|
|
Задание. Определить величину электродного потенциала никеля, опущенного в раствор NiSO4 c концентрацией 0,1 М при 25 0С.
Решение:
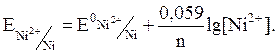 .
.
Концентрация ионов Ni2+ равна концентрации сульфата никеля, так как последний диссоциирует следующим образом:
NiSO4⇄Ni2+ + 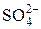 , тогда
, тогда 
Задания к самостоятельной работе
71. Рассчитайте значения  при концентрациях Mg2+, равных 1,0; 0,1; 0,001 моль/л. Сделайте вывод об изменении значения электродного потенциала с разбавлением.
при концентрациях Mg2+, равных 1,0; 0,1; 0,001 моль/л. Сделайте вывод об изменении значения электродного потенциала с разбавлением.
72. ЭДС гальванического элемента, составленного из медного электрода (катод), опущенного в раствор CuSO4 с концентрацией 0,01 моль/л, и электрода из неизвестного металла, опущенного в раствор с [Me2+]=1 моль/л, равна 0,532 В. Какой это металл?
73. Гальванический элемент состоит из металлического цинка, погруженного в 0,1 М раствор Zn(NO3)2, и металлического свинца, погружённого в 0,01 M раствор Pb(NO3)2. Вычислите ЭДС элемента, составьте его схему.
74. Гальванический элемент состоит из двух серебряных электродов, опущенных в растворы AgNO3, ЭДС этого элемента равна 0,118 В. Концентрация AgNO3 у одного электрода (катода) равна 0,05 моль/л. Чему равна концентрация AgNO3 у другого электрода?
75. Вычислите ЭДС гальванического элемента, образованного двумя никелевыми электродами, находящимися в растворах NiSO4 с концентрациями 0,01 и 0,0001 моль/л. Как называются элементы такого типа?
76. Составьте схему гальванического элемента, составленного из кобальтовой и железной пластин, опущенных в раствор их сульфатов. Вычислите ЭДС этого элемента, если [CoSO4]=0,01 моль/л, а [FeSO4]=0,0001 моль/л.
77. Вычислите ЭДС гальванического элемента, состоящего из медной и магниевой пластин, опущенных в растворы своих солей с концентрацией [Cu2+]=[Mg2+]=0,01 моль/л.
78. При какой концентрации ионов Cu2+ значение медного электрода становится равным 0,224 В?
79. Опишите принцип работы и приведите уравнения процессов, протекающих при разрядке и зарядке свинцового кислотного аккумулятора.
80. Опишите принцип работы и приведите уравнения процессов, протекающих при разрядке и зарядке никелевого щелочного аккумулятора.
|
|
|
|
|
Дата добавления: 2015-07-02; Просмотров: 2248; Нарушение авторских прав?; Мы поможем в написании вашей работы!