
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химический потенциал
|
|
|
|
Рассмотренные выше соотношения относятся к однородной системе, состояние которой характеризуются двумя параметрами. Если система содержит несколько компонент, то состав системы должен быть включен в число основных параметров. В простейшем случае состав задается указанием числа молей:  . Иными словами,
. Иными словами,
 ,
,
а, следовательно,
 .
.
Производные

называются химическим потенциалом i-го компонента.
Химический потенциал показывает насколько увеличивается потенциал системы при добавлении к ней одного моля данного вещества. Для любого компонента он зависит в общем случае от состава смеси.
Исключение составляют идеальные газы. В этом случае химические потенциалы компонент не зависят от их содержания в системе:
 ,
,
и для смеси
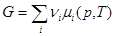 ,
,
где 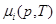 - мольный термодинамический потенциал Гиббса компонента, взятого в чистом виде.
- мольный термодинамический потенциал Гиббса компонента, взятого в чистом виде.
Как мы видели, химический потенциал идеального газа совпадает с
мольным потенциалом Гиббса. По определению для одного моля
 .
.
Входящую в формулу энтальпию можно выразить через теплоемкости:
 , (2.1.23)
, (2.1.23)
где Н 0 - энтальпия газа при температуре Т.
Энтропию можно найти из формулы, объединяющей первое и второе
начало термодинамики
 , (2.1.24)
, (2.1.24)
где  . Исключим из (2.1.24) мольный объем, выразив его через
. Исключим из (2.1.24) мольный объем, выразив его через
p и T из закона Клапейрона
V = R0T/p,
откуда
 ,
,
и
 .
.
Интегрируя обе части, найдем
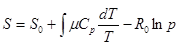 . (2.1.25)
. (2.1.25)
Подставляя (2.1.23) и (2.1.25) в выражение для потенциала Гиббса, получим
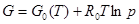 , (2.1.26)
, (2.1.26)
где
 G(T).
G(T).
Формула (2.1.26) выражает мольный потенциал идеального газа через
температуру и давление. Следовательно, химический потенциал i - ой
компоненты газовой смеси
 (2.1.27)
(2.1.27)
где р - парциальное давление этой компоненты.
Состав газовой смеси можно задать концентрациями с компонент. Концентрации определяются соотношением:
 ,
,
а, следовательно, из уравнения Клапейрона

следует, что

и
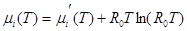 (T). (2.1.28)
(T). (2.1.28)
|
|
|
|
|
Дата добавления: 2015-06-27; Просмотров: 321; Нарушение авторских прав?; Мы поможем в написании вашей работы!