
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Гидролиз солей
|
|
|
|
Гидролизом соли называетсявзаимодействие ионов соли с молекулами воды, сопровождающееся изменением рН раствора. Гидролиз протекает только тогда, когда при взаимодействии ионов и воды образуются малодиссоциированные вещества. Известны следующие виды гидролиза солей.
1. Гидролиз по аниону.
В этом случае гидролизуются соли сильного основания и слабой кислоты, при этом реакция среды становится щелочной (рН > 7). Например
СН3СООNa ® СН3СОО – + Na+;
Na+ + HOH®реакция практически не идет;
СН3СОО – + HOH Û СН3СООН + ОН –,рН > 7.
Молекулярное уравнение гидролиза
СН3СООNa + HOH Û СН3СООН + NaОН.
Если анион многозарядный, то гидролиз протекает ступенчато, например
Na2CO3 + HOH Û NaHCO3 + NaOH;
I ступень гидролиза: CO 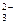 + HOH Û HCO
+ HOH Û HCO 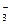 + OH –;
+ OH –;
II ступень гидролиза: НCO 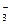 + HOH Û H2CO3 + NaOH.
+ HOH Û H2CO3 + NaOH.
Накапливающиеся в растворе ионы ОН –препятствуют протеканию II ступени гидролиза, поэтому практически гидролиз идет только по I ступени.
2.Гидролиз по катиону.
В этом случае гидролизуются соли слабого основания и сильной кислоты, при этом реакция среды становится кислой (рН < 7). Например
(NH4)2SO4 ® 2NH4+ + SO 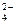 ;
;
SO 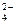 + HOH ® реакция практически не идет;
+ HOH ® реакция практически не идет;
NH4+ + HOH Û NH4OH + H+, рН < 7.
Молекулярное уравнение гидролиза
(NH4)2SO4 + HOH Û NH4OH + NH4HSO4 .
Гидролиз не доходит до конца, так как накопление в растворе ионов водорода препятствует образованию свободной кислоты.
3. Гидролиз по катиону и аниону одновременно.
Такому виду гидролиза подвергаются соли слабого основания и слабой кислоты. В реакции участвуют и катион, и анион соли. Реакция среды определяется относительной силой образующихся слабой кислоты и слабого основания. Если K Д (кислоты) > K Д (основания), то рН < 7; если K Д (кислоты)) < K Д (основания), то рН > 7, а когда K Д (кислоты) = K Д (основания), то рН» 7. Например
NH4COOH + HOH Û NH4OH + HCOOH, рН = 7,
так как K Д(HCOOH) = K Д(NH4OH) = 1,76 × 10-5.
4. Необратимый полный гидролиз.
Если кислота и основание, образующие соль, являются не только слабыми электролитами, но и малорастворимы или неустойчивы и разлагаются с образованием газообразных продуктов, то гидролиз, как правило, протекает практически необратимо, например
Al2S3 + 6HOH ® 2Al(OH)3¯ + 3H2S ;
2Al3+ + 3S2– + 6HOH ® 2Al(OH)3¯ + 3H2S .
Количественно гидролиз соли характеризуется степенью гидролиза h и константой гидролиза K г.
Степень гидролиза h показывает,какая часть соли находится в гидролизованном состоянии и выражается в долях единицы или в процентах
h = С г/ С 2, (51)
где С г – концентрация гидролизованной части соли; С 2– общая концентрация растворенной соли.
Расчет константы гидролиза K г и степени гидролиза h следует вести по формулам:
1) гидролиз по аниону
K г = 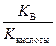 , h =
, h = 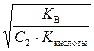 =
= 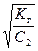 , (52)
, (52)
где K кислоты – константа диссоциации слабой кислоты.
Если гидролиз протекает ступенчато, то в выражение для расчета константы гидролиза по первой ступени входит константа диссоциации слабого электролита по последней ступени.
Концентрация ионов ОН– и рН раствора соли могут быть вычислены по формулам
[ОН–] = 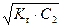 = h× С 2 , (53)
= h× С 2 , (53)
рН = 14 – рОН = 14 + lg 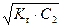 . (54)
. (54)
2) гидролиз по катиону
K г = 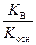 , h =
, h =  =
= 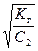 , (55)
, (55)
где K осн – константа диссоциации слабого основания.
[H+] = 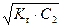 = h × С 2 , (56)
= h × С 2 , (56)
рН = –lg[H+] = –lg 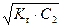 . (57)
. (57)
3 ) гидролиз по катиону и аниону одновременно:
K г =  . (58)
. (58)
Для этого случая концентрация раствора соли практически не влияет на степень гидролиза
h = 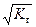 . (59)
. (59)
[H+] = 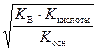 , (60)
, (60)
рН = –lg 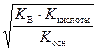 . (61)
. (61)
|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 720; Нарушение авторских прав?; Мы поможем в написании вашей работы!