
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Б. Реакции циклических форм
|
|
|
|
Рассмотренные выше свойства моносахаридов не противоречат их строению как полиоксиальдегидов и полиоксикетонов. Однако ряд свойств пентоз и гексоз приведенные формулы объяснить не могли. Так, оказалось, что пентозы и гексозы в отличие от обычных альдегидов не образуют бисульфитных производных. Кроме того, полные метиловые эфиры, приготовленные из пентоз и гексоз действием диметилсульфата и щелочи (или иодистого метила в присутствии оксида серебра), не давали характерного осадка с реактивом Фелинга, а также реакции серебряного зеркала, типичных для альдегидов.
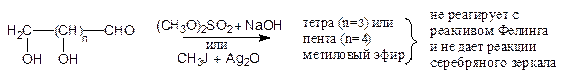
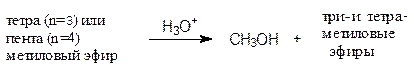 В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый:
В тоже время гидролиз этих эфиров разбавленным раствором кислоты, т.е. в условиях, в которых простые эфиры устойчивы, приводил к отщеплению одной метильной группы. Так, из тетраметилового эфира, приготовленного из пентоз, получался триметиловый эфир, а из пентаметилового, приготовленного из гексоз, – тетраметиловый:
Продукты такого «монодеметилирования» полных метиловых эфиров пентоз и гексоз уже давали реакцию серебряного зеркала.
Таким образом, было установлено, что какая-то одна из гидроксогрупп в молекулах пентоз и гексоз обладает особыми свойствами. Особые свойства этой гидроксогруппы явились следствием того, что она внутримолекулярно взаимодействует с карбонильной группой, образуя циклический полуацеталь (кольчато-цепная таутомерия). Эта гидроксогруппа также и называется, полуацетальной.
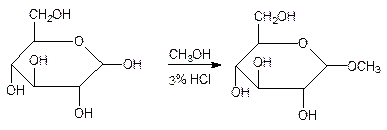 С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода:
С ее участием легко образуются метиловые эфиры. Для получения последних соответствующий моносахарид достаточно обработать метиловым спиртом в присутствии 3%-ного хлористого водорода:
Полученные таким образом производные пентоз и гексоз называют метилгликозидами; полуацетальный гидроксил, который легко замещается – гликозидным гидроксилом; атом углерода С1, у которого произошло замещение – гликозидным центром; вступающий заместитель – агликоном.
Легкость замещения гликозидного гидроксила используется для получения гликозидов самого разнообразного строения. Так, при обработке пентоз и гексоз аминами, не являющихся сильными основаниями (иначе пойдет эпимеризация), происходит образование соответствующих N-гликозидов. Например:
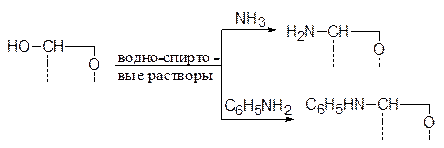 |
Фрагмент молекулы
моносахарида
Здесь агликонами являются аминная и фениламинная группы.
Остаток моносахарида сообщает связанному с ней агликону легкую растворимость в воде, делает его способным функционировать в живой (животной или растительной) клетке.
В связи с этим становится понятным чрезвычайно большая распространенность гликозидов в природе. Примерами могут служить компоненты нуклеиновых кислот – нуклеозиды; действующее начало горчичного масла – глюкоиберин, арбутин, используемые в цветной фотографии, и многие другие. В молекулы моносахаридов в качестве агликонов иногда вводят физиологически активные вещества, что облегчает их применение в медицине (усвояемость, возможность использования растворов).
Контрольные вопросы
1. Какими реакциями можно доказать наличие в молекуле глюкозы альдегидной и гидроксильных групп.
2. Что произойдет при нагревании пентаметилглюкозы и пентаацетилгалактозы при нагревании их с разбавленной серной кислотой.
3. Какие продукты образуются при окислении маннозы, при ее восстановлении, при взаимодействии с гидроксиламином, с избытком фенилгидразина.
4. Какиe два моносахарида дадут тот же озазон, что и L-галактоза.
5. Напишите схемы получения следующих гликозидов: а) метил-b-D-глюко-фуранозида; б) этил-a-D-галактопиранозида; в) изопропил-b-D-фруктопирано-зида, г) о-(оксиметил)фенил-b-D-глюкопиранозида (салицина), д) метил-b-D-рибофуранозида.
6. Нагревание пентоз с разбавленной серной кислотой приводит к образованию фурфурола. Напишите уравнение реакции.
7. Напишите проекционные формулы Фишера всех D-альдогексоз, которые при восстановлении образуют оптически неактивные многоатомные спирты.
8. Какой продукт получается при окислении азотной кислотой D-галактозы? Почему полученное соединение не обладает оптической активностью.
Тестовые задания
1. Какое из соединений является a-D-рибопиранозой?








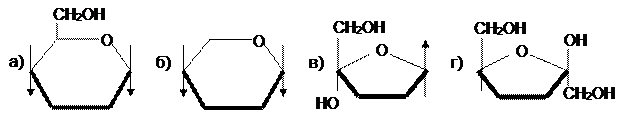
2. Образование соединения синего цвета при взаимодействии глюкозы (раствор) с гидроксидом меди (II) с образованием глюконата меди (II) обусловлено наличием в ее молекуле:
а) одной ОН-группы б) s- и p-связей
в) нескольких ОН-групп г) альдегидной группы
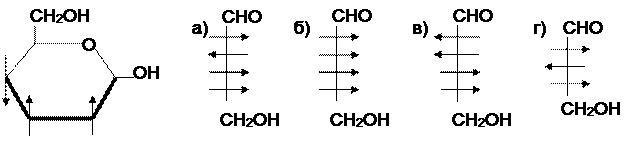
3. Какому моносахариду в открытой форме соответствует структура следующего циклического полуацеталя:
4. Углеводом, входящим в состав РНК, является:
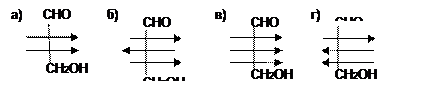
5. D-глюкоза и D-галактоза являются между собой:
а) эпимерами б) диастереомерами в) гомологами г) изомерами
6. Метилгликозид можно получить при взаимодействии:
а) глюкозы с ангидридом уксусной кислоты
б) галактозы с метиловым спиртом
в) крахмала с метилхлоридом
г) глюконовой кислоты с метанолом
7. Озазон – это продукт взаимодействия углевода с:
а) гидроксиамином б) гидразином в) вторичным амином г) HCN
8. Какая структура соответствует метил-a–D-глюкопиранозиду:
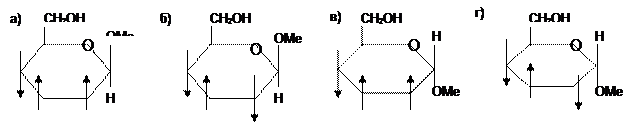
9. Какой из реагентов не вызывает ответной реакции у глюкозы?
а) NH2OH б) Cu(OH)2 в) NaHSO3 г) Ag(NH3)2OH
10. Какой из моносахаридов входит в состав нуклеиновых кислот?
а) a-D-глюкопираноза б) b-D-фруктофураноза
в) a-L-маннопираноза г) b-D-рибофураноза
11. Шестиатомный спирт сорбит образуется при взаимодействии глюкозы с?
а) уксусной кислотой б) Ag(NH3)2OH в) этанолом г) водородом
12. При растворении сахаров с течением времени происходит изменение угла вращения до определенной равновесной величины. Это явление называется:
а) поляризация б) конформационная изомерия
в) мутаротация г) ионизация
13. Как называются два оптических изомера по отношению друг к другу:
|
 а) эпимеры б) цис-транс-изомеры
а) эпимеры б) цис-транс-изомеры
в) энантиомеры г) диастереомеры
14. Реакция с каким веществом используется для доказательства того, что глюкоза – пятиатомный спирт?
а) Cu(OH)2 б) CH3COOH в) Ag2O г) NaHSO3
15. Продуктом реакции является:


а) метил-a-D-галактопиранозид
б) метил-b-D-галактопиранозид
в) метил-2,3,4,6-тетра-О-метил-a-D-галактопиранозид
г) метил-2,3,4,6-тетра-О-метил-b-D-галактопиранозид
16. Названию 2,3,6-три-О-метил-a-D-глюкопиранозе соответствует структура:
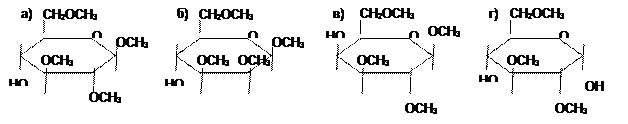
17. Альдозу от изомерной ей кетозы можно отличить по реакции с:
а) Н2 б) NaHSO3 в) Ag(NH3)2OH г) C6H5NHNH2
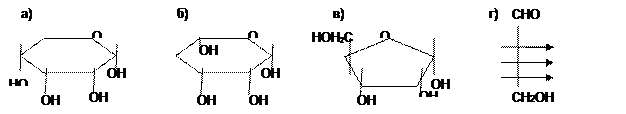
18. Какое из приведенных соединений не является компонентом таутомерного равновесия D-рибозы:
19. Фруктоза дает реакцию серебряного зеркала, так как:
а) возможна цикло-оксо-таутомерия б) возможна кето-енольная таутомерия в) содержится кето-группа г) содержится виц-диольный фрагмент
20. Фруктоза является:
а) кетогексозой б) кетопентозой в) альдогексозой г) дисахаридом
21. a– и b–глюкоза – это:
а) оптические изомеры б) структурные изомеры
в) олигосахариды г) цис-транс-изомеры
22. Какая функциональная группа присутствует в циклической форме глюкозы:
а) гидроксильная б) альдегидная в) карбоксильная г) карбонильная
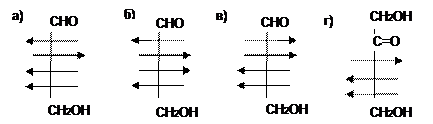
23. Какая формула отвечает L-маннозе
24. Изомерами являются:
а) 2-метилпропанол-1 и бутанол-1 б) D- и L-аланин
в) метанол и метаналь г) глюкоза и фруктоза
25. Какая характеристика не соответствует глюкозе:
а) имеет неразветвленный углеродный скелет
б) содержит кетонную группу
в) в циклической форме имеет 4 асимметрических центра
г) окисляется Cu(OH)2 при нагревании
26. Какая проекционная формула соответствует R-конфигурации глицеринового альдегида:
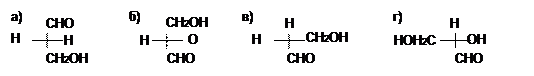
27. Конечным продуктом цепочки превращений является:
C6H5NHNH2 H2O Zn/CH3COOH


 D-глюкоза … ….
D-глюкоза … ….
(избыток) H+
а) крахмал б) фенилозазон D-глюкозы в) фруктоза г) сахароза
28. Какие схемы реакций показывают наличие в глюкозе альдегидной группы?
 а) С6Н12О6 + Cu(OH)2 (комн. t)
а) С6Н12О6 + Cu(OH)2 (комн. t)
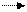 б) С6Н12О6 + HNO3
б) С6Н12О6 + HNO3
 в) С6Н12О6 + Ag(NH3)2OH
в) С6Н12О6 + Ag(NH3)2OH
 г) С6Н12О6 + Cu(OH)2 (высокая t)
г) С6Н12О6 + Cu(OH)2 (высокая t)
29. Какие моносахариды относятся к типу альдоз:
а) глюкоза б) рибоза в) дезоксирибоза г) сорбит
30. Сколько асимметрических атомов углерода в молекуле b-D-рибофуранозы:
а) один б) два в) три г) четыре
I.9. Производные моносахаридов
Кроме известных нам моносахаридов из природных объектов часто выделяют соединения, которые можно рассматривать как продукты определенных изменений в молекулах обычных альдоз и кетоз. Такие модифицированные моносахариды оказывают определенное влияние на характер функционирования в живом организме биополимеров, в состав которых они входят.
К производным моносахаридов относят соединения, имеющие моносахаридную природу и содержащие вместо гидроксильных групп (одной или несколько) атом водорода или другие функциональные группы, например аминогруппу или карбоксильную группу.
Дезоксисахара – моносахариды, в которых одна или несколько ОН-групп заменены на атом водорода. К числу важных дезоксисахаров относятся 2-дезокси-D-рибоза – структурный компонент нуклеиновых кислот (в составе ДНК); 6-дезокси-L-галактоза (фукоза) – компонент олигосахаридов животного происхождения, в частности, концевые остатки L-фукозы служат маркировкой поверхности клеток, определяющих групповую принадлежность крови человека; 6-дезокси-D-
глюкоза (хиновоза). Дезоксисахара обладают свойствами обычных моносаха-ридов.

Аминосахара – производные моносахаридов, содержащие аминогруппу вместо ОН-группы (чаще всего при С2). Аминогруппа может быть содержать остатки уксусной, иногда серной кислот. Аминосахара обладают оснόвными свойствами и образуют с кислотами хорошо кристаллизующиеся соли, легко ацилируются, алкилируются, образуют основания Шиффа. Аминосахара являются компонентами биополимеров (хитин, мурамин, гепарин и др.), Важнейшими представителями аминосахаров служат 2-аминоаналоги D-глюкозы и D-галактозы.
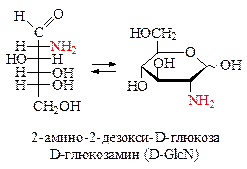 | 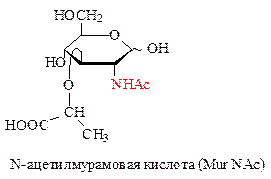 | ||||||
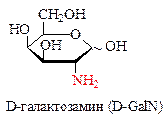 | |||||||
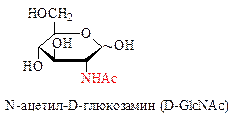 |
2-Ацетамидо-2-дезоксиглюкоза, часто неправильно называемая N-ацетил-глюкзамином, входит в состав ряда важных полисахаридов, в частности, является главным компонентом хитина (панцири ракообразных и насекомых; стенки бактериальной клетки; стенки клеток грибов и дрожжей), а также полисахаридов соединительной ткани животных и человека.
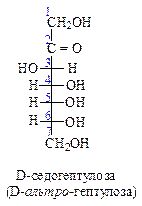
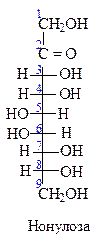 Высшие сахара – моносахариды с 7-9 атомами углерода. К высшим сахарам относится D-седогептулоза – кетоза с семью атомами углерода. Конфигурация хиральных центров этого соединения совпадает с альтрозой, отсюда второе название D- альтро -гептулоза. Соединение является промежуточным продуктом в фотосинтезе растений, углеводного обмена животных и микроорганизмов.
Высшие сахара – моносахариды с 7-9 атомами углерода. К высшим сахарам относится D-седогептулоза – кетоза с семью атомами углерода. Конфигурация хиральных центров этого соединения совпадает с альтрозой, отсюда второе название D- альтро -гептулоза. Соединение является промежуточным продуктом в фотосинтезе растений, углеводного обмена животных и микроорганизмов.
Важнейшими представителями высших сахаров являются нейраминовая кислота и ее N- и O-ацилированные производные – сиаловые кислоты. Базисный моносахарид нейраминовой кислоты содержит 9 атомов углерода и относится к кетозам, т. е. это нонулоза. В нейраминовой кислоте имеется карбоксильная группа вместо СН2ОН (при С1), атом водорода вместо ОН-группы (при С3) и аминогруппа вместо ОН-группы (при С5).
N-Ацетилнейраминовая кислота получается при альдольной конденсации пировиноградной кислоты и N-ацетил-D-маннозамина при участии специфичес-ких ферментов. Нейраминовая кислота в свободном виде встречается в спинномозговой жидкости и играет исключительно важную роль в животных организмах (специфическая маркировка поверхностей клеток и молекул биополимеров). Сиаловые кислоты входят в состав крови, ганглиозидов мозга, участвующих в проведении нервных импульсов. Сиаловые кислоты во многом определяют свойства клеточной поверхности, ответственны за злокачественное перерождение клеток.
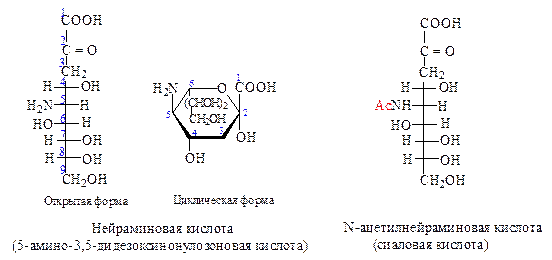
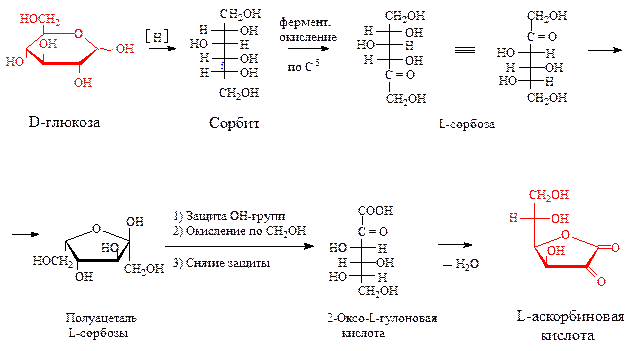 Аскорбиновая кислота (витамин С) – один из водорастворимых Витами-нов. Своим названием обязана противоцинговой активности («а» – нет, «скорбут» – цинга). Аскорбиновая кислота по структуре близка к моносахаридам L-ряда. Отметим, что D-форма этого соединения является антивитамином. Аскорбиновая кислота содержится во фруктах (лимоны, апельсины), ягодах (шиповник, черная смородина), овощах и молоке. Синтезируется в организмах многих животных, кроме морских свинок, обезьян и человека. Суточная норма для взрослого человека 0,15г (по рекомендациям врачей), 7-10г по мнению Л. Полинга. В промышленности производится в большом масштабе из глюкозы или из продукта восстановления глюкозы – сорбита (рис.1).
Аскорбиновая кислота (витамин С) – один из водорастворимых Витами-нов. Своим названием обязана противоцинговой активности («а» – нет, «скорбут» – цинга). Аскорбиновая кислота по структуре близка к моносахаридам L-ряда. Отметим, что D-форма этого соединения является антивитамином. Аскорбиновая кислота содержится во фруктах (лимоны, апельсины), ягодах (шиповник, черная смородина), овощах и молоке. Синтезируется в организмах многих животных, кроме морских свинок, обезьян и человека. Суточная норма для взрослого человека 0,15г (по рекомендациям врачей), 7-10г по мнению Л. Полинга. В промышленности производится в большом масштабе из глюкозы или из продукта восстановления глюкозы – сорбита (рис.1).
Рис.1. Схема синтеза аскорбиновой кислоты
Аскорбиновая кислота является g-лактоном 2-оксо-L-гулоновой кислоты. Существует в виде двух таутомерных форм (оксо-енольная таутомерия).
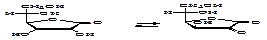 |
 Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).
Из химических свойств аскорбиновой кислоты рассмотрим два – наиболее важных. Аскорбиновая кислота проявляет довольно сильные кислотные свойства, обусловленные диссоциацией одной из ОН-групп ендиольного фрагмента. Показатель кислотности рКа 4,2 (сравните, для уксусной кислоты рКа 4,76).
Аскорбиновая кислота обладает сильными восстановительными свойствами. Образующаяся при ее окислении дегидроаскорбиновая кислота легко восстанавливается обратно в аскорбиновую кислоту. Этот процесс обеспечивает некоторые окислительно-восстановительные реакции в организме, например гидроксилирование пролина и лизина – аминокислот, необходимых для синтеза прочного коллагена. При цинге – болезни, вызванной недостатком витамина С, синтез коллагена нарушен, образуются менее прочные коллагеновые волокна. С этим связана ломкость кровеносных сосудов и возникновение множественных точечных кровоизлияний.

|
|
|
|
|
Дата добавления: 2015-07-13; Просмотров: 5360; Нарушение авторских прав?; Мы поможем в написании вашей работы!