
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Области pv- диаграммы
|
|
|
|
РЕАЛЬНЫЕ ГАЗЫ
ЛЕКЦИЯ 7
Сопло Лаваля
Проведенный анализ касался течения газа через суживающееся сопло. Из него не следует делать вывод о том, что вообще не возможно, например, при адиабатном течении получить скорость потока выше звуковой.
Как следует из уравнения (10.1), для перехода в область сверхзвуковых скоростей необходимо иметь расширяющийся канал. Следовательно, дополняя суживающийса канал, где газ достигает критической скорости, расширяющимся, мы предоставляем газу возможность продолжить свое расширение и приобрести сверхзвуковую скорость. Такое комбинированное сопло называется соплом Лаваля (рис. 4).
Сопло Лаваля целесообразно применять лишь при 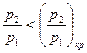 . Скорость истечения, например, при адиабатном течении определится с помощью уравнения (14). Расход определится по минимальному сечению, где имеет место кризис течения. Для этого используется уравнение для определения
. Скорость истечения, например, при адиабатном течении определится с помощью уравнения (14). Расход определится по минимальному сечению, где имеет место кризис течения. Для этого используется уравнение для определения  , в которое следует подставлять вместо f минимальное сечение сопла fmin.
, в которое следует подставлять вместо f минимальное сечение сопла fmin.
В ряде случаев приходится иметь дело с системами, состояние которых не позволяет использовать модель идеального газа. В качестве примера можно назвать водяной пар в тех состояниях, при которых он используется в паросиловых установках.
Здесь приходится принимать во внимание, что молекулы имеют определенные размеры и между ними существуют силы взаимодействия: притяжение при сравнительно больших расстояниях между молекулами и отталкивание при сближении молекул на малые расстояния.
Модель реального газа представляется в виде твердых шариков диаметром d0, взаимно притягивающихся друг к другу.
Как видно, модель реального газа отличается от модели идеального газа, во-первых, тем, что сами молекулы имеют некоторый объем, во-вторых, наличием сил межмолекулярного сцепления.
В общем случае, это приводит к тому, что в отличие от идеального газа
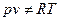
и при T = const
 .
.
Устройство pv – диаграммы реального газа
Впервые подробное экспериментальное исследование зависимости p от v в разных изотермических процессах сжатия реального газа провел на углекислоте в 1857 – 1969 г.г. английский физик Эндрюс. Результаты его экспериментов показаны на рис. 1.
Как видно, при температурах, меньших 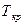 , изотермическое сжатие углекислоты (СО2) вначале сопровождается ростом давления. В точке а начинается процесс конденсации. Состояние, отвечающее этой точке, называют сухим насыщенным паром. При продолжении изотермического сжатия давление остается постоянным, а уменьшение объема сопровождается тем, что все большее количество пара превращается в жидкость.
, изотермическое сжатие углекислоты (СО2) вначале сопровождается ростом давления. В точке а начинается процесс конденсации. Состояние, отвечающее этой точке, называют сухим насыщенным паром. При продолжении изотермического сжатия давление остается постоянным, а уменьшение объема сопровождается тем, что все большее количество пара превращается в жидкость.
Наконец, в точке b конденсация завершается, и рабочее тело представляет собой кипящую жидкость. На участке ab одновременно существует и жидкая и газообразная фазы. Состояния, характеризуемые точками на ab, называют влажным насыщенным паром.
Соотношение между паровой и жидкой фазой характеризуют степенью сухости пара - это массовая доля сухого насыщенного пара во влажном. Степень сухости пара определяется выражением
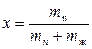 ,
,
где mn и mж – соответственно масса пара и жидкости во влажном насыщенном паре.
Удельный объем сухого насыщенного пара обозначают 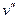 (точка а), а кипящей жидкости –
(точка а), а кипящей жидкости – 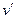 (точка b).
(точка b).

Рис. 1. PV – диаграмма реального газа
При продолжении изотермического сжатия в области v < v' отмечается резкое возрастание давления, так как жидкость обладает малой сжимаемостью.
С ростом температуры разность (v" - v'), быстро убывает за счет интенсивного уменьшения v" и некоторого роста v', т.е. с ростом температуры уменьшается разница между плотностями жидкой и газовой фаз.
Уменьшение (v" - v') продолжается вплоть до температуры Ткр, когда эта разность обращается в нуль (точка К), т.е. в этой точке исчезает различие между плотностями жидкости и пара. Точка К, отвечающая этому состоянию, называется критической точкой. Соответственно давление, температура и удельный объем называются критическими (ркр, Ткр, vкр). Естественно, что все попытки обеспечить путем изотермического сжатия сжижение газа при Т > Ткр, обречены на неудачу.
Критической температуре можно дать молекулярно-кинетическое толкование. Объединение свободнодвижущихся молекул в каплю, жидкости при сжижении газа происходит исключительно под действием сил взаимного притяжения. Этому препятствует кинетическая энергия движения молекул, равная с среднем kT (k – постоянная Больцмана). Очевидно, объединение молекул в каплю может произойти лишь при том условии, что кинетическая энергия движения молекул, пропорциональная Т, меньше или равна потенциальной энергии из взаимного притяжения (uo). Если кинетическая энергия больше потенциальной энергии взаимного притяжения, то конденсация жидкости при изотермическом сжатии не сможет произойти. Сопоставление этих положений с результатом анализа диаграммы Эндрюса позволяет сделать вывод о том, что Ткр – температура, соответствующая равенству указанных энергий
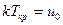 .
.
Если 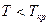 , то
, то 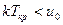 и конденсация при изотермическом сжатии возможна.
и конденсация при изотермическом сжатии возможна.
Если 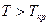 , то
, то 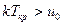 и конденсация при изотермическом сжатии не возможна.
и конденсация при изотермическом сжатии не возможна.
1. Область левее нижней пограничной кривой KI – это область некипящей жидкости.
2. Линия KI - это геометрическое место точек начала парообразования или конца конденсации. Иначе эту линию называют нижняя пограничная кривая. Степень сухости на нижней пограничной кривой равняется нулю (x = 0), а состояние вещества кипящая жидкость.
3. Область между KI и KII - область влажного насыщенного пара.
Это смесь сухого насыщенного пара с каплями жидкости (туманообразное состояние). Это двухфазное состояние.
Для того чтобы превратить 1 кг жидкости в пар, надо сообщить ей какое-то количество теплоты. Эту величину называют удельной теплотой парообразования r, кДж/кг.
4. Линия KII - это геометрическое место точек конца парообразования или начала конденсации. Линию KII иначе называют верхняя пограничная кривая. Степень сухости на верхней пограничной кривой равняется единице (x = 1), а состояние вещества сухой насыщенный пар.
Насыщенный пар - это пар, находящийся в динамическом равновесии с жидкостью.
5. Точка К - критическая точка.
6. Область правее и выше верхней пограничной кривой – это область перегретого пара.
|
|
|
|
|
Дата добавления: 2017-01-14; Просмотров: 907; Нарушение авторских прав?; Мы поможем в написании вашей работы!