
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тема № 5. Гетероциклические соединения
|
|
|
|
Ферменты
Лабораторная работа № 7
Ферменты – это биологические катализаторы белковой природы, образуемые живой клеткой. Ускоряя многочисленные реакции, протекающие в живом организме, ферменты являются движущей силой обмена веществ.
Все ферменты в зависимости от типа катализируемой реакции подразделяются на 6 классов:
1 Оксидоредуктазы – катализируют окислительно - восстановительные реакции.
2 Трансферазы – катализируют реакции переноса различных химических групп с одной молекулы на другую.
3 Гидролазы – катализируют реакции гидролиза.
4 Лиазы – катализируют реакции отщепления от субстратов негидролитическим путем той или иной химической группы с образованием двойной связи или присоединение химической группы по месту двойной связи.
5 Изомеразы – катализируют реакции изомеризации органических соединений.
6 Лигазы, или синтетазы – катализируют реакции синтеза веществ, сопровождающиеся расщеплением высокоэнергетической связи в молекуле АТФ или аналогичного нуклеозидтрифосфата.
Цель работы: в ыяснить химическую природу, отдельные свойства ферментов. Изучить основные факторы определяющие ферментативную активность.
Реактивы и оборудование:
1) 1 % раствор крахмала;
2) 1% раствор сахарозы,
3) слюна;
4) 1% раствор KI (или 1 % раствор Люголя);
5) 1% раствор CuSO4;
6) 10% раствор NaOH
7) картофель сырой и вареный;
8) раствор пероксида водорода
9) штатив с пробирками;
10) водяная баня;
11) Термометр;
12) Электроплитка.
Опыт 7.1. Ферментативный гидролиз крахмала
В пробирку собрать 2 – 3 мл. слюны, разбавить ее водой в 5 – 6 раз.
Взять 3 пробирки, пронумеровать и налить в каждую примерно 1 мл. раствора слюны.
Раствор слюны в первой пробирке прокипятить, во вторую пробирку добавить 1 мл. раствора CuSO4 и раствора NaOH. В первые две пробирки прилить по 5 мл. раствора крахмала, а в третью раствора сахарозы. Поставить все три пробирки в водяную баню (39 – 41оС) на 15 минут затем достать, охладить до комнатной температуры, добавить в первые две пробирки по одной капле раствора Люголя. В тех пробирках, где нет синего (сине – фиолетового) окрашивания и с раствором третьей пробирки проделать реакцию Троммера..
В две пробирки налить 5 капель раствора крахмала и добавить 3 капли воды: в первую- добавить раствор KI, во вторую – 2 капли раствора CuSO4 и 2 - 3 капли раствора NaOH.
Полученные результаты занести в таблицу.
| № п/ п | Субстрат | Ферменты | Дополните-льный фактор | Результаты опыта | Выводы | |
| Реак-ция с йодом | Реак-ция Троммера | |||||
| крахмал крахмал сахароза крахмал крахмал | амилаза амилаза амилаза вода вода | кипячение |
Опыт 7.2 Открытие каталазы
Каталаза – фермент, который разлагает пероксид водорода. Относится к классу оксидоредуктаз. Каталаза является сложным ферментом, состоящим из белкового комплекса и группы, содержащей железо.
Каталаза расщепляет перекись водорода на молекулярный кислород и воду 2H2O2 → O2 + 2H2O
В пробирку поместить 10 капель Н2О2 и кусочек сырого картофеля. В другую пробирку - 10 капель Н2О2 и кусочек вареного картофеля.
Отметить происходящие изменения.
Контрольные вопросы
1. Классификация белков. Простые и сложные белки.
2. Строение белковой молекулы: первичная, вторичная, третичная и четвертичная структура белка.
3. Что такое денатурация белков?
4. Какие вы знаете денатурирующие факторы и в чем особенности их действия?
5. Какие структуры белковых молекул изменяются при денатурации?
6. Является ли денатурация обратимым процессом?
7. Какие методы определения аминокислотной последовательности вы знаете?
8. В чем заключается стабилизация вторичной и третичной структур.
9. Что значит окислительное дезаминирование?
10. Какие белки называются глобулярными? Приведите примеры глобулярных бедков.
11. Какие белки называются фибриллярными? Приведите примеры фибриллярных белков.
Упражнения по теме «Белки».
1. Укажите методы, которые применяют для определения последовательности аминокислотных остатков в пептиде. Проиллюстрируйте их на примере глицилаланилфенилаланина.
2. Напишите формулы: а) изомерных дипептидов, составленных из глицина и аланина; б) изомерных трипептидов, составленных из глицина, аланина и серина. Назовите их.
3. Приведите примеры, позволяющие определять N-и C-концевые аминокислоты в полипептиде. Проиллюстрируйте их на примере трипептида – фенилаланилвалилглицина.
4. Напишите структурную формулу трипептида, при полном гидролизе которого образуется глицин, аланин и цистеин, а при частичном гидролизе- аланилглицин и глицилцистеин.
5. Используя метод защиты аминогруппы карбобензоксихлоридом (С6Н5СН2ОСОСI), осуществите синтез трипептидов; а) глицилаланилглицина; б) аланилглицилфенилаланина.
6. Укажите наиболее характерные свойства молекул белка.
7. Какие белки называются гормонами?
8. Что такое ферменты?
9. Как осуществляется синтез белков в живых клетках?
Циклические соединения, у которых циклы образованы не только углеродными атомами, но и атомами других элементов – гетероатомами (О, S, N), - называются гетероциклическими. Гетероциклические соединения делят по размерам цикла и числу гетероатомов в цикле.
Среди этих соединений наибольшее значение имеют пяти- и шестичленные гетероциклические соединения. Типичные гетероциклические соединения обладают ароматическим характером. Однако, наличие гетероатома сказывается на распределении электронной плотности. Например, в пятичленных гетероциклах (в фуране, тиофене, пирроле) электронная плотность смещена от гетероатома в сторону кольца и максимальна в a-положениях. Поэтому в a-положениях наиболее легко идет реакция электрофильного замещения (SЕ).
В шестичленных циклах (например, пиридине) гетероатом, связанный с углеродом двойной связью, оттягивает на себя p-электронную плотность цикла, поэтому электронная плотность в молекуле пиридина понижена в a и g-положениях. Это согласуется с предпочтительной ориентацией в эти положения реагентов при нуклеофильном замещении (SN). Так как в пиридине электронная плотность больше в b - положении, то электрофильный реагент ориентируется в b - положение.
При изучении гетероциклов с двумя гетероатомами особо обратить внимание на пиримидин и его производные: урацил, тимин, цитозин. Пиримидиновое ядро встречается в многочисленных природных продуктах: витаминах, коферментах и нуклеиновых кислотах:
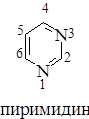
Электрофильное замещение для пиримидина проходит в положении 5; нуклеофильное (как и для пиридина) затруднено и атаке подвергается атом углерода в положениях 4 и 6.
Сложная гетероциклическая система, состоящая из двух конденсированных гетероциклов – пиримидина и имидазола называется ядром пурина.
Пуриновая группировка лежит в основе многих соединений, прежде всего нуклеиновых кислот, в которые она входит в виде пуриновых оснований: аденина (6-аминопурин) и гуанина(2-амино-6-оксипурин).
Интерес представляет кислородное производное пурина - мочевая кислота (2,6,8 – триоксипурин).
|
|
|
|
|
Дата добавления: 2017-02-01; Просмотров: 111; Нарушение авторских прав?; Мы поможем в написании вашей работы!