
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Co, Ni, Sn, Pb, H , Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au
|
|
|
|
Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd,
При сравнении металлов в ряду напряжений за меру химической активности принимается сумма трех слагаемых: энергии атомизации, характеризующей прочность кристаллической решетки данного металла; энергии ионизации атомов - отрыва от них валентных электронов и энергии гидратации, зависящей от электронной структуры иона, его заряда и радиуса. Чем меньше радиус иона и больше заряд, тем больше энергия гидратации, так как поле возникающее вблизи маленьких ионов с большим зарядом будет больше.
Ряд напряжений характеризует химические свойства металлов:
1) чем левее расположен металл в ряду напряжений, тем сильнее его восстановительная способность и тем слабее окислительная способность его иона в растворе (т.е. тем легче он отдает электроны (окисляется) и тем труднее его ионы присоединяют обратно электроны);
2) каждый металл способен вытеснять из растворов солей те металлы, которые стоят в ряду напряжений правее его, т.е. восстанавливает ионы последующих металлов в электронейтральные атомы, отдавая электроны и сам превращаясь в ионы;
3) только металлы, стоящие в ряду напряжений левее водорода (Н), способны вытеснять его из растворов кислот (например, Zn, Fe, Pb, но не Сu, Hg, Ag).
В справочных таблицах приводят стандартные электродные потенциалы ряда металлов, показывающие возможность переноса электронов между ними. Эти данные получены для систем, содержащих водный раствор ионов металла с концентрацией (активностью) 1 М и электрод из этого металла; электрический потенциал Е определяется относительно стандарта – водородного электрода.
Записывать потенциалы можно по разному, поскольку в полуреакции заключено равновесие. Но наиболее удобно и сейчас повсеместно принято писать Ox + ne ® Red. При составлении таблицы потенциалов положительные потенциалы записываем ниже нуля (там, где DG<0), а отрицательные - по возрастанию абсолютной величины вверх.
В этой таблице сильные окислители находятся в левом нижнем углу, сильные восстановители - в правом верхнем.
Потенциал системы из двух металлов вычисляется по таблицам.
Для системы:
Zn + Cu2+ = Zn2+ + Cu
Е0 = Е0 (ок-ль) – Е0 (восст-ль) = +0,34 - (-0,76) = 1,1 В.
Направление окислительно-восстановительной реакции обусловливает тот окислитель, у которого значение электродного потенциала больше.
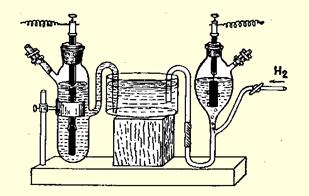
Рисунок 14.3 - Измерение потенциала металлического электрода (слева) по водородному
Помимо окислительно-восстановительных реакций, в которых атомы металла-восстановителя взаимодействуют с ионами металла-окислителя, известно множество окислительно-восстановительных реакции, где в роли окислителя выступают ионы металла, а в роли восстановителя – ионы неметалла:
2Fе3+ + 2I- = 2Fе2 + I2,
а также реакции, где одни анионы-окислители – окисляют, другие анионы–восстановители, например:
MnO4 - + 5 Cl =8H+ = Mn2+ +2 ½ + Cl2 + 4H2O.
Подобные окислительно-восстановительные реакции можно провести таким образом, чтобы одни ионы отдавали свои электроны другим не непосредственно, а через проводник (инертный платиновый электрод). Растворы в таких сосудах соединяют трубкой, заполненной раствором КСl, а электроды – проводником. Во внешней цепи появляется электрический ток.
В каждом из полуэлементов на границе между инертным электродом и раствором возникает разность потенциалов, называемая окислительно-восстановительным потенциалом. Последний, будучи измерен по отношению к водородному электроду, называется стандартным электродным окислительно-восстановительным потенциалом
В Приложении Б приведены значения стандартных электродных потенциалов некоторых окислительнл-восстановительных систем в водных растворах при температуре 25 0С.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 602; Нарушение авторских прав?; Мы поможем в написании вашей работы!