
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химическая коррозия
|
|
|
|
15.2.1 Термодинамика химической коррозии
Химическая коррозия представляет собой самопроизвольное разрушение металлов в среде окислительного газа (например, кислорода, галогенов) при повышенных температурах или в жидких неэлектролитах. Сущность процессов химической коррозии сводится к окислительно-восстановительной реакции, осуществляемой непосредственным переходом электронов металла на окислитель.
Рассмотрим химическую коррозию в газах (газовую коррозию), в частности, коррозию в атмосфере кислорода. Уравнение реакции окисления металлов кислородом можно записать в общем виде:
nM + m/2О2 = МnOm.
В соответствии с законами химической. термодинамики эта реакция, как и другие реакции коррозии, может протекать лишь при условии уменьшения энергии Гиббса системы, т.е. при условии, если энергия Гиббса меньше нуля: AG < 0. Так как, по определению, энергия Гиббса образования простых веществ равна нулю, то энергия Гиббса окисления металлов равна энергия Гиббса образования оксидов. Энергию Гиббса реакции окисления рассчитывают по уравнению
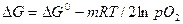 , (15.1)
, (15.1)
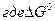 — стандартная энергия Гиббса реакции;
— стандартная энергия Гиббса реакции;
р0 — относительное парциальное давление кислорода (р /100).
Стандартные значения ∆G° приведены в справочниках. Для подавляющего большинства металлов стандартная энергия Гиббса их окисления ниже нуля, что говорит о возможности протекания этой реакции при атмосферном давлении кислорода.
Для большинства металлов условие ∆G > 0, при котором коррозия невозможна, проявляется при очень низких давлениях кислорода, не реализуемых на практике. Однако энергия Гиббса реакции меняется при изменении температуры, соответственно меняется и давление кислорода, при котором ∆G > 0.
15.2.2 Кинетика химической коррозии
Скорость химической коррозии зависит от многих факторов и в первую очередь от характера продуктов коррозии. В процессе окисления на поверхности металла образуется твердая пленка оксидов. Для продолжения коррозии необходимо, чтобы ионы металла или кислород (или оба одновременно) диффундировали через эту плёнку. Обычно с поверхности раздела металл — оксид в направлении от металла к внешней поверхности пленки происходит диффузия ионов металла, а не атомов, так как ионы металлов по размерам меньше атомов. Одновременно в этом же направлении должны перемещаться электроны. Ионы О2- имеют больший радиус, чем атомы, поэтому с поверхности раздела оксид — газ в глубину пленки двигаются не ионы, а атомы кислорода, которые в пленке ионизируются (О + 2е = О2-) и, встречаясь с ионами металла, образуют оксиды.
Скорость окисления определяется сплошностью и защитными свойствами поверхностной пленки и зависит от наличия в ней трещин. Поскольку пленки продуктов коррозии обычно хрупки и малопластичны, образование трещин в известной степени зависит от того, претерпевает ли пленка в процессе роста растяжения, благоприятствующие ее разрушению, или же она образуется в условиях сжатия. Это, в свою очередь, зависит от соотношения между объемами продуктов коррозии и металла, из которого они образовались:
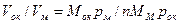 , (15.2)
, (15.2)
где VOK — объем оксида;
Мок — молярная масса оксида;
рм — плотность металла;
п — число атомов металла в молекуле оксида:
Мм — молярная масса металла;
рок — плотность оксида.
Если VOK / Vм < 1, то образующаяся пленка не может быть сплошной и защищать металл от коррозии. Скорость роста пленки во времени у таких металлов остается постоянной (рисунок 15.2). Толщина пленки пропорциональна времени окисления:
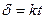 , (15.3)
, (15.3)
где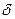 — толщина пленки;
— толщина пленки;
k — постоянная;
t — время окисления.
Для щелочных и щелочно-земельных металлов действительно наблюдается указанный линейный закон роста пленок во времени. При повышении температуры реакция окисления таких металлов начинает резко ускоряться вследствие плохого отвода теплоты. Рыхлая пленка оксида металла является препятствием для отвода теплоты, выделяющейся в ходе реакции. В результате происходит разогрев металла, скорость окисления его резко возрастает. Линейное увеличение толщины пленки во времени наблюдается также при высоких температурах для ванадия, вольфрама) и молибдена, образующих летучие оксиды.
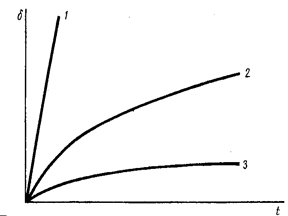 |
15.2 – Рост толщины слоя пленки во времени по линейному (1), параболическому (2)
и логарифмическому (3) законам
Для металлов, у которых в результате химической коррозии получаются сплошные пленки (VOK/VM > 1), процесс коррозии будет тормозиться диффузией реагентов через пленку, и по мере утолщения пленки дальнейший рост ее будет все время замедляться. Для таких металлов (Fe, Co, Ni, Mn, Ti) в общем наиболее характерна параболическая зависимость для кинетики окисления (см. рисунок 15.2), которая в простейшем случае (исключая начальный период роста пленки) определяется выражением
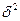 = kDСо t, (15.4)
= kDСо t, (15.4)
где k — константа;
D — коэффициент диффузии иона;
Со — концентрация кислорода в газе.
Для ряда металлов (Zn, Al, Cr) установлена логарифмическая зависимость роста пленки во времени (рисунок 15.2):
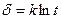 . (15.5)
. (15.5)
Пленки у таких металлов обладают высокими защитными свойствами. Различают тонкие, средние и толстые пленки. Толщина тонких пленок составляет от толщины монослоя молекул до 40 нм. Такие пленки на поверхности металла невидимы; их наличие может быть установлено с помощью специальных методов. Пленки средней толщины порядка 40-50 нм уже вполне соизмеримы с длиной волны видимых световых лучей. Эти пленки становятся видимыми вследствие их окраски. Толстые пленки могут достигать значительных толщин (например, окалина на стали, толстослойные анодные пленки на алюминиевых сплавах).
При рассмотрении коррозии необходимо учитывать наличие на поверхности металла видимых и невидимых пленок, так как коррозионное поведение металла тесно связано с возникновением, устойчивостью и разрушением защитных пленок. Наиболее высокими защитными свойствами обладает сплошная, достаточно тонкая прочная и эластичная пленка, имеющая хорошее сцепление с металлом и одинаковый с ним коэффициент линейного расширения, и возникающая на его гладкой поверхности. При этом пленка должна иметь некоторую оптимальную толщину, чтобы в достаточной степени тормозить встречную диффузию молекул агрессивного агента и ионов металла.
На большинстве металлов защитная пленка после достижения известной толщины растрескивается, что позволяет химической коррозии развиваться дальше. Разрушение пленки возможно по ряду причин. Если объем пленки больше объема металла, на месте которого она образовалась, то это приводит к появлению внутренних напряжений сжимающих пленку параллельно поверхности и стремящихся оторвать ее от металла. При высоких внутренних напряжениях пленка разрушается. Таким образом, важны не только защитные свойства пленки, но и ее механические свойства — прочность, упругость.
Скорость коррозии возрастает с увеличением температуры из-за повышения коэффициента диффузии и изменения защитных свойств пленки. Быстрое разрушение защитной пленки часто вызывает резкие температурные изменения. Это связано прежде всего с различными коэффициентами линейного расширения металла и пленки.
До сих пор рассматривалось образование, устойчивость и разрушение защитных оксидных пленок, возникающих на металле при химическом взаимодействии его с кислородом. Но помимо кислорода ряд других газов может обладать сильными агрессивными свойствами по отношению к металлам при повышенных температурах. Наиболее активными газами являются фтор, диоксид серы, хлор, сероводород. Их агрессивность по отношению к различным металлам, а следовательно, и скорость коррозии последних не одинаковы. Так, например, алюминий и его сплавы, хром и стали с высоким содержанием хрома устойчивы в атмосфере, содержащей в качестве основного агрессивного агента кислород, но становятся совершенно неустойчивыми, если в атмосфере присутствует хлор. Никель неустойчив в атмосфере диоксида серы, а медь вполне устойчива. Коррозия низколегированных и углеродистых сталей в выхлопных газах двигателей внутреннего сгорания, в топочных и печных газах сильно зависит от соотношения СО и О2. Повышение содержания О2 увеличивает скорость газовой коррозии и, наоборот, повышение содержания СО ослабляет коррозию. Ряд металлов (Со, Ni, Cu, Pb, Cd, Ti) устойчивы в атмосфере чистого водяного пара при температуре выше температуры кипения воды.
Различная скорость коррозии металлов в разных средах обусловлена прежде всего свойствами образующихся на поверхности металлов пленок. При изменении состава внешней среды изменяется состав защитной пленки и ее физико-химические свойства. Кроме того, атомы различных реагентов с разной скоростью диффундируют через защитную пленку.
Таким образом, скорость химической коррозии определяется прежде всего свойствами возникающей при коррозии пленки на поверхности металла, характер которой определяется природой металла и окислителя, а также температурой.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 655; Нарушение авторских прав?; Мы поможем в написании вашей работы!