
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Тонкая структура энергетических уровней атома водорода
|
|
|
|
Два физических фактора порождают тонкую структуру энергетических уровней атома водорода:
1) релятивистский эффект зависимости массы атомного электрона от скорости его движения вокруг ядра, 2) взаимодействие собственного магнитного момента электрона с магнитном полем, создаваемым электроном в его движении около ядра.
Причем последний фактор, связанный со спином электрона и его орбитальным движением так же обладает релятивистской природой.
При расчете энергетического спектра атома с помощью уравнения Шредингера эти факторы учесть нельзя, поскольку оно не удовлетворяет требованиям теории относительности. Поэтому при помощи уравнения Шредингера нельзя описать тонкую структуру энергетического спектра атома. Энергетический спектр атома и его тонкую структуру можно рассчитать при помощи уравнения Дирака - квантомеханического уравнения, учитывающего требования специальной теории относительности. Можно поступить иначе, воспользоваться менее строгим, но физически более наглядным способом – рассмотрением энергетических поправок к основным состояниям атома водорода, обусловленных каждым из указанных выше факторов. В наших условиях предпочтительней второй путь.
Влияние релятивистского эффекта на энергетические состояния атома было впервые рассмотрено Зоммерфельдом (1916). Окончательное выражение для релятивистской энергетической поправки к энергетическому уровню Е имеет вид:
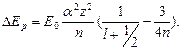 (5.3)
(5.3)
Здесь  – постоянная тонкой структуры,
– постоянная тонкой структуры, 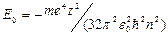 энергия атома водорода без учета релятивистских эффектов.
энергия атома водорода без учета релятивистских эффектов.
Из (5.3) видно, что постоянная тонкой структуры определяет масштаб релятивистской энергетической поправки. Величина поправки DЕр мала, порядка a2 Ео ~ 10-3 эВ.
Рассмотрим теперь влияние спина электрона на его энергию в атоме с одним валентным электроном. Благодаря собственному магнитному моменту электрон ведет себя как «магнитный диполь», помещенный в магнитное поле, создаваемое движением этого же электрона по орбите. В атомной физике взаимодействие магнитного спинового момента с орбитальным магнитным полем носит название спин – орбитального взаимодействия (l s-взаимодействие). Благодаря этому магнитному взаимодействию электрон обладает дополнительный энергией 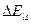 .Теперь учтем энергию спин – орбитального взаимодействия. Допустим, что индукция магнитного поля возникающего при движении электрона в поле ядра
.Теперь учтем энергию спин – орбитального взаимодействия. Допустим, что индукция магнитного поля возникающего при движении электрона в поле ядра , а спиновый магнитный момент электрона
, а спиновый магнитный момент электрона . Тогда энергия спин – орбитального взаимодействия
. Тогда энергия спин – орбитального взаимодействия 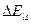 будет равна
будет равна
 (5.4)
(5.4)
Собственный (спиновый) магнитный момент электрона определяется выражением

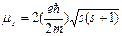 ,
,
где 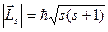 ;
; 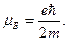
 - собственный момент импульса электрона, mБ – магнетон Бора, s – спиновое квантовое число (s=1/2). Для описания спин – орбитального взаимодействия, а также для целей систематики спектров атомов применяется векторная модель атома. В этой модели момент импульса, соответствующий орбитальному движению электрона, представляется вектором
- собственный момент импульса электрона, mБ – магнетон Бора, s – спиновое квантовое число (s=1/2). Для описания спин – орбитального взаимодействия, а также для целей систематики спектров атомов применяется векторная модель атома. В этой модели момент импульса, соответствующий орбитальному движению электрона, представляется вектором  ,а его спин – вектором
,а его спин – вектором  . Благодаря спин – орбитальному взаимодействию орбитальный момент
. Благодаря спин – орбитальному взаимодействию орбитальный момент  электрона складывается с его спином
электрона складывается с его спином  . Результирующий вектор
. Результирующий вектор
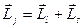
называется вектором полного момента импульса электрона.
Окончательное выражение для энергии 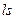 - взаимодействия
- взаимодействия 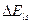 имеет вид // 5.6.1-3/
имеет вид // 5.6.1-3/
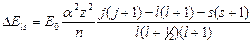 (5.5)
(5.5)
Из (5.5) следует, что величина энергетической поправки на 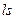 - взаимодействие зависит от взаимной ориентации векторов
- взаимодействие зависит от взаимной ориентации векторов  и
и  т.е. от
т.е. от  . Кроме того, поскольку в одноэлектронном атоме при данном l квантовое число j принимает два значения
. Кроме того, поскольку в одноэлектронном атоме при данном l квантовое число j принимает два значения 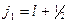 и
и 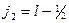 из (5.5) следует, что
из (5.5) следует, что 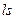 - взаимодействие приводит к расщеплению
- взаимодействие приводит к расщеплению 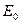 уровня, в то время как поправка
уровня, в то время как поправка 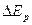 приводит только к смещению. Из последнего соотношения видно, что
приводит только к смещению. Из последнего соотношения видно, что 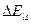 ~
~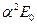 . Таким образом, оба эффекта – собственно - релятивистский и связанный со спин – орбитальным взаимодействием имеют один порядок величины:
. Таким образом, оба эффекта – собственно - релятивистский и связанный со спин – орбитальным взаимодействием имеют один порядок величины: 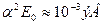
Энергетическая добавка 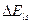 должна быть учтена наряду с релятивисткой поправкой D
должна быть учтена наряду с релятивисткой поправкой D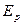 при определении энергии электрона в атоме.
при определении энергии электрона в атоме.
Таким образом, энергия атома равна
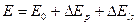 (5.6)
(5.6)
Подставляя в (5.6) соотношения (5.3), (5.5) и учитывая, что у одноэлектронного атома 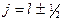 , получим
, получим
 , (5.7)
, (5.7)
где,  (5.8)
(5.8)
Таким образом, вследствие влияния обоих факторов все уровни одноэлектронного атома согласно (5.7) расщепляются на два подуровня по числу возможных значений квантового числа j. Это расщепление (поскольку масштаб его мал) называется тонким или мультиплетным расщеплением. Поэтому безразмерная постоянная a, определяющая масштаб расщепления, называется постоянной тонкой структуры. Из (5.7), (5.8) следует, что величина расщепления уровня (разница энергий между подуровнями 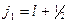 и
и 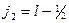 одного и того же уровня между
одного и того же уровня между 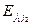 ) равна:
) равна:
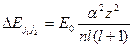 (5.9)
(5.9)
Из (5.9) видно, что наличие дублетного расщепления уровня зависит от заряда (~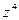 ) и быстро убывает с увеличением главного (~1/
) и быстро убывает с увеличением главного (~1/ ) и орбитального квантовых чисел (~1/
) и орбитального квантовых чисел (~1/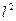 ).
).
 5.3.3. Тонкая структура энергетических уровней атома щелочных элементов
5.3.3. Тонкая структура энергетических уровней атома щелочных элементов
Из результатов предыдущего параграфа следует, что поскольку при расчете энергии валентного (оптического) электрона в атоме щелочного элемента не учитывали спина электрона, то соотношение (5.2) необходимо уточнить, т.е. учесть эффекты собственно релятивистский и связанный со спин-орбитальным взаимодействием.
Учет релятивистской поправки  и энергетической добавки
и энергетической добавки 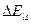 , осуществленный методом, аналогичным рассмотренному в 5.3.2. приведет соотношение (5.2) к виду
, осуществленный методом, аналогичным рассмотренному в 5.3.2. приведет соотношение (5.2) к виду
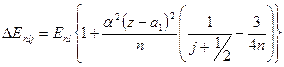 (5.10)
(5.10)
Из (5.10) видно, что все энергетические уровни атома щелочного элемента (за исключением s- уровней) расщеплены на два подуровня (по числу возможных значений квантового числа j у атома с одним оптическим электроном). Причем, как это следует из (5.10), величина расщепления уровня (разница энергий между подуровнями 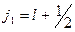 и
и 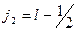 одного и того же уровня n, l) равна
одного и того же уровня n, l) равна
 (5.11)
(5.11)
Из сравнения (5.11) и (5.9) вытекает, что величина расщепления уровня атома щелочного элемента значительно больше (~ ), чем у атома водорода(
), чем у атома водорода(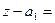 z эфф>1; z у водорода равен 1) и быстро растет с увеличением z. Это связано со следующим обстоятельством: величина расщепления уровня пропорциональна (1/ r3) [9], т.е. существенно определяется областью малых значений r. На малых же расстояниях (внутри атомного остатка) заряд ядра не полностью экранируется электронами внутренних оболочек, поэтому эффективный заряд z эфф> e.
z эфф>1; z у водорода равен 1) и быстро растет с увеличением z. Это связано со следующим обстоятельством: величина расщепления уровня пропорциональна (1/ r3) [9], т.е. существенно определяется областью малых значений r. На малых же расстояниях (внутри атомного остатка) заряд ядра не полностью экранируется электронами внутренних оболочек, поэтому эффективный заряд z эфф> e.
Согласно современной теории атома (что частично видно из изложенного выше) состояние электрона в атоме может быть охарактеризовано набором из четырех квантовых чисел, например: n, l, j, mj. n- главное квантовое число. Оно определяет в первом, самом грубом, приближении энергию электрона в атоме и принимает значения n =1,2,3,4 и т.д.
l- орбитальное квантовое число, определяющее орбитальный момент импульса электрона. При заданном n оно принимает значения l=0,1… n -1. Соответствующие состояния с l=0,1,2,3 и т.д. обозначаются s,p,d,f и т.д. s=1/2- спиновое кантовое число, определяющее величину собственного момента импульса электрона.
j- внутреннее квантовое число, определяющее полный момент импульса электрона в атоме. Оно при заданных l и s принимает значения j= l+s,l+s-1,…,½l-s½, т.е. всего 2 s +1 значение.
mj –магнитное внутреннее квантовое число. Оно определяет величину проекции полного момента импульса электрона на какое либо направление (направление магнитного поля). При заданном j оно принимает значения mj = j, j-1, j-2, …, -j, т.е. всего 2 j+1 значение.
Если внешних полей нет, то несмотря на то, что состояние движения электрона в атоме характеризуется четырьмя квантовыми числами, энергия валентного электрона в атоме с одним оптическим электроном определяется тремя квантовыми числами n,l, j (внешнего поля нет и нет зависимости от ориентации момента, т.е. от mj см (5.10)), однако, энергия водородоподобного атома зависит только от двух квантовых чисел n, j (5.7).
Для обозначения состояния электрона в атоме применяется специальная символика, т.е. определенная форма записи заданного набора квантовых чисел. Записывается латинская буква, соответствующая орбитальному числу, внизу справа от этой буквы значение внутреннего квантового числа j, слева вверху – мультиплетность, т.е. значение 2 s +1 (s – спиновое квантовое число). Перед латинской буквой пишется значение главного квантового числа n.
Основное состояние оптического электрона в атоме щелочного элемента записывается  , что соответствует l =0, s =1/2, j =1/2, n =2 для Li, n =3 для Na и т.д.
, что соответствует l =0, s =1/2, j =1/2, n =2 для Li, n =3 для Na и т.д.
На основании (5.10), в согласии с последними замечаниями, можно графически представить энергетический спектр атома щелочного элемента так, как это показано на рис. 5.1.
 Если атом (например, натрий) находится в основном состоянии (3
Если атом (например, натрий) находится в основном состоянии (3 ), то при возбуждении, согласно правилам отбора, возможны переходы только в Р – состояния и тем самым, возможно, появление главной серии (3 S – nP). Но P – термы (уровни) дублетны, поэтому главная серия будет дублетной (см. рис. 5.1.). Если атом лития находится в 3P – состоянии, то возможны переходы в S и D состояния. При этом в согласии с правилами отбора, возникают дублетные линии резкой серии (3P – nS) и триплетные линии диффузной серии (3P – nD).
), то при возбуждении, согласно правилам отбора, возможны переходы только в Р – состояния и тем самым, возможно, появление главной серии (3 S – nP). Но P – термы (уровни) дублетны, поэтому главная серия будет дублетной (см. рис. 5.1.). Если атом лития находится в 3P – состоянии, то возможны переходы в S и D состояния. При этом в согласии с правилами отбора, возникают дублетные линии резкой серии (3P – nS) и триплетные линии диффузной серии (3P – nD).
Атом натрия. В данной работе изучается спектр испускания атома натрия. На его диаграмме уровней энергии (рис. 5.1.) для большей наглядности уровни с одинаковыми значениями орбитального квантового числа выделены в отдельные «лесенки». Там же для сравнения показаны уровни энергии атома водорода.F – и D – уровни натрия практически не отличаются от водородных, и квантовые дефекты для них близки к нулю: 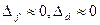 . Однако расположение нижних уровней s – и p – состояний заметно отличается от водородных. Так, уровень 42S лежит гораздо ниже, чем уровень 32D, т.е. имеет место уже упоминавшееся перемешивание уровней с разными n. (В отличие от состояний уровни энергии принято обозначать заглавными буквами S,P,D,F,G и т.д.)
. Однако расположение нижних уровней s – и p – состояний заметно отличается от водородных. Так, уровень 42S лежит гораздо ниже, чем уровень 32D, т.е. имеет место уже упоминавшееся перемешивание уровней с разными n. (В отличие от состояний уровни энергии принято обозначать заглавными буквами S,P,D,F,G и т.д.)
Тонкая структура уровней. Все уровни с l ¹0 состоят из двух близко расположенных компонент (дублетов). Это так называемая тонкая структура. Тонкой она называется потому, что расщепление уровней мало по сравнению с расстоянием между уровнями n и l. Причиной тому является магнитное взаимодействие спинового и орбитального моментов электрона. Спиновый магнитный момент электрона  может принимать две различные ориентации в магнитном поле В l, которое возникает вследствие его же орбитального движения. При этом появляется добавка к энергии атома DE l,s = -
может принимать две различные ориентации в магнитном поле В l, которое возникает вследствие его же орбитального движения. При этом появляется добавка к энергии атома DE l,s = - В l, которая принимает два разных значения в зависимости от взаимной ориентации векторов
В l, которая принимает два разных значения в зависимости от взаимной ориентации векторов  и В l. Двум ориентациям отвечают два значения внутреннего квантового числа j = l – 1/2 и j = l +1/2, причем уровень при j = l – 1/2 обычно лежит ниже уровня при j = l +1/2.
и В l. Двум ориентациям отвечают два значения внутреннего квантового числа j = l – 1/2 и j = l +1/2, причем уровень при j = l – 1/2 обычно лежит ниже уровня при j = l +1/2.
Количественное рассмотрение спин – орбитального взаимодействия упрощается в системе координат, жестко связанной с электроном, поскольку именно в данной системе взаимодействия является чисто магнитным, причем поле В l обусловлено движением эффективного ядра. Расчет приводит к формуле
 , (5.11а)
, (5.11а)
из которой видна зависимость величины расщепления от орбитального квантового числа l и эффективного заряда ядра 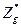 . Здесь a - постоянная тонкой структуры, которая равна
. Здесь a - постоянная тонкой структуры, которая равна
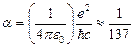 .
.
Для S – уровней спин – орбитальное взаимодействие отсутствует. Они не расщепляются, т.е. являются синглетами, потому что в s – состояниях отсутствуют орбитальные механический и магнитный моменты и В l = 0.
Следует иметь в виду, что эффективный заряд 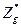 не совпадает с эффективным зарядом
не совпадает с эффективным зарядом 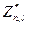 ,входящим в формулу (5.1), для энергии электрона: он оказывается заметно больше. Это объясняется тем, что экранировка магнитного взаимодействия электронами атомного остова значительно слабее по сравнению с экранировкой электростатического взаимодействия.
,входящим в формулу (5.1), для энергии электрона: он оказывается заметно больше. Это объясняется тем, что экранировка магнитного взаимодействия электронами атомного остова значительно слабее по сравнению с экранировкой электростатического взаимодействия.
Правила отбора и спектр. Квантовые переходы между состояниями атома с испусканием или поглощением света возможны лишь при определенных ограничениях, накладываемых на величину изменения квантовых чисел так называемыми правилами отбора.
Переходы возможны, если орбитальное квантовое число начального и конечного состояний атома различается на единицу, т.е.
D l =±1, (5.12)
а квантовое число полного момента этих состояний либо так же различается на единицу, либо имеет одинаковые значения (не нулевые!):
D j =0,±1. (5.13)
Излучательные переходы при иных изменениях квантовых чисел l и j запрещены. Главное квантовое число n может изменяться при переходах на любую величину либо совсем не изменяться.
Правило отбора по орбитальному квантовому числу (5.12) связано с законом сохранения четности волновой функции.
Правило отбора по квантовому числу полного момента (5.13) станет понятным, если учесть, что фотон имеет спиновой момент импульса, равный 1ћ, и что при рождении или поглощении фотона должен выполняться закон сохранения момента импульса. Фотон может ориентироваться спином в момент вылета из атома параллельно, антипараллельно и перпендикулярно по отношению к полному моменту импульса атома в конечном состоянии. Если спин фотона параллелен конечному моменту атома, то для выполнения закона сохранения момента импульса полный момент в конечном состоянии должен быть на 1ћ меньше в начальном. Это происходит за счет уменьшения орбитального момента в процессе испускания фотона. При антипараллельной ориентации спина фотона по отношению к моменту конечного состояния по той же причине полный и орбитальный моменты конечного состояния должны быть на 1ћ больше моментов начального состояния. Наконец, когда спин фотона перпендикулярен моменту конечного состояния, полный момент при испускании меняться не должен. Но орбитальный момент уменьшается на 1ћ (ведь для образования фотона необходимо откуда-то взять момент, равный 1ћ). Однако, несмотря на уменьшение орбитального момента, полный момент не уменьшается потому, что в процессе излучения спин электрона переворачивается из антипараллельного положения в параллельное. Это и компенсирует уменьшение орбитального момента, входящего составной частью в полный момент.
Правило отбора по орбитальному квантовому числу (5.12) связано как с законом сохранения момента импульса, так и с законом сохранения четности волновой функции. Поскольку фотон обладает отрицательной четностью, то в результате его испускания или поглощения четность волновой функции атома должна измениться. Четность Р для атома с одним валентным числом через соотношение Р=(-1) l, и переходы без изменения l (или D l =0) оказываются невозможными. Что касается переходов, при которых D l =±3, ±5,…, то на них накладывает запрет закон сохранения момента импульса.
Правила отбора по l приводят к появлению в спектре испускания натрия нескольких серий спектральных линий. Как известно, серию образуют спектральные линии с общим нижним уровнем, причем обычно они располагаются в одной спектральной области (ультрафиолетовой, видимой, инфракрасной). Волновые числа 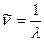 линий, входящих в серию, подчиняются простым закономерностям, называемым сериальными формулами. Ниже приводятся важнейшие серии атома натрия и их сериальные формулы, наблюдающиеся в испускании:
линий, входящих в серию, подчиняются простым закономерностям, называемым сериальными формулами. Ниже приводятся важнейшие серии атома натрия и их сериальные формулы, наблюдающиеся в испускании:
Главная серия 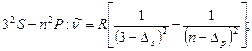
Резкая серия 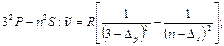
Диффузная серия 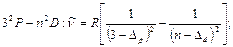
Фундаментальная серия 
где n =4,5,6,….
Главная серия наблюдается также в спектре поглощения, проявляя тем самым сходство с серией Лаймана для водорода. Некоторые квантовые переходы из приведенных серий показаны на рис.5.1.
Принятые в спектроскопии буквенные обозначения состояний с различными значениями орбитального квантового числа l =0,1,2,3 происходят как раз от наименования серий в спектрах щелочных элементов. Буквы s, p, d, f являются начальными буквами английских названий серий s (sharp – резкая), p (principal – главная), d (diffuse – диффузная), f (fundamental – фундаментальная).
Тонкая структура линий. Зная тонкую структуру уровней, нетрудно выяснить характер расщепления линий различных серий. Учитывая правила отбора по j (D j =0,±1), получаем:
Главная серия–дублеты
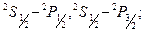

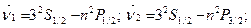
Резкая серия–дублеты
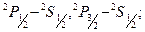
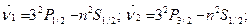
Диффузная серия–триплеты
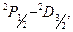
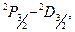
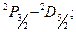
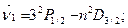
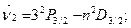
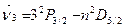
Фундаментальная серия–триплеты
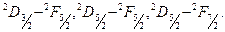
При анализе экспериментальных данных надо учитывать быстрое убывание тонкого расщепления с увеличением n и l, следующее из формулы (5.11а). Дублетное расщепление линий главной серии определяется тонкой структурой верхних уровней 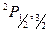 , так как нижний уровень является синглетным (рис.5.2). Поэтому дублетное расщепление особенно велико для головной линии главной серии
, так как нижний уровень является синглетным (рис.5.2). Поэтому дублетное расщепление особенно велико для головной линии главной серии 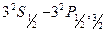 . При переходе к высшим, более коротковолновым членам серии оно быстро падает. Дублетное расщепление линии резкой серии, наоборот, полностью определяется тонкой структурой нижнего уровня
. При переходе к высшим, более коротковолновым членам серии оно быстро падает. Дублетное расщепление линии резкой серии, наоборот, полностью определяется тонкой структурой нижнего уровня  , и все линии резкой серии имеют в шкале частот или волновых чисел одинаковые дублетные расщепления.
, и все линии резкой серии имеют в шкале частот или волновых чисел одинаковые дублетные расщепления.
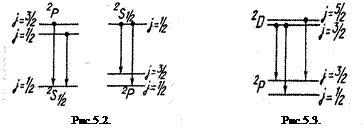 Расстояние между двумя компонентами триплета
Расстояние между двумя компонентами триплета 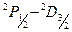 и
и 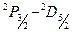 определяется расщеплением нижнего уровня и постоянно для всех линий серии (рис.5.3.). Расстояние же между компонентами
определяется расщеплением нижнего уровня и постоянно для всех линий серии (рис.5.3.). Расстояние же между компонентами 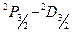 и
и 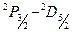 , определяемое расщеплением верхнего уровня, значительно меньше по величине и быстро убывает для высших членов серии. При небольшой разрешающей силе спектрального прибора эти компоненты не разрешаются и линии диффузной серии имеют вид дублетов. Аналогичным образом легко установить структуру линий фундаментальной серии.
, определяемое расщеплением верхнего уровня, значительно меньше по величине и быстро убывает для высших членов серии. При небольшой разрешающей силе спектрального прибора эти компоненты не разрешаются и линии диффузной серии имеют вид дублетов. Аналогичным образом легко установить структуру линий фундаментальной серии.
Дублетное расщепление линий в шкале волновых чисел равно (см. формулу (5.11а)):
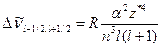 (5.14)
(5.14)
5.4. Экспериментальная установка
 Исследование тонкой структуры ряда спектральных линий атома натрия осуществляется на установке, общий вид которой изображен на рис 5.4.
Исследование тонкой структуры ряда спектральных линий атома натрия осуществляется на установке, общий вид которой изображен на рис 5.4.
Источником возбуждения исследуемого спектра служит дуговой разряд между угольными электродами, в канал одного из них (нижнего) помещена соль натрия. В результате последнего разряд происходит в парах натрия. Термические электроны при неупругих столкновениях с атомами передают им свою энергию. При этом внутренняя энергия возрастает – его оптический электрон переходит из основного состояния в возбужденное, (т.е. на какой – либо выше расположенный энергетический уровень). В возбужденном состоянии атом находится короткое время (t~ 10-7-10 -8сек). Затем оптический электрон с верхнего уровня переходит либо в основное (самое глубокое) состояние, либо на какой – нибудь ниже расположенный уровень, а уже с него в основное состояние. При этих переходах электрона разность его энергии на различных уровнях будет излучаться в виде фотонов той или иной длины волны. Так возникает эмиссионный линейчатый спектр в натриевой дуге.
Спектрограф ДФС-8. Для исследования тонкой структуры спектра натрия в лабораторной работе используется спектрограф ДФС-8. Его оптическая схема приведена на рис.5.4.
Свет от натриевой дуги через осветительные линзы (1,2,3), регулируемую щель (4), попадает на поворотное зеркало (5). От него отраженный луч попадает на зеркальный объектив (6), причем в его фокусе находится щель (4). От объектива (6) параллельный пучок света направляется на отражающую дифракционную решетку (7). Далее, отраженный от решетки, свет собирается зеркальным объективом (6) и направляется на фотопластинку (12).
ДФС-8 – спектральный прибор достаточно высокого разрешения. Поэтому для получения области спектра 330-620 нм, где расположены основные линии Na необходимо фотографировать спектр при различных положениях решетки. При атом для получения нужного участка спектра с помощью барабана поворачивают решетку на нужный угол, который контролируется по шкале – указателю длин волн света, попадающего от решетки на фотопластинку.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 3663; Нарушение авторских прав?; Мы поможем в написании вашей работы!