
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Молекулярные спектры
|
|
|
|
Химические связи и строение молекул.
Молекула – наименьшая частица вещества, состоящая из одинаковых или различных атомов, соединенных между собой химическими связями, и являющаяся носителем его основных химических и физических свойств. Химические связи обусловлены взаимодействием внешних, валентных электронов атомов. Наиболее часто в молекулах встречается два типа связи: ионная и ковалентная.
Ионная связь (например, в молекулах NaCl, КВr) осуществляется электростатическим взаимодействием атомов при переходе электрона от одного атома к другому, т.е. при образовании положительного и отрицательного ионов.
Ковалентная связь (например, в молекулах Н2, C2, CO) осуществляется при обобществлении валентных электронов двумя соседними атомами (спины валентных электронов должны быть антипараллельны). Ковалентная связь объясняется на основе принципа неразличимости тождественных частиц, например электронов в молекуле водорода. Неразличимость частиц приводит к обменному взаимодействию.
Молекула является квантовой системой; она описывается уравнением Шредингера, учитывающим движение электронов в молекуле, колебания атомов молекулы, вращение молекулы. Решение этого уравнения – очень сложная задача, которая обычно разбивается на две: для электронов и ядер. Энергия изолированной молекулы:
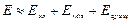 , (13.1)
, (13.1)
где 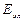 – энергия движения электронов относительно ядер,
– энергия движения электронов относительно ядер, 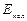 – энергия колебаний ядер (в результате которых периодически изменяется относительное положение ядер),
– энергия колебаний ядер (в результате которых периодически изменяется относительное положение ядер), 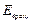 – энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве). В формуле (13.1) не учтены энергия поступательного движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не квантуется, поэтому ее изменения не могут привести к возникновению молекулярного спектра, а вторую можно не учитывать, если не рассматривать сверхтонкую структуру спектральных линий. Доказано, что
– энергия вращения ядер (в результате которых периодически изменяется ориентация молекулы в пространстве). В формуле (13.1) не учтены энергия поступательного движения центра масс молекулы и энергия ядер атомов в молекуле. Первая из них не квантуется, поэтому ее изменения не могут привести к возникновению молекулярного спектра, а вторую можно не учитывать, если не рассматривать сверхтонкую структуру спектральных линий. Доказано, что 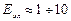 эВ,
эВ, 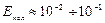 эВ,
эВ, 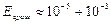 эВ, поэтому
эВ, поэтому 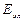 >>
>>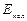 >>
>>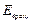 .
.
Каждая из входящих в выражение (13.1) энергий квантуется (ей соответствует набор дискретных уровней энергии) и определяется квантовыми числами. При переходе из одного энергетического состояния в другое поглощается или испускается энергия D E=hv. При таких переходах одновременно изменяются энергия движения электронов, энергии колебаний и вращения. Из теории и эксперимента следует, что расстояние между вращательными уровнями энергии D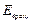 гораздо меньше расстояния между колебательными уровнями D
гораздо меньше расстояния между колебательными уровнями D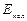 , которое, в свою очередь, меньше расстояния между электронными уровнями D
, которое, в свою очередь, меньше расстояния между электронными уровнями D . На рисунке 13.1 схематически представлены уровни энергии двухатомной молекулы (для примера рассмотрены только два электронных уровня – показаны жирными линиями).
. На рисунке 13.1 схематически представлены уровни энергии двухатомной молекулы (для примера рассмотрены только два электронных уровня – показаны жирными линиями).
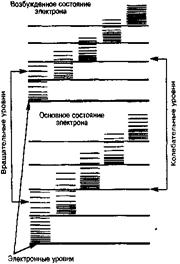 Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах – спектрах излучения (поглощения), возникающих при квантовых переходах между уровнями энергии молекул. Спектр излучения молекулы определяется структурой ее энергетических уровней и соответствующими правилами отбора.
Строение молекул и свойства их энергетических уровней проявляются в молекулярных спектрах – спектрах излучения (поглощения), возникающих при квантовых переходах между уровнями энергии молекул. Спектр излучения молекулы определяется структурой ее энергетических уровней и соответствующими правилами отбора.
Итак, при разных типах переходов между уровнями возникают различные типы молекулярных спектров. Частоты спектральных линий, испускаемых молекулами, могут соответствовать переходам с одного электронного уровня на другой ( электронные спектры)или с одного колебательного (вращательного) уровня на другой (колебательные (вращательные) спектры).Кроме того, возможны и переходы с одними значениями 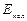 и
и 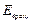 на уровни, имеющие другие значения всех трех компонентов, в результате чего возникают электронно-колебательные и колебательно-вращательные спектры.
на уровни, имеющие другие значения всех трех компонентов, в результате чего возникают электронно-колебательные и колебательно-вращательные спектры.
Типичные молекулярные спектры – полосатые, представляющие собой совокупность более или менее узких полос в ультрафиолетовой, видимой и инфракрасной областях.
Применяя спектральные приборы высокой разрешающей способности, можно видеть, что полосы представляют собой настолько тесно расположенные линии, что они с трудом разрешаются. Структура молекулярных спектров различна для разных молекул и с увеличением числа атомов в молекуле усложняется (наблюдаются лишь сплошные широкие полосы). Колебательными и вращательными спектрами обладают только многоатомные молекулы, а двухатомные их не имеют. Это объясняется тем, что двухатомные молекулы не имеют дипольных моментов (при колебательных и вращательных переходах отсутствует изменение дипольного момента, что является необходимым условием отличия от нуля вероятности перехода). Молекулярные спектры применяются для исследования строения и свойств молекул, используются в молекулярном спектральном анализе, лазерной спектроскопии, квантовой электронике и т.д.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 974; Нарушение авторских прав?; Мы поможем в написании вашей работы!