
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворы
|
|
|
|
ЛЕКЦИЯ №9
Все вещества в одной Катализатор находится в
фазе 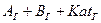 в другой фазе.
в другой фазе. 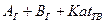
Ускоряет действие катализатора работает поверхность ускоряющее
Получаются нестойкие соединения действие катализ. 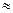 поверхность
поверхность
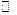 Случай гомогенного катализа: хим. теория
Случай гомогенного катализа: хим. теория 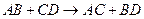
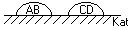
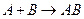 Е
Е
1. 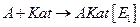
2. 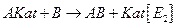 Катализатор сорбирует на своей
Катализатор сорбирует на своей
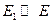
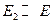 поверхности металлы
поверхности металлы
Роль катализатора - уменьшение Процесс абсорбции
потенциального барьера, т.е. А…Kat С…Kat
увеличение скорости реакции. B…Kat D…Kat
Ослабление межмолекулярных связей,
молекулы становятся возбужденными
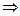 идет реакция
идет реакция
По Баландину: чтобы ускорить ту или
иную реакцию, необходимо выдержать
геометрическое расположение между
молекулами и активными центрами.
Раствор – термодинамическая равновесная (гомогенная) система, состоящая из двух или более фаз.
Истинный раствор, когда размеры частиц соизмеримы с размерами молекул, ионов 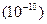
Коллоидный раствор (НМ) Суспензия (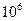 )
)
Фаза, в которой больше – растворитель, меньше – растворимое вещество
 Х – концентрация
Х – концентрация 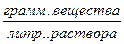 Y – концентрация
Y – концентрация 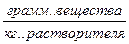
g – процентная концентрация 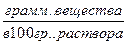
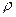 - плотность
- плотность 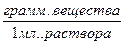
1мл.=1см3
С, СМ, М – молярность 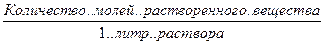
СН, Н – нормальность 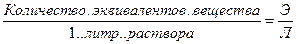
M – моляльность 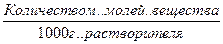
Т – титр 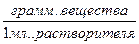
N – мольная доля 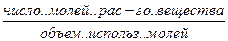
Виды растворов:
1. Разбавленные (малой концентрации)
2. Концентрированные (большой концентрации)
3. Насыщенные (предельно допустимая концентрация)
4. Пересыщенные (концентрация больше предельно допустимой, такие растворы неравновесные)
Растворимость газов в газах: растворяются неограниченно, в любых пропорциях.
Растворимость газов в жидкостях: Справедлив закон Генри: при постоянной температуре растворимость газа пропорциональна его давлению. С=ГР Г – постоянная Генри. С ростом температуры – растворимость уменьшается.
Закон Дальтона: Растворимость газа из смеси газа пропорциональна его парциальному давлению.
Растворимость жидкостей в жидкостях: 2 случая
- неограниченная растворимость
- ограниченная растворимость
Растворимость меняется при изменении температуры: при низкой – неполная растворимость, при высокой – полная.
 1 – не растворяется в 2
1 – не растворяется в 2
3 – растворяется и в 1 и в 2
К – коэф-т распределения 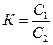
Пример: раствор йода в воде – хотим убрать йод, добавим хлороформ.
Йод – 3, хлороформ – 2, вода – 1 К=130 (раствор йода в хлороформе)
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 414; Нарушение авторских прав?; Мы поможем в написании вашей работы!