
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства соединений цинка, кадмия и ртути
|
|
|
|
Металлы IIБ-группы реагируют при нагревании с галогенами (если без нагревания, то необходимо увлажнение), кислородом, серой. Цинк и кадмий реагируют также с фосфором.
При взаимодействии с кислородом образуются оксиды общей формулы МО. Оксиды имеют характерную окраску: ZnО — белый, СdO — коричневый, НgО — желтый или красный. Оксиды не растворяются в воде, но растворяются в кислотах.
Оксидам МО соответствуют гидроксиды типа М(ОН)2, нерастворимые в воде. Термическая устойчивость гидроксидов Zn (II) и Сd(II) значительно выше гидроксида ртути (II), который разлагается в момент осаждения из раствора.
При обработке НgО водным раствором NНз образуется желтый осадок (основание Миллона):
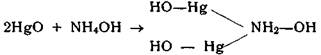
При нагревании этого соединения до 125°С образуется гидроксид:
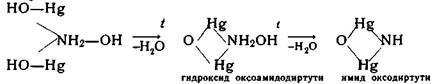
Диспергированный гидроксид ртути (II) в коллоидном состоянии служит бактерицидным средством. Антисептическим действием обладает также белый осадок ртути амидохлорида, который получается взаимодействием водного раствора аммиака с сулемой (НgСl2) или каломелью (Нg2Сl2):
НgСl2 + 2NН3 → НgNH2Сl + NН4Сl
Нg2Сl2 + 2NН3 → НgNН2Сl + NН4Сl + Нg
Обе реакции используются в химическом анализе для обнаружения ионов Нg2+ и Нg22+.
Амидохлорид ртути НgNН2Сl может взаимодействовать в биологической системе с сульфогидроксильными группами белков. Этим объясняется антисептическое действие амидохлорида ртути.
Для обнаружения ионов аммония NH4+ также используются соединения ртути К2[НgI4] (калий тетраиодомеркурат — реактив Несслера)
2К2[НgI4] + NН3 + 3КОН → НОНgNННgI + 7КI + 2Н2О
Из других солей ртути в медицине и ветеринарии применялись Нg2Сl2 и НgСl2.
Каломель в воде растворяется незначительно и поэтому менее токсична, чем сулема.
Сулема НgСl2 представляет собой бесцветные кристаллы, достаточно хорошо растворимые в воде, спирте, эфире, пиридине и др.
Интересно, что в водных растворах НgСl2 почти не диссоциирует и находится в молекулярной форме. Поэтому водные растворы сулемы не проводят электрический ток.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1231; Нарушение авторских прав?; Мы поможем в написании вашей работы!