
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Опираясь на имеющиеся данные получаем, что
|
|
|
|
p С(МеC) <0
и возрастает в последовательности
Мо2С– Fe3С–Со3С–Ni3C
Параллельно возрастанию активности углерода, которая оказывается выше, чем у графита (pС=0). Для другого ряда карбидов
p С(МеC) <0,
т.е. активность углерода оказывается ниже, чем у графита, и понижается в последовательности
Al4C3-CaC2-Cr4C-Mn3C-SiC-ZnC-TiC.
Согласно равенству, при этом понижается содержания СО в газовой фазе, необходимое для полного науглероживания металла. Кривая предельного науглероживания, подобная SЕ, при увеличении химического сродства металла к углероду должна смещаться в область малых содержаний СО.
Источником углерода, поглощаемого металлом, могут быть другие компоненты газовой фазы. К ним следует отнести такие активные карбюризаторы, как углеводороды различной сложности. Их действие можно оценить на примере цементации железа простейшем углеводородом – метаном СН4. его особенности выявляются из закономерностей реакции образования – разложения
Сгр+2Н2= СН4 +ΔH1
В сравнении с реакцией
Сгр+СО2=2СО –ΔH2,
которая ранее служила источником углерода.
Опираясь на принцип смещения равновесий, можно отметить противоположное действие факторов, содействующих распаду СН4 и СО и выделению углерода. В случае метана этому содействует повышение температуры и понижения давления, что, напротив, уменьшает полноту разложения окиси углерода. Отмеченные особенности отражаются в количественных выражениях ΔH и ΔG° образования метана:
ΔG°=-46240+26,96Т
и константы равновесия
Кр(71)=РСН4/Р²Н2
lnКр=2418/Т-1,41
Равновесные кривые метановой реакции имеют сходство с кривыми газификации, но имеют противоположное расположение по отношению к оси температур (рис 9).
Отмеченные особенности метана накладывают свой отпечаток на реакции цементации, которые развиваются с образованием растворов.
СН4 = [С]Fe+2Н2 +ΔH1
Или до предельного науглероживания железа
СН4 + 3Fe = Fe3С+ 2Н2 +ΔH2
Другие возможные варианты реакций и равновесии можно установить, как и ранее, на основе диаграмме состояния Fe-C и правила фаз. Для всех вариантов справедливо одно и то же выражение константы равновесия при разных соотношениях РСН4/Р²Н2 и величин активности ас в зависимости от состояния углерода в твердых фазах:
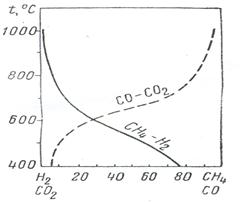 Рис.9. Равновесные кривые реакции образования диссоциации метана при Р=1,013·10⁵ н/м². (1,0 атм).
Рис.9. Равновесные кривые реакции образования диссоциации метана при Р=1,013·10⁵ н/м². (1,0 атм).
Кр1= Кр2= Кр3= Кр4= РСН4/Р²Н2 · а С=Кр
Количественные данные по равновесиям метановых реакций неоднократно определялись экспериментальным путем. Однако возможен расчетный переход от известных данных для цементации железа СО к реакциям цементации метаном:
1) 3Fe+2CO= Fe3С+CO2; -ΔH1
2) CO2+С=2СО +ΔH2
3) СН4 =С+2Н2 +ΔH3
4) СН4 +3Fe= Fe3С+ 2Н2 +ΔH4
ΔG°4= ΔG°1+ ΔG°2+ ΔG°3;
ΔH4= ΔH1+ ΔH2+ ΔH3
ΔG°4= RT lnКр (71)
На основе количественных данных построена равновесная диаграмма цементации железа метаном (рис.10). при замене окиси углерода метаном изменяется форма диаграммы и положение равновесных кривых по отношению к температурной оси. Они выражают теперь более полное науглероживание с повышением температуры и понижением давления. В последнем случае равновесные кривые смещаются влево, в сторону меньших содержании СН4 в газовой фазе.

Рис.10. диаграмма равновесии науглероживания железа метаном.
Следует отметить широкие поля устойчивости цементита Fe3С и феррита при сужении области аустенита. Относительно небольшие изменения в составе газовой фазы могут вызвать значительные науглероживания железа. С другой стороны, газ, богатый водородом, обеспечивает довольно полное обезуглероживания металла без описания его окисления. Диаграмма ориентирует при выборе условий- состава газовой фазы и температуры, при которых превращения развиваются до заданного конечного состава конденсированной фазы.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 432; Нарушение авторских прав?; Мы поможем в написании вашей работы!