
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоемкость
|
|
|
|
Первое начало (первый закон) термодинамикиявляется обобщением закона сохранения и превращения энергии для термодинамической системы. Количество теплоты, полученное термодинамической системой, идет на изменение внутренней энергии системы и совершение системой работы над внешними телами.
В этой формулировке и соответствующей ей формуле (2.1.2) предполагается следующее правило знаков:
D U > 0, если внутренняя энергия термодинамической системы увеличивается; соответственно, D U < 0, если внутренняя энергия уменьшается.
Q > 0, если система получает тепло, и Q < 0, если отдает тепло.
A > 0, если система совершает работу над внешними телами, и A < 0, если внешние силы совершают над системой работу.
Первое начало термодинамики для элементарного процесса, т.е. такого процесса, в котором изменения термодинамических параметров бесконечно малы, принимает следующий вид:
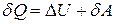 . (2.1.3)
. (2.1.3)
В формуле (2.1.3) для элементарной работы и элементарного количества теплоты введены обозначения dA и dQ. Это связано с тем, что в отличие от изменения внутренней энергии, которое выражается в виде разности внутренних энергий в конечном (U 2) и начальном (U 1) состояниях системы: 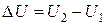 , такое представление для элементарных работы и количества теплоты невозможно.
, такое представление для элементарных работы и количества теплоты невозможно.
Первое начало термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Важным следствием первого начала термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины. Такая гипотетическая машина получила название вечного двигателя (perpetuum mobile) первого рода. Многочисленные попытки создать ее неизменно заканчивались провалом, т.к. любая машина может совершать положительную работу A над внешними телами только за счет получения некоторого количества теплоты Q от окружающих тел или уменьшения ΔU своей внутренней энергии.
Теплоемкостью вещества называется величина, численно равная количеству теплоты, которое надо подвести к веществу, чтобы увеличить его температуру на 1 К.
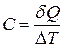 . (2.2.1)
. (2.2.1)
Теплоемкость зависит от способа передачи энергии, т.е. не определяется однозначно формулой (2.2.1), поэтому следует оговорить, каким образом происходит подвод тепла.
Удельной теплоемкостью вещества называется величина, численно равная количеству теплоты, которое надо подвести к 1 кг вещества, чтобы увеличить его температуру на 1 К.
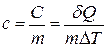 . (2.2.2)
. (2.2.2)
Молярной теплоемкостью (теплоемкостью одного моля) вещества называется величина, численно равная количеству теплоты, которое надо подвести к 1 молю вещества, чтобы увеличить его температуру на 1 К.
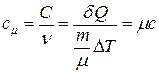 . (2.2.3)
. (2.2.3)
Позже рассмотрим подробнее теплоемкости для различных процессов, происходящих с идеальным газом.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 349; Нарушение авторских прав?; Мы поможем в написании вашей работы!