
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Теплоемкость идеального газа
|
|
|
|
Первое начало термодинамики для изопроцессов.
1. Для изотермического процесса T = const, Þ D U = 0. Тогда
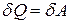 . (2.6.1)
. (2.6.1)
2. Для изохорного процесса V = const, Þ dA = 0. В этом случае
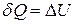 . (2.6.2)
. (2.6.2)
3. Для изобарного процесса P = const, Þ 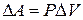 . Тогда
. Тогда
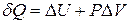 . (2.6.3)
. (2.6.3)
Как отмечалось ранее в §2, теплоемкость зависит от способа передачи тепла, т.е. от процесса перехода идеального газа из одного состояния в другое.
Для изотермического процесса D T = 0, поэтому теплоемкость в таком процессе 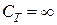 .
.
Теплоемкость газа, участвующего в изохорном процессе называется теплоемкостью при постоянном объёме и обозначается CV (удельная теплоемкость - cV, а молярная - cmV).
Пользуясь первым началом термодинамики для изохорного процесса (2.6.2), получим
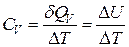 , (2.7.1)
, (2.7.1)
Откуда следует выражение для изменения внутренней энергии:
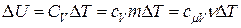 . (2.7.2)
. (2.7.2)
Если изохорный процесс происходит с идеальным газом, то из формулы (2.4.4) для внутренней энергии идеального газа следует, что 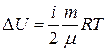 . Тогда для теплоемкостей идеального газа при постоянном объёме получим следующие выражения:
. Тогда для теплоемкостей идеального газа при постоянном объёме получим следующие выражения:
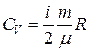 , (2.7.3)
, (2.7.3)
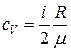 , (2.7.4)
, (2.7.4)
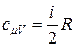 . (2.7.5)
. (2.7.5)
Теплоемкость газа, участвующего в изобарном процессе называется теплоемкостью при постоянном давлении и обозначается Cp (удельная теплоемкость - cp, а молярная - cmp).
Из первого начала термодинамики для изобарного процесса (2.6.3), происходящего с идеальным газом, получим следующее выражение
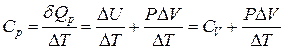 ,
,
которое можно упростить, если воспользоваться уравнением состояния идеального газа: 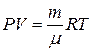 , Þ
, Þ 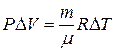 , Þ
, Þ 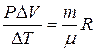 . Тогда
. Тогда
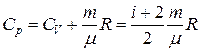 , (2.7.6)
, (2.7.6)
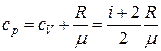 , (2.7.7)
, (2.7.7)
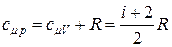 . (2.7.8)
. (2.7.8)
Формулы (2.7.6) - (2.7.8), связывающие теплоемкости при постоянном давлении и объёме, называются уравнениями Майера.
Как видно из формул (2.7.3) - (2.7.8), удельная и молярная теплоемкости при постоянном объёме и постоянном давлении не зависят от параметров состояния идеального газа,
Термодинамические процессы, в которых теплоемкость газа остается неизменной, т.е. не зависящей от давления, объема и температуры газа, называются политропическими.
Уравнение политропического процесса имеет вид:
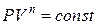 , (2.7.9)
, (2.7.9)
где 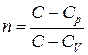 , C = const – теплоемкость политропного процесса.
, C = const – теплоемкость политропного процесса.
Все изопроцессы являются политропными. Так для изотермического процесса (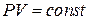 ) n = 1, для изобарного процесса (P = const) n = 0, а изохорного процесса n = ¥. Чтобы получить из (2.7.9), уравнение для случая, когда n = ¥, извлечем из левой части уравнения (2.7.9) корень n -ой степени. Тогда
) n = 1, для изобарного процесса (P = const) n = 0, а изохорного процесса n = ¥. Чтобы получить из (2.7.9), уравнение для случая, когда n = ¥, извлечем из левой части уравнения (2.7.9) корень n -ой степени. Тогда 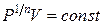 , т.е. при n ® ¥, V = const.
, т.е. при n ® ¥, V = const.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 918; Нарушение авторских прав?; Мы поможем в написании вашей работы!