
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Произведение растворимости. Значительная часть солей неорганических кислот (сульфиды, карбонаты, фосфаты переходных металлов и ряд других) малорастворимы в воде
|
|
|
|
Значительная часть солей неорганических кислот (сульфиды, карбонаты, фосфаты переходных металлов и ряд других) малорастворимы в воде. Поскольку большинство таких солей являются сильными электролитами, то в растворе они находятся в виде ионов. Таким образом малорастворимая соль состава MetxAny в воде будет полностью диссоциирована на катионы металла Metn+ и анионы кислотного остатка Anm–, которые будут находится в равновесии с твердой фазой (осадком MetxAny):
| MetxAny D x Metn+ + y Anm–. | (1.5) |
В соответствии с законом действующих масс можно записать константу равновесия данной реакции:
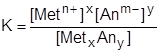 , ,
| (1.6) |
где [Metn+] – молярная концентрация катионов металла, [Anm–] –молярная концентрация анионов кислотного остатка, [MetxAny] – молярная концентрация соли.
Поскольку в силу малой растворимости концентрация соли практически не изменяется, ее значение можно считать постоянной величиной. Поэтому уравнение (1.6) можно переписать в виде:
| [Metn+]x[Anm–]y=const=ПР. | (1.7) |
Т.е. в насыщенном растворе малорастворимой соли произведение концентраций ионов при данной температуре и давлении является величиной постоянной. Данная величина называется произведением растворимости и обозначается ПР. В зарубежной литературе принято обозначение Lp или Sp. Значения ПР для различных солей определяются экспериментально и заносятся в химические справочники.
Произведение растворимости имеет размерность, которая зависит от состава соли и пропорциональна размерности молярной концентрации (моль/л):
CuS D Cu2+ + S2–
ПР(CuS)=[Cu2+][S2–]=3.2×10–38 моль2/л2
Mg3(PO4)2 D 3Mg2+ + 2PO43–
ПР(Mg3(PO4)2)=[ Mg2+]3[PO43–]2=1×10–13 моль5/л5
В справочниках размерность ПР как правило не указывается.
Анализ значения произведения растворимости позволяет ориентировочно оценить, выпадет ли в данных условиях осадок данного вещества или нет. Для этого необходимо концентрацию ионов подставить в выражение (1.7) и сравнить полученное произведение с табличным значением ПР для данной соли. Условием образования осадка является превышение произведения концентрации ионов в степенях соответствующих стехиометрическим коэффициентам малорастворимого электролита над его произведением растворимости.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 697; Нарушение авторских прав?; Мы поможем в написании вашей работы!