
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Химические свойства. Описание и растворимость
|
|
|
|
Описание и растворимость
Получение
Na2B4O7 • 10 H2O
Формы выпуска
Применение
Хранение
В хорошо укупоренной таре.
Наружно как антисептические средства в виде водных, спиртовых и глицериновых растворов, мазей, присыпок
субстанция; 1-2-3% спиртовые растворы, 10% раствор в глицерине, 5% мазь.
Натрия тетраборат (бура) Natrii tetraboras (ЛH)
Sodium tetraborate (MHH)
В природе встречается в свободном виде и в виде минералов.
В химическом отношении, это кристаллогидрат натриевой соли тетраборной кислоты:

Основной промышленный способ– из кислоты борной или борокальцита при нагревании с раствором натрия карбоната:
4Н3ВО3 + Na2CO3 → Na2B4O7 + CO2↑ + 6Н2O
CaB4O7 • 4Н2 O + Na2CO3 → Na2B4O7 + CaCO3 + 4Н2 O
бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок.
Растворим в воде, очень легко в кипящей воде, практически не растворим в спирте, легко растворим в глицерине.
Кислотно-основные.
1.Водные растворы имеют солоновато – щелочной вкус и щелочную реакцию среды, так как происходит гидролиз:
Na2B4O7 + 7Н2O ←→ 4Н3BO3 + 2NaOH
2.Реакция среды глицериновых растворов кислая. При растворении в глицерине образуются натриевая соль глицеринборной кислоты и свободная глицеринборная кислота:
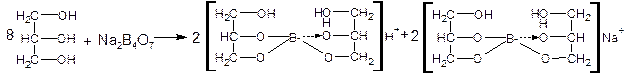
Кислая реакция среды определяется образованием глицероборной кислоты.
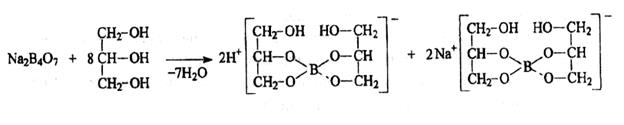
3.Под действием минеральных кислот образуется борная кислота:
Na2B4O7 •10H2O + 2НСl → 4Н3В03 + 2NaCl + 5Н20
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 1074; Нарушение авторских прав?; Мы поможем в написании вашей работы!