
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Коричнево-черный осадок
|
|
|
|
Подлинность
Описание и растворимость
Белый аморфный или мелкокристаллический порошок, без запаха. Практически нерастворим в воде и спирте. Легко растворим в разведенных минеральных кислотах – азотной, хлороводородной, серной.
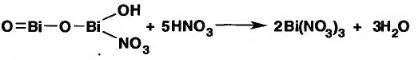
Порошок, смоченный водой, окрашивает синюю лакмусовую бумагу в красный цвет, так как при гидролизе вещества выделяется кислота азотная:
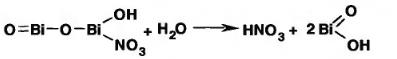
1. При прокаливании JIB образуется остаток ярко-желтого цвета и выделяются бурые пары азота (IV) оксида:
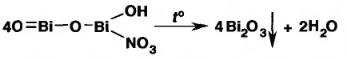 + 2NO2↑ + ½О2 ↑
+ 2NO2↑ + ½О2 ↑
Для проведения реакций подлинности на ионы Bi3+ и NO-
ЛB растворяют в разбавленной кислоте хлороводородной или серной
2. Реакция осаждения раствором натрия сульфида – образование коричнево – черного осадка Bi2S3.
2Bi3+ + 3Na2S → Bi2S3↓ + 6Na+
Из концентрированных растворов соли выпадает осадок коричнево – черного цвета, при меньшем содержании висмута образуется коричнево – черное окрашивание. Реакция очень чувствительная, висмут открывается в разведении 1: 100000 (0,001%).
Осадок не растворим в минеральных кислотах, кроме НNО3:
Bi2S3 + 8НNО3 → 2 Bi(NO3)3 + 2NO2↑ +4H2O + 2S↓
3. Реакция осаждения и комплексообразования с раствором калия йодида.
Ион висмута с раствором калия йодида образует черный осадок висмута йодида:
Bi3+ + 3KI → BiI3↓ + ЗК+
2 капли черный осадок
Осадок растворяется в избытке реактива с образованием желто-оранжевого раствора комплексного соединения - калия тетрайодвисмутата (III):
BiI3 + KI → K[BiI4]
избыток желто-оранжевое окрашивание
4. Реакция осаждения раствором натрия гидроксида или раствором аммиака:
Bi3+ + 3NaOH → Bi(OH ) 3↓+ 3Na+
Образуется белый осадок висмута гидроксида, нерастворимый в избытке реактива и растворимый в минеральных кислотах.
5. Доказательство нитрат-иона. Реакция с раствором дифениламина в кислоте серной концентрированной. Дифениламин окисляется нитратами до дифенилдифенохинондиимина гидросульфата, окрашенного в синий цвет.
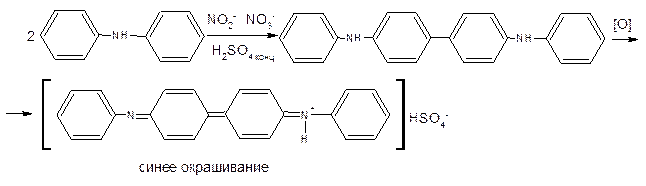
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 5944; Нарушение авторских прав?; Мы поможем в написании вашей работы!