
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Пример 6. Написать уравнения процессов, происходящих при электролизе раствора сульфата натрия с инертным анодом и разделенным катодным и анодным пространством
|
|
|
|
Пример 5
Написать уравнения процессов, происходящих при электролизе раствора сульфата натрия с инертным анодом и разделенным катодным и анодным пространством.
Решение. В растворе сульфата натрия будет происходить диссоциация согласно уравнению
Na2SO4 = Na+ + SO42–.
К отрицательному электроду (катоду) будут подходить ионы натрия и воды. Так как стандартный электродный потенциал системы
Na+ + 1 е – = Na0
значительно отрицательнее потенциала водородного электрода, то согласно правилам электролиза (табл. 9.6.1) на катоде будет происходить электрохимическое восстановление воды, а ионы натрия Na+, приходящие к катоду, будут накапливаться в прилегающей к нему части раствора.
На аноде (табл. 9.6.2) будет происходить электрохимическое окисление воды, приводящее к выделению кислорода, так как стандартный электродный потенциал реакции окисления воды ниже, чем стандартный потенциал окисления сульфат ионов. Ионы SO42–, движущиеся при электролизе к аноду, будут накапливаться в анодном пространстве.
Таким образом, будут протекать следующие реакции:
| Катод (–): | 2H2O + 2 e – → H2 + 2OH–, |
| Анод (+): | 2H2O – 4 e – → O2 + 4H+. |
Складывая катодные и анодные процессы и умножая левую и правую части катодного процесса на 2, получаем суммарное уравнение
6H2O → 2H2 + 4OH–+ O2 + 4H+.
Одновременно происходит накопление ионов Na+ в катодном пространстве и SO42–в анодном пространстве. Таким образом, одновременно с выделением водорода и кислорода образуется гидроксид натрия в катодном пространстве и серная кислота в анодном пространстве.
Ток силой 3 А проходит через раствор электролита СuSO4 за 30 мин. Определить массу выделившегося металла. Записать электродные процессы.
Решение. Согласно правилам электродных процессов при электролизе сульфата меди будут протекать следующие реакции:
| Катод (–): | Cu+2+ 2 e – → Cu0, |
| Анод (+): | 2H2O – 4 e – → O2 + 4H+. |
Закон Фарадея (9.6.2) для меди, выделяющейся на катоде, будет выглядеть следующим образом:
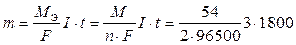 = 1,51 г.
= 1,51 г.
|
|
|
|
|
Дата добавления: 2014-11-06; Просмотров: 2420; Нарушение авторских прав?; Мы поможем в написании вашей работы!