
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Концентрационные гальванические элементы
|
|
|
|
Поскольку электродный потенциал металла зависит от концентрации ионов металлов в растворе, можно составить концентрационные гальванические элементы.
При этом пластина металла, погруженного в более разбавленный раствор соли, будет обладать более низким потенциалом и выполнять роль анода. Пластина, погруженная в более концентрированный раствор, выступает в роли катода.
Например: рассчитать ЭДС концентрационного гальванического элемента:
A(-) Ni / NiCl2 // NiCl2 / Ni K(+)
0,00001М 1М
Рассчитаем потенциал никелевой пластины, погруженной в 0,00001М раствор хлорида никеля по уравнению Нернста:
eNi/Ni2+ = e◦ + 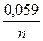 ∙ lg [ Ni2+ ] = - 0,25 +
∙ lg [ Ni2+ ] = - 0,25 +  ∙lg10-5 =
∙lg10-5 =
-0,25 +0,029∙(-5) = -0,25+(-0,145) = -0,395B = -0,39B
Потенциал никелевой пластины, погруженной в 1М раствор соли, равен стандартному электродному потенциалу никеля.
Следовательно: ЭДС = ек –еа = -0,85 – (-0,39) = 0,14В
Процессы, протекающие на электродах:
A(-) Ni – 2e  Ni2+
Ni2+
K(+) Ni2+ + 2e  Ni0
Ni0
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 387; Нарушение авторских прав?; Мы поможем в написании вашей работы!