
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Биологическая роль серы
|
|
|
|
Сера входит в состав важных аминокислот цистеина, глютатиона. Цистеин, является составной частью белковых молекул, содержит сульфгидрильную группу –SH. При окислении этой аминокислоты происходит отщепление водорода от сульфгидрильных групп двух молекул цистеина, а остатки соединяются, образуя молекулу цистина, содержащую дисульфидную связь S – S.Дисульфидные связи очень распространены и играют большую роль в поддержании определенной конфигурации белковых молекул. Переходы от сульфидных связей к дисульфидным обратимы и осуществляются в процессах переноса водорода в клетках. Кроме того дисульфидные и сульфидные группы способны блокировать свободные радикалы H+ и ОН-, возникающие из молекулы воды при радиационном воздействии на организм. Таким образом осуществляется химическая защита клеток от облучения. Чистая сера не ядовита. Прием внутрь небольших ее количеств, способствует рассасыванию нарывов и полезен, в частности, при геморрое. Очень мелко раздробленная сера входит в состав ряда мазей, предназначенных для ухода за кожей и лечением кожных заболеваний.
Медицинские применения гипосульфита довольно разнообразны. Его применяют внутрь при (или вводят внутривенно) при отравлении тяжелыми металлами, As, и цианидами, а также для дезинфекции кишечника. Наружное применение показано при тяжелых ожогах и воспалениях кожи, а также для лечения чесотки.
Na2SO4•10H2O - глауберова соль – обладает слабительным и мочегонным действием.
MgSO4•7H2O – горькая соль, как слабительное (15-30г), как обезболивающее и наркотическое средство при обезболивании родов, при гипертонии.
BaSO4 – сульфат бария – для рентгеноскопии.
СuSO4•5H2O – применяется как антисептическое и вяжущее средство в глазной практике. Иногда применяется внутрь как рвотное средство (10-30 мл 1% раствора).
ZnSO4•7H2O – как антисептическое и вяжущее средство при коньюктивитах, при хроническом катаральном ларингите.
KАl(SO4)2•12H2O – алюминиево-калиевые квасцы, применяются наружно в качестве вяжущего средства в водных растворах (0,5 – 1%) для полоскания, примочек при заболеваниях слизистых оболочек и кожи.
Тема: Р-Элементы VII группы
Ключевые слова: p-элементы, фтор, хлор, бром, иод, «галогены», двухатомные молекулы, типичные неметаллы, водородные связи, галиды,кислородные кислоты хлора, хлорная известь, хлораты, броматы, иодаты, химизм бактерицидного действия, хлорная вода, хлориды, фториды, бромиды, иодиды.
Характеристика элементов
| 9F | 1s22s22p5 |
| 17Cl | [Ne] 3s23p5 |
| 35Br | [Ar] 3d104s24p5 |
| 53I | [Kr] 4d105s25p5 |
| 85At | [Xe] 4f145d106s26p5 |
5 элементов главной подгруппы VII группы имеют общее групповое название «Галогены» (Hal), что означает «солерождающие». Одинаковое строение внешнего электронного слоя (ns2np5) обусловливает большое сходство элементов.
Сходство элементов
Ø Типичные неметаллы, р-элементы
Ø Большая величина энергии сродства к ē
Ø Высокие значения электроотрицательности (ЭО)
Ø Стремление к присоединению 1 ē до завершения октета Hal0 + 1ē = Hal-
Ø Устойчивость анионов Hal-
Ø Высокая окислительная активность
Ø Наиболее устойчивая степень окисления атомов в соединениях -1 (валентность I)
 Закономерное вертикальное изменение свойств элементов
Закономерное вертикальное изменение свойств элементов
F Заряд ядра ↑
Cl Число электронных слоев ↑
Br Радиус атома ↑
I Е сродства к ē ↓
At Электроотрицательность ↓
Неметалличность ↓
Простые вещества Hal2
 F2 (газ) Т. пл. и т. кип. ↑
F2 (газ) Т. пл. и т. кип. ↑
Cl2 (газ) Растворимость в воде ↓ (к F2 не относится)
Br2 (ж) Прочность связи в молекулах ↓
I2 (тв.) Неметаллические свойства ↓
Окислительная способность ↓
Химическая активность ↓
Валентные состояния атомов Cl, Br, I - ns2np5
nd
np 
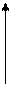









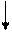
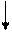
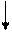
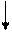










ns
При образовании ковалентных связей галогены чаще всего используют один неспаренный р-электрон, имеющийся в невозбужденном атоме, проявляя при этом В = 1.
Образуя связи с атомами более электроотрицательных элементов, атомы хлора, брома и йода могут переходить из основного валентного состояния в возбужденное, что сопровождается переходом электронов на вакантные орбитали d-подуровня. При этом число неспаренных электронов увеличивается, вследствие чего атомы Cl, Br, I могут образовывать большее число ковалентных связей:
| Возбужденные состояния | Число неспаренных ē | Валентность |
| ns2np4nd1 | III | |
| ns2np3nd2 | V | |
| ns1np3nd3 | VII |
Отличие F от других галогенов
В атоме фтора валентные электроны находятся на 2-м энергетическом уровне, имеющем только s- и р-подуровень. Это исключает возможность перехода атомов F в возбужденные состояния, поэтому фтор во всех соединениях проявляет постоянную валентность, равную I. Кроме того, фтор – самый электроотрицательный элемент, вследствие чего имеет постоянную с.о. -1.
Важнейшие соединения галогенов
- Галогеноводороды HHal
- Галогениды металлов (соли галогеноводородных кислот) – самые многочисленные и устойчивые соединения галогенов.
- Галогенорганические соединения.
- Кислородсодержащие вещества:
- неустойчивые оксиды, из которых достоверным можно считать существование 6 оксидов (Cl2O, ClO2, Cl2O7, Br2O, BrO2, I2O5).
- неустойчивые оксокислоты, из которых только 3 кислоты выделены как индивидуальные вещества (HClO4, HIO3, HIO4).
- соли оксокислот, главным образом хлориты, хлораты и перхлораты.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 1197; Нарушение авторских прав?; Мы поможем в написании вашей работы!