
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
УРОВЕНЬ А. 1. Составить схемы электролиза и написать уравнения электродных процессов водных растворов (анод инертный): а) хлорида меди (II)
|
|
|
|
1. Составить схемы электролиза и написать уравнения электродных процессов водных растворов (анод инертный): а) хлорида меди (II), б) гидроксида натрия.
Какие продукты выделяются на катоде и аноде?

| РЕШЕНИЕ а) CuCl2 = Cu2+ + 2Cl-, Схему электролиза составляем в соответствии с таблицами 11.1 и 11.2: K(-) A(+) инертный Cu2+ + 2ē = Cu 2Cl-- 2ē = Cl2 H2O H2O |
На катоде выделяется Cu, на аноде выделяется Cl2.
б) NaОН = Na+ + ОН-
K(-) A(+) инертный
Na+ 4ОН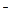 - 4ē = О2+ 2H2О
- 4ē = О2+ 2H2О
2H2O+2ē = H2+2OH-
На катоде выделяется Н2, на аноде выделяется О2.
2.Составить схемы электролиза и написать уравнения электродных процессов водного раствора сульфата никеля (II), если: а) анод инертный, б) анод никелевый. Какие продукты выделяются на катоде и аноде?

| РЕШЕНИЕ
а) анод – инертный
NiSO4 = Ni2+ + 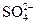 Схему электролиза составляем в соответствии с таблицами 11.1. и 11.2:
Схему электролиза составляем в соответствии с таблицами 11.1. и 11.2:
|
K(-) A(+) инертный
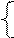 Ni2+ + 2ē = Ni
Ni2+ + 2ē = Ni 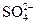
2H2O+2ē=H2+2OH- 2H2O-4ē=О2+4H+
На катоде выделяется Ni и H2, на аноде выделяется О2.
б) анод – никелевый:
NiSO4 = Ni2+ + 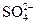
K(-) A(+) (Ni)
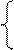 Ni2+ + 2ē = Ni
Ni2+ + 2ē = Ni 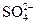 , Н2О
, Н2О
2H2O+2ē = H2+2OH- Ni - 2ē = Ni2+
На катоде выделяется Ni и H2, на аноде растворяется Ni.
3.При электролизе растворов а) нитрата кальция, б) нитрата серебра на аноде выделяется 560 мл газа (н.у.). Составить схему электролиза и написать уравнения электродных процессов. Определить какое вещество и в каком количестве выделилось на катоде? Анод инертный.
|

| РЕШЕНИЕ
а) Ca(NO3)2 = Ca2+ + 2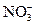 Схема электролиза:
K(-) A(+) инертный
Ca2+
Схема электролиза:
K(-) A(+) инертный
Ca2+ 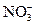 2H2O+2ē=H2+2OH- 2H2O - 4ē =
= О2+4H+
На катоде выделяется Н2, на аноде выделяется О2
По закону эквивалентов: nэк (В1)(анод) = nэк (В2)(катод)
2H2O+2ē=H2+2OH- 2H2O - 4ē =
= О2+4H+
На катоде выделяется Н2, на аноде выделяется О2
По закону эквивалентов: nэк (В1)(анод) = nэк (В2)(катод)
|
В соответствии со схемой электролиза:
nэк (О2)(анод) = nэк (Н2)(катод) или 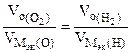 ,
,
откуда
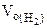 =
=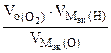 =
=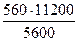 = 1120 см3,
= 1120 см3,
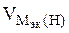 = 11200 см3/моль
= 11200 см3/моль
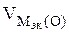 = 5600 см3/моль.
= 5600 см3/моль.
На катоде выделилось 1120 см3 водорода.
Ответ: 1120 см3 водорода.
б) AgNO3 = Ag+ + 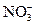
Схема электролиза:
K(-) A(+) инертный
Ag+ + ē = Ag 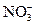
H2O 2H2O-4ē=О2+4H+
На катоде выделяется Ag, на аноде выделяется О2.
По закону эквивалентов: nэк(Ag)(катод) = nэк(О2)(анод) или  , откуда
, откуда 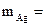
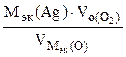 =
= 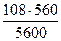 = 10,8 г.
= 10,8 г.
где 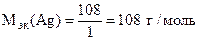
На катоде выделилось 10,8 г серебра.
Ответ: 10,8 г серебра.
|
|
|
|
|
Дата добавления: 2014-10-15; Просмотров: 3061; Нарушение авторских прав?; Мы поможем в написании вашей работы!
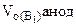 = 560 см3
Анод инертный
1. Схема электролиза-?
2.
= 560 см3
Анод инертный
1. Схема электролиза-?
2. 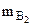 -?
3.
-?
3. 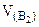 -?
4.
-?
4. 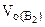 -?
-?