
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Галогены F, Cl, Br, I
|
|
|
|
СОЕДИНЕНИЯ S
СЕРА S
| В природе:FeS2 – железный колчедан (пирит), CuSO4·2H2O – гипс, Na2SO4·10H2O – глауберова соль; в органических веществах. | |
| Получение: 1) 2H2S+O2=2S+2H2O (нагрев) (способ Клауса) 2) 2SO2+4H2S=6S+4H2O (NH4)2S5=(NH4)2S+4S (нагрев) | Физические свойства: S – твердое хрупкое вещество желтого цвета, не растворимо в воде, плохо проводит тепло и электричество. Ткип. = 444,6˚С. Аллотропные модификации: α-сера, β-сера, сера моноклинная (S8), сера ромбическая (S8), сера пластическая (Sn). |
| Химические свойства серы | |
| S – окислитель(нагревание) S + 2Na = Na2S; S + H2 = H2S | S – восстановитель S + O2 = SO2 (голубое пламя) |
| Сероводород H2S |
| Физические свойства:H2S – бесцветный газ с запахом тухлых яиц, ядовит, поражает нервную систему. Химические свойства: H2S – восстановитель 1) 2H2S+O2=2S+2H2O (недост. О2); 2H2S+3O2=2SO2+2H2O (изб. О2); 2) H2S+I2=2HI+S (с галогенами); 3) H2S+FeCl3=2FeCl2+2HCl+S. Получение:1) H2+S=H2S; 2) FeS+2HCl=H2S+FeCl2. |
| Соли: Cульфиды– не растворимы в воде (кроме сульфидов щелочных и щелочноземельных металлов). Гидросульфиды – растворимы в воде (напр., NaHS). |
| Оксид серы (IV) |
| Физические свойства: SO2 – бесцветный газ с резким запахом. Химические свойства: SO2 – кислый оксид. 1) SO2+NaOH=NaHSO3 (SO2 изб.); SO2+2NaOH=Na2SO3+H2O (NaOH изб.) 2) SO2+2H2S=3S+2H2O 3) SO2+PbO2=PbSO4↓ 4) SO2+Br2+2H2O=H2SO4+2HBr Получение: 1)S + O2 = SO2 (нагревание) 2)Cu + 2H2SO4 = CuSO4 + SO2↑+ 2H2O (в лаборатории) |
| Сернистая кислота: SO2+H2O↔H2SO3 Соли: СульфитыH2SO3+2NaOH=Na2SO3+2H2O ГидросульфитыH2SO3+NaOH=NaHSO3+H2O (недост. щелочи) |
| Применение SO2 и H2SO3: красители; уничтожение микроорганизмов; при перевозке, хранении фруктов и ягод. Для получения серной кислоты. |
| Оксид серы (VI) SO3 |
| Физические свойства:бесцветная жидкость, t<17˚C –затвердевает. Химические свойства: SO3 – кислотный оксид H2O+ SO3=H2SO4 Получение:2SO2+O2=2SO3 (нагревание, кат.V2O5). |
| Серная кислота H2SO4 |
| Физические свойства: тяжелая бесцветная маслянистая жидкость, гигроскопична, нелетучая и не имеет запаха, не проводит электрический ток. Химические свойства: 1) обугливает углеводы 6H2SO4(конц.)+C6H12O6=6C+6H2SO4·H2O 2) с металлами (стоящими до водорода в ряду напряжения Me) H2SO4(разб.)+Zn=ZnSO4+H2↑ 2H2SO4(конц.)+ Zn = ZnSO4 + SО2 + 2H2O 3) с сухими солями NaNO3+4H2SO4= NaHSO4+HNO3 Применение: производство химических волокон, красителей, моющих, взрывчатых веществ, удобрений; рафинирование минеральных масел, травление металлов. |
| Соли серной кислоты: сульфатыH2SO4+NaOH = Na2SO4+2H2O гидросульфатыH2SO4 + NaOH = NaHSO4 + H2O (недостаток щелочи) |
| Качественная реакция на сульфат-ион |
| Реагент – соли бария, например BaCl2 H2SO4+ BaCl2=BaSO4↓+2HCl Na2SO4+ BaCl2=BaSO4↓+2NaCl BaSO4 – нерастворимый в воде и кислотах белый осадок. |
Элементы VII A группы
ХЛОР Cl2
Общая характеристика элементов
d
 p p
   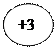 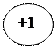 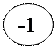 +ē s +ē s
 -nē степени -nē степени
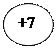 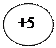  окисления окисления
F – трудносжимающийся газ Cl – легкосжимающийся газ Br – жидкость I – твердое вещество
| |||||||||||||||||||||||
| В природе:в водах океанов, морей и озер – соединения хлора. NaCl – хлорид натрия сильвинит; KCl – хлорид калия; MgCl2·6H2O – хлорид магния. | |||||||||||||||||||||||
| Получение: 1) В лаборатории: 4HCl+MnO2=Cl2+MnCl2+2H2O; 2) В промышленности: электролиз раствора NaCl(конц.), Cl2 выделяется на аноде. | |||||||||||||||||||||||
| Физические свойства:Cl2 – ядовитый газ желто-зеленного цвета с резким запахом, тяжелее воздуха в 2,5 раза. | |||||||||||||||||||||||
Химические свойства:  1)
1)
    с металлами Cu+Cl2=CuCl2; с металлами Cu+Cl2=CuCl2;2) 3) с водородом на свету (со взрывом) Cl2+H2=2HCl; 4) вытесняет бром и йод Cl2+2KBr=2KCl+Br2; 5) с водой Cl2+H2O↔HCl+HClO – хлорноватистая кислота. Применение: обезвоживание воды и др.; отбеливание тканей и бумаги; для получение HCl, хлорной извести. |
|
|
|
|
|
Дата добавления: 2014-10-31; Просмотров: 1079; Нарушение авторских прав?; Мы поможем в написании вашей работы!


 с неметаллами 2Р+3Cl2=2РCl3;
с неметаллами 2Р+3Cl2=2РCl3;