
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Растворы
|
|
|
|
6.1 Способы выражения концентрации растворов
Растворами, как известно, называют термодинамически устойчивые однородные системы, состоящие из двух и более компонентов (растворенных веществ и растворителя). Растворенные вещества – это компоненты раствора, которые меняют свое агрегатное состояние при его образовании. Растворитель – вещество, не изменяющее своего агрегатного состояния при образовании раствора.
Наиболее широкое распространение получили водные растворы (растворителем в которых является вода).
Количественной характеристикой, определяющей состав любого раствора, является концентрация. Концентрация выражает относительное содержание растворенного вещества в растворе. Различают процентную, нормальную, молярную и моляльную концентрации. Рассмотрим способы их выражения на конкретном примере.
Пример 1. В 2-х л воды растворено 40 г карбоната калия. Вычислите 1) процентную; 2) молярную; 3) нормальную; 4) моляльную концентрации полученного раствора, плотность которого равна 1,02 г/см3.
Решение.
Расчет процентной концентрации
Процентная концентрация определяет процент растворенного вещества в растворе, т.е. число граммов растворенного вещества, содержащихся в 100 г раствора, и выражается в %.
С % = 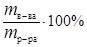 , (17)
, (17)
где m в-ва – масса растворенного вещества, г;
m р-ра – масса раствора, г.
Отношение w К 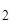 СО
СО 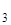 =
= 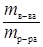 называется массовой долей. Поэтому С% = w ×100%.
называется массовой долей. Поэтому С% = w ×100%.
Рассчитаем массу раствора. Т.к. плотность воды близка к 1 г/см3, то принимаем массу воды равной m 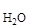 = 2000 мл × 1 г/мл = 2000г, тогда:
= 2000 мл × 1 г/мл = 2000г, тогда:
m р-ра = m 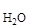 + m
+ m 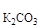 = 2000 + 40 = 2040 г.
= 2000 + 40 = 2040 г.
Процентная концентрация раствора составит:
С% = 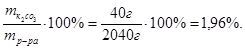
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 420; Нарушение авторских прав?; Мы поможем в написании вашей работы!