
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет нормальной концентрации 2 страница
|
|
|
|
ЗАДАЧИ
121-123. Вычислите константу диссоциации кислот по следующим данным и запишите уравнения диссоциации кислот по всем ступеням.
| № задачи | кислота | Концентрация, моль/л | a (для 1 ступени), % | Ответы |
| Н2СО3 | 0,006 | 0,85 | 4,3×10-7 | |
| Н3РО3 | 0,1 | 1×10-2 | ||
| Н2S | 0,1 | 0,07 | 5×10-8 |
124. Определите концентрацию ОН- - ионов в а) 1М; б) 0,02М растворе NН4ОН. К Д основания равно 1,8×10-5.
Ответ: а) 0,4×10-2 г-ион/л; б) 0,6×10-3г-ион/л.
125. Степень диссоциации уксусной кислоты СН3СООН в 1М растворе при 190С равна 0,004. Вычислите концентрацию ионов СН3СОО–, Н+ и общую концентрацию ионов в растворе.
Ответ: 0,004 моль/л; 0,008 моль/л.
126. Вычислите степень электролитической диссоциации 0,05 М раствора НIО3, если константа диссоциации кислоты равна 3×10-5.
Ответ: 2,45×10-2.
127. Вычислите концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты НСlО (КД= 5×10-8).
Ответ: 7×10-5моль/л
128. Определите рН и рОН раствора NaOH с концентрацией 0,1 моль/л.
Ответ: 13 и 1.
129. Ступенчатые константы диссоциации Н2S равны К1 = 6 × 10-8,
К2 =1×10-14. Вычислите константу полной диссоциации и концентрации ионов Н+, НS-, S2- в 0,1 М растворе сероводородной кислоты.
Ответ: 7,7×10-5моль/л, 1×10-14моль/л.
130-134. Вычислите произведение растворимости вещества (ПР) по данным о его растворимости в воде.
| № задачи | Вещество | Растворимость, моль/л | Ответы |
| ВаС2О4 | 4,03×10-4 | 1,62×10-7 | |
| Аg2СО3 | 1,15×10-4 | 6,15×10-12 | |
| ВаСО3 | 8,40×10-5 | 7,05×10-9 | |
| Аg2SО4 | 2,68×10-2 | 7,70×10-5 | |
| Вi(IО3)3 | 2,80×10-4 | 1,66×10-13 |
135-139. Выпадет ли осадок при сливании равных объемов растворов 1 и 2 с концентрацией С, моль/л? Напишите уравнения реакций.
| № задачи | Растворы | Осадки | ПР | |||
| С1 | С2 | |||||
| СаСl2 | 0,02 | Nа2SО4 | 0,02 | СаSО4 | 1,0×10-5 | |
| LаСl3 | 0,02 | NаОН | 0,03 | Lа(ОН)3 | 5×10-21 | |
| Sr(NО3)2 | 0,002 | К2SО4 | 0,002 | SrSO4 | 3,6×10-7 | |
| СuSO4 | 0,01 | (NН4)2S | 0,02 | СuS | 4×10-38 | |
| АgNO3 | 0,02 | Н2SO4 | Аg2SO4 | 2×10-5 |
140. Вычислите концентрацию [Н+] в растворах, в которых концентрация [ОН-] – ионов (в моль/л) составляет:
а) 10-4, б) 3,2×10-6, в) 7,4×10-11.
Ответы: а) 10-10моль/л, б) 3,12×10-9 моль/л, в) 1,35×10-4моль/л.
7 ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Окислительно-восстановительными реакциями называются реакции, в результате которых изменяются степени окисления элементов.
Степени окисления определяются числом электронов, передаваемых от атома с меньшей электроотрицательностью к атому с большей электроотрицательностью. Например, в молекуле NаСl менее электроотрицательным является атом натрия, более электроотрицательным – атом Сl, поэтому электроны смещаются в сторону атома хлора. Натрий приобретает степень окисления +1, а хлор -1.
Процесс присоединения электронов частицами (атомами, ионами, молекулами) называется их восстановлением, а вещество, содержащее такую частицу, является окислителем.
Процесс отдачи электронов – окисление, а вещество – восстановитель. Следует также учесть, что если атомы окислителя и восстановителя содержатся в одной и той же молекуле, то реакция называется реакцией внутримолекулярного окисления – восстановления. Например:
2КСlО3 = 2 КCl +3О2
Если же в таких реакциях окислителем и восстановителем являются атомы одного и того же элемента, то окислительно-восстановительный процесс называется диспропорционированием. Например, в реакции:
3К2МnО4 + 2Н2О = 2КМnО4 + МnО2¯ + 4КОН
Mn+6 диспропорционирует в Mn+7 и в Мn+4.
Имеют место и реакции обратного диспропорционирования, в которых атомы, находящиеся в различных степенях окисления, приобретают одинаковую окисленность (степень окисления), например:
NH4NO3 = N2О + 2H2O
где N-3, окисляясь, а N+5, восстанавливаясь, переходят в N+1.
Типичными окислителями являются: F2, О2, Сl2, перманганат-ион MnО 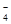 , дихромат-ион Cr2O
, дихромат-ион Cr2O  , диоксид свинца РbО2. Типичными восстановителями являются: активные металлы (К, Nа, Са), углерод (С), сульфид-ион(S-2), иодид-ион (I–), сульфит-ион (SO
, диоксид свинца РbО2. Типичными восстановителями являются: активные металлы (К, Nа, Са), углерод (С), сульфид-ион(S-2), иодид-ион (I–), сульфит-ион (SO 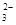 ), Fе2+, Sn2+ и др.
), Fе2+, Sn2+ и др.
В простых веществах О2, Cl2, Н2, N2 и др. оба атома имеют одинаковую электроотрицательность. При образовании из этих атомов молекул смещения электронов не происходит, поэтому степень окисления в простых веществах равна нулю. Некоторые простые вещества, например Fе, S, С и другие могут иметь разную степень окисления. Так, железо может иметь степень окисления +2 и +3, медь – +1 и +2, сера – +2, +4, +6. Кислород, как правило, имеет степень окисления –2, но в пероксидах его степень окисления равна (–1), во фторидах (+2). Постоянную степень окисления имеют щелочные металлы (+1), элементы II группы – (+2), алюминий – (+3), галоген-ионы – (-1).
В зависимости от того, к какому атому больше смещена электронная пара, говорят о положительной или отрицательной степени окисления. Степень окисления элемента, ближе к которому смещена электронная пара, является отрицательной, тогда как степень окисления другого атома в молекуле – положительна. Например, в молекуле воды электронная пара смещена в сторону атома кислорода. Следовательно, атом кислорода проявляет отрицательную степень окисления, а атомы водорода положительную.
В связи с тем что молекула в целом электронейтральна, то количество всех отрицательных единиц степени окисления должно быть равно количеству положительных единиц.
Положительная степень окисления, как правило, присуща тем элементам, которые на внешнем энергетическом уровне имеют 1, 2, 3 электрона, и, чтобы создать устойчивую 8-электронную оболочку, им легче отдать эти электроны, чем присоединить 7, 6, 5 электронов соответственно. Поэтому эти атомы будут отталкивать электроны.
Отрицательную по знаку степень окисления, как правило, будут иметь те элементы, у которых на внешнем энергетическом уровне 5, 6, 7 электронов, и для создания 8-электронного энергетического уровня им легче принять недостающие, чем отдать 5, 6, 7 электронов. Эти атомы будут притягивать электроны.
Знание знака и величины степени окисления атомов с постоянным значением позволяет вычислить степени окисления других атомов в сложных соединениях.
Пример 1. Определить степень окисления серы в серной кислоте Н2SO4.
Решение. Для определения степени окисления серы в серной кислоте вспомним, что атом кислорода имеет степень окисления (-2), а атом водорода (+1). В целом молекула любого вещества электронейтральна, следовательно, 2×(+1) + х + (-2)×4 = 0. Отсюда сера в серной кислоте имеет степень окисления +6.
Пример 2. Определить степень окисления марганца в перманганате калия КМnO4.
Решение. Степень окисления кислорода –2, калия +1. Молекула КМnO4 электронейтральна, следовательно: (+1)×1 + х + 4×(-2)=0.
Степень окисления марганца в перманганате калия равна +7.
Подбор коэффициентов в окислительно-восстановительных реакциях
При подборе коэффициентов в уравнениях окислительно-восстановительных реакций пользуются двумя методами: электронного баланса и ионно-электронного баланса. Остановимся на первом.
Для успешной расстановки коэффициентов в окислительно-восстановительных уравнениях важно соблюдать следующую последовательность:
1 Записать уравнение реакции, отметить элементы, изменяющие в результате реакции свои степени окисления, найти окислитель и восстановитель.
2 Составить схемы полуреакций окисления и восстановления с указанием исходных и образующихся частиц.
3 Уравнять число частиц каждого элемента в левой и правой частях полуреакций.
4 Уравнять суммарное число зарядов в левой и правой частях каждой полуреакции; для этого прибавить или отнять в левой части полуреакций необходимое число электронов.
5 Подобрать множители для полуреакций так, чтобы число электронов, отдаваемых при окислении, было равно числу электронов, принимаемых при восстановлении.
6 Сложить уравнения полуреакций с учетом найденных коэффициентов.
7 Расставить коэффициенты в уравнении реакции и проверить правильность расстановки. Число частиц каждого элемента в правой части уравнения должно быть равно числу частиц в левой части.
Рассмотрим применение метода электронного баланса в окислительно-восстановительных реакциях на нескольких примерах.
Пример 3.
К2 

Решение. Определим степень окисления всех элементов и установим, у каких из них она меняется. В молекуле К2Сr2O7 ионы кислорода имеют суммарный электрический заряд, равный (–2)×7 = -14. Молекула электронейтральна. Заряд двух ионов калия равен +2, а два иона хрома имеют заряд +12, следовательно, на долю одного иона хрома приходится +6 зарядов.
В правой части уравнения в молекуле Сr2(SO4)3 хром связан с кислотным остатком серной кислоты, имеющим заряд –2. Молекула электронейтральна, следовательно, два иона хрома должны быть связаны с тремя SО 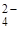 – ионами. Рассуждая таким же образом, приходим к выводу, что степень окисления серы в сульфите натрия Nа2SO3 равна +4, а в сульфате натрия Nа2SO4 +6.
– ионами. Рассуждая таким же образом, приходим к выводу, что степень окисления серы в сульфите натрия Nа2SO3 равна +4, а в сульфате натрия Nа2SO4 +6.
Составим электронные уравнения и приводим к балансу количество отданных и принятых электронов (окислителя и восстановителя). С учетом коэффициентов складываем ионы левых и правых частей полуреакций.


 2Сr+6 + 6ē ® 2Сr+3 2 1 восстановление, окислитель
2Сr+6 + 6ē ® 2Сr+3 2 1 восстановление, окислитель
S+4 - 2ē ® S+6 6 3 окисление, восстановитель
2Сr+6+ 3S+4®2Cr+3 +3S+6
Полученные коэффициенты переносим в молекулярное уравнение, причем коэффициент для хрома не удваиваем, чтобы сохранить его баланс в левой и правой частях уравнения.
Приводим к балансу ионы калия и натрия.
Подсчитываем количество кислотных остатков справа и вычитаем три кислотных остатка в составе Nа2SO3, участвующих в окислении. Разница в коэффициентах дает коэффициент для кислоты.
Уравниваем водород в составе молекулы воды.
Проверку правильности расстановки коэффициентов проводим по количеству атомов кислорода. В левой и правой частях уравнения оно равно 32.
Окончательное уравнение реакции: К2Сr  .
.
Пример 4. 
Решение. Определяем степень окисления всех элементов и устанавливаем, что они меняются у марганца и хлора.
Составляем электронные уравнения и приводим к балансу ионы окислителя и восстановителя. С учетом коэффициентов складываем ионы левой и правой частей уравнений: 



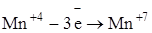 6 3 окисление, восстановитель
6 3 окисление, восстановитель
Сl+5 + 6ē ®Сl- 3 1 восстановление, окислитель
3Мn+4 + Cl+5 ® 3Мn+7 + Cl–
Коэффициенты краткого уравнения переносим в молекулярное уравнение, затем приводим к балансу коэффициенты других ионов.
Проверку правильности расстановки коэффициентов проводим по кислороду. В левой и правой части уравнения количество атомов кислорода равно 15.
3 МnO2 + КСlO3 + 6КОН ® 3К2МnO4 + КСl + 3Н2О
ЗАДАЧИ
Расставьте коэффициенты в уравнениях окислительно-восстановительных реакций. Укажите окислитель и восстановитель.
141. МnSO4 + КМnO4 + Н2О ® МnO2 + К2SO4 + Н2SO4
142. FеSO4 + КClO3 + Н2SO4 ® Fе2(SO4)3 + КСl + Н2О
143. КIО3 + КI + Н2SO4 ® I2 + К2SO4 + Н2О
144. I2 + Сl2 + Н2О ® НIО3 + НСl
145. NаСrO2 + Вr2 + NаОН ® Nа2СrO4 + NаВr + Н2О
146. Р + НClO3 + Н2О ® Н3РО4 + НСl
147. РbS + НNO3 ® S + Рb(NO3)2 + NO + Н2О
148. КВr + РbО2 + НNO3 ® Рb(NO3)2 + Вr2 + КNO3 +Н2О
149. Sb2O3 + НВrO3 ® Sb2O5 + НВr
150. Сr2O3 + КNО3 + КОН ® К2СrO4 + КNO2 + Н2О
151. Н2S + Cl2 + Н2О ® Н2SO4 + НСl
152. Nа2МnO4 + NаNO2 + Н2О ® МnO2 + NаNO3 + NаОН
153. КМnО4 + НСl ® МnСl2 + КCl + Сl2 + Н2O
154. Н2SO3 + К2Сr2О7 + Н2SO4 ® Cr2 (SO4)3 + К2SO4 + Н2О
155. FеSO4 + КМnO4 + Н2SO4 ® Fе2(SO4)3 + МnSO4 + Н2О + К2SO4
156. NаBr + MnO2 + Н2SO4 ® МnSO4 + Nа2SO4 + Br2 + Н2О
157. Мg + Н2SO4 ® МgSO4+ S+ Н2О
158. Н2SO3 + Cl2 + Н2О ® Н2SO4 + НСl
159. Н2S + НNO3 ® S + NO2 + Н2О
160. КNО3 + КI + Н2SO4 ® NO + I2 + К2SO4+ Н2О
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 718; Нарушение авторских прав?; Мы поможем в написании вашей работы!