
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Общая характеристика органических соединений
|
|
|
|
V Элементы органической химии
Органическая химия изучает соединения углерода. Как правило, элементарный углерод, оксид углерода (II), оксид углерода (IV), карбонаты относят к неорганическим соединениям. Но такое разделение является искусственным и бесполезным, так как химия «органических» и «неорганических» соединений основывается на одних и тех же подходах. В настоящее время многочисленные междисциплинарные исследования показали, что разграничение органической и неорганической химии, биохимии и биологии нельзя считать строго определённым, и все эти дисциплины неразрывно связаны между собой. Их нельзя рассматривать по отдельности; настоящий прогресс в науке невозможен без обмена знаниями и достижениями между исследователями различных областей науки.
Углеводороды состоят только из атомов углерода и водорода. Органические соединения – это углеводороды и их многочисленные производные, в состав которых могут входить многие элементы периодической системы. Органические соединения обладают рядом характерных особенностей, которые отличают их от неорганических соединений: большинство из них горючи и не диссоциируют на ионы, что обусловлено природой ковалентной связи – основного вида химической связи в органических веществах.
Для органических соединений характерно явление изомерии. Оно заключается в том, что вещества, обладающие одинаковым составом и молекулярной массой, имеют разное строение, а, значит, и различные физические и химические свойства. К таким соединениям, называемым изомерами, относятся, например, этиловый спирт
СН3 – СН2 –ОН и диэтиловый эфир СН3 – О – СН3.
Классификация органических соединений
Все органические соединения в зависимости от строения углеродной цепи (углеродного скелета) классифицируют следующим образом:
I. Ациклические соединения -соединения с открытой (незамкнутой) цепью углеродных атомов (прямой или разветвлённой):
- С – С – С – С – С – С - - С – С – С – С – С -
│
С
Такие соединения называют также алифатическими соединениями или соединениями жирного ряда. Они бывают предельными, или насыщенными (парафины, или алканы), и непредельными, или ненасыщенными, соединениями ряда этилена (олефины, или алкены) и ацетилена (алкины).
II. Циклические соединения – соединения, в которых углеродные атомы образуют циклы, делятся на:
1. Карбоциклические (изоциклические) – циклические соединения, образованные только атомами углерода. Они подразделяются на алициклические (нафтены) и ароматические соединения. Алициклические соединения бывают насыщенными (циклоалканы, или циклопарафины) и ненасыщенные (циклоалкены, или циклоолефины).
2. Гетероциклические соединения – циклы, в состав которых кроме атомов углерода входят другие атомы – гетероатомы (O, S, N и др.).
При замещении одного или нескольких атомов водорода в углеводородах на другие атомы или группы атомов (функциональные группы) образуются различные производные углеводородов – классы органических соединений (табл.1). Функциональная группа – группа атомов в молекуле, вступающая в характерные химические реакции.
Таблица 1
Классы органических соединений
| Классы органических соединений | Функциональная группа, определяющая класс органических соединений |
| Галогенопроизводные Спирты, фенолы Альдегиды Кетоны Простые эфиры Сложные эфиры Карбоновые кислоты Тиоспирты Тиоэфиры Сульфокислоты Амины Имины Амиды Нитрилы Нитросоединения Нитрозосоединения Гидразины Гидразосоединения Азо- и диазосоединения | - Hal (Cl, Br, F, I) - OH - CHO >C=O - O – R - COOR - COOH - SH - SR - SO3H - NH2 = NH -CONH2 - C≡N - NO2 - NO - NH – NH2 - NH – NH – - N=N-; - N+≡N |
Классификация органических реакций
Органические реакции, подобно неорганическим, можно классифицировать по их результатам на три основных типа реакций:
реакции замещения (символ S от англ. substitution – замещение):
RH + Cl2 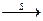 RCl + HCl
RCl + HCl
реакции присоединения (символ A от англ. addition – присоединение):
CH2=CH2 + HCl 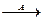 CH3CH2Cl
CH3CH2Cl
HC≡CH + 2Br2 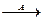 Br2CHCHBr2
Br2CHCHBr2
реакции отщепления (символ Е от англ. elimination – отщепление):
CH3CH2OH 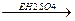 CH2=CH2 + H2O
CH2=CH2 + H2O
Кроме того, органические реакции классифицируют по их механизмам, т.е. по способу разрыва ковалентных связей в реагирующих соединениях и образования новых химических связей в процессе реакции. Различают два способа разрыва связей между атомом углерода (С) и уходящей группой Х (Х – функциональная группа, атом Н или С):
- >C: X:
1) гомолитический разрыв (его называют также радикальным) -> C∙ ¦ ∙X ковалентной связи заключается в том, что связующая электронная пара разъединяется, при этом каждый из образующихся осколков (свободных радикалов) получает один неспаренный электрон;
2) гетеролитический разрыв (называемый также ионным)
а) -> C ¦:X; б) -> C: ¦ X приводит к переходу связующей пары электронов к одному из осколков. В результате данного разрыва возникают заряженные частицы.
Реакции с гомолитическим характером разрыва связей называются гомолитическими или радикальными (например, SR – радикальное замещение; АR – радикальное присоединение).
Гетеролитические реакции с разрывом связей типа «а» являются нуклеофильными («любящие ядро») по отношению к атому углерода с полным или частичным положительным зарядом. Символ SN означает нуклеофильное замещение.
Гетеролитические реакции с разрывом связей у атома углерода типа «б» называются электрофильными. Например, АЕ – электрофильное присоединение.
|
|
|
|
|
Дата добавления: 2014-11-25; Просмотров: 4274; Нарушение авторских прав?; Мы поможем в написании вашей работы!