
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Константа рівноваги
Хімічна рівновага.
Стан хімічної рівноваги є характерним для оборотних реакцій, тобто реакцій, які відбуваються як у прямому, так і оберненому напрямку. Межею протікання таких реакції є досягнення моменту динамічної рівноваги, коли швидкості прямої й оберненої реакцій стають рівними.
Для оборотної гомогенної реакції загального виду:

mA + nB Û pC +qD
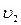
швидкість прямої реакції відповідно до ЗДМ (1):
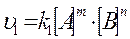 , а оберненої
, а оберненої 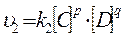 . В момент рівноваги:
. В момент рівноваги:
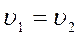 і
і 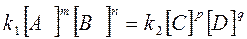
Звідси 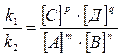 .
.
Замінимо відношення двох сталих величин k1/k2 сталою K і одержимо:
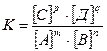 . (3)
. (3)
де [А], [В], [С], [D] - рівноважні концентрації реагуючих речовин, моль/л;
m, n, p, q- стехіометричні коефіцієнти в рівнянні реакції.
Величина K називається константою хімічної рівноваги. Вона залежить від температури і природи реагуючих речовин але не залежить від їхніх концентрацій. Отже, в оборотних реакціях рівновага встановлюється, коли відношення добутку концентрацій продуктів реакції та добутку концентрації вихідних речовин у відповідних ступенях стає рівним деякий сталій величині.
Для гомогенної оборотної реакції: H2(г) + I2(г) = 2 НІ(г)
константа рівноваги  .
.
У випадку гетерогенних реакцій концентрації твердих речовин не входять у вираз константи рівноваги. Так, для реакції:
3 Fe(T) + 4 H2O(П) = Fe3O4(T) + 4H2(Г)
константа рівноваги 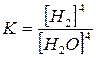 .
.
|
|
Дата добавления: 2014-11-16; Просмотров: 1312; Нарушение авторских прав?; Мы поможем в написании вашей работы!