
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Следовательно,. Изменение энергии Гельмгольца в процессе изотермического расширения
|
|
|
|
Изменение энергии Гельмгольца в процессе изотермического расширения
Тогда изменение энергии Гиббса составит
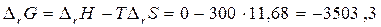 Дж.
Дж.
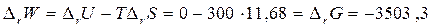 Дж.
Дж.
Пример 4. Для газофазной реакции А2 + В2 → 2АВ при некоторой температуре Т константа равновесия равна 100. Определите, будет ли в этой системе происходить образование газа АВ при следующих начальных концентрациях газов:
| № | С(А2),моль∙л-1 | С(В2),моль∙л-1 | С(АВ),моль∙л-1 |
| 1,5 | 0,5 | 2,0 | |
| 1,0 | 1,0 | 10,0 | |
| 0,5 | 1,0 | 10,0 |
Решение. Для трёх случаев рассчитаем 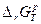 , используя уравнение изотермы химической реакции. Так как для данной реакции ∆n = 0, то
, используя уравнение изотермы химической реакции. Так как для данной реакции ∆n = 0, то
 .
.
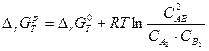 , где
, где 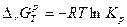 .
.
Для рассматриваемой реакции KP = KC.
1) 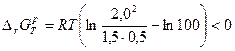 − идёт образование продукта реакции;
− идёт образование продукта реакции;
2)  − система находится в равновесии, следовательно, образование продукта не происходит;
− система находится в равновесии, следовательно, образование продукта не происходит;
3) 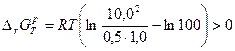 − образования продукта не происходит.
− образования продукта не происходит.
Пример 5. Рассчитайте стандартную свободную энергию Гиббса и константу реакции при температуре Т = 1200 К
СО(г) + Н2О(г) →СО2(г) + Н2(г),
используя справочные данные по энтальпиям образования и энтропиям участников реакции, а также температурную зависимости Ср участников реакции:
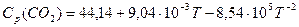 , Дж∙моль-1∙К-1;
, Дж∙моль-1∙К-1;
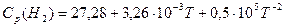 , Дж∙моль-1∙К-1;
, Дж∙моль-1∙К-1;
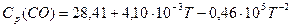 , Дж∙моль-1∙К-1;
, Дж∙моль-1∙К-1;
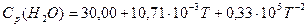 , Дж∙моль-1∙К-1.
, Дж∙моль-1∙К-1.
Будет ли данная реакция самопроизвольной при данных условиях?
Решение. Воспользуемся данными из приложения (Т = 298 К):
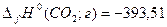 кДж∙моль-1;
кДж∙моль-1;
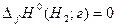 кДж∙моль-1;
кДж∙моль-1;
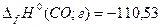 кДж∙моль-1;
кДж∙моль-1;
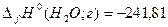 кДж∙моль-1;
кДж∙моль-1;
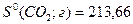 Дж∙моль-1∙К-1;
Дж∙моль-1∙К-1;
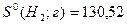 Дж∙моль-1∙К-1;
Дж∙моль-1∙К-1;
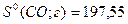 Дж∙моль-1∙К-1;
Дж∙моль-1∙К-1;
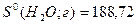 Дж∙моль-1∙К-1.
Дж∙моль-1∙К-1.
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 774; Нарушение авторских прав?; Мы поможем в написании вашей работы!