
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Повышение температуры кипения раствора определим по формуле
|
|
|
|
Отсюда
Сумма мольных долей компонентов раствора равна 1.
Следовательно, моляльность раствора
Отсюда
Г воды содержит 80 г соли;
Отсюда
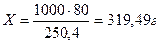
Молекулярная масса NaBr равна 102,89 г∙моль-1. Следовательно, молярность раствора
 .
.
в) в 230 г воды содержится 80 г NaBr. Из пропорции находим массу соли в 1000 г воды:
1000 г воды содержит у г соли.
 .
.
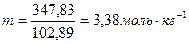 .
.
г) Мольная доля соли в растворе
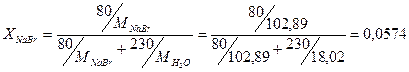 .
.
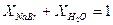
 .
.
Пример 3. В 1 кг воды растворено 15,6 г мочевины. Определите осмотическое давление раствора при 20оС, если плотность раствора при этой температуре равна 1,01 г·см−3. Рассчитайте температуру кипения и температуру кристаллизации раствора, а также давление насыщенного пара над раствором, если давление насыщенного пара над чистой водой при 20оС составляет 17,54 мм рт. ст. Укажите выбранные Вами приближения для расчётов перечисленных величин.
Решение. Молярная масса мочевины CO(NH2)2 M2 = 60 г·моль−1. Приближения для расчётов - модель идеального бесконечно разбавленного раствора. Осмотическое давление такого раствора можно определить по формуле
π = с2RT,
где с2 - молярная концентрация: 
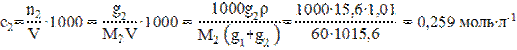
где g1 и g2 – массы растворителя и растворённого вещества в г,
V – объём раствора в см3.
π = 0,259∙0,082∙293 = 6,23 атм.
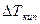 = Еm2,
= Еm2,
где Е – эбулиоскопическая постоянная воды,
m2 – моляльная концентрация:
 моль∙кг-1.
моль∙кг-1.
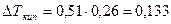 К
К
 оС
оС
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 933; Нарушение авторских прав?; Мы поможем в написании вашей работы!