
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
После подстановки численных значений
|
|
|
|
После подстановке численных значений находим
Отсюда, энергия активации
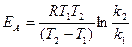
В нашем случае: k1 = 6,72 л∙моль-1∙мин-1; Т1 = 986 К
k2 = 977,0 л∙моль-1∙мин-1; Т2 = 1165 К

При известной энергии активации константу скорости k3 при температуре Т3 = 1053 К рассчитываем по уравнению:

или 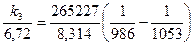
Отсюда k3 = 52,83 л∙моль-1∙мин-1.
Кинетическое уравнение реакции 2-го порядка имеет вид:
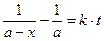 ,
,
где а – начальная концентрация N2O, равная 2 моль∙л-1;
х – уменьшение концентрации N2O к моменту времени t.
 .
.
Отсюда х = 1,998 моль∙л-1.
Отношение х / а даёт степень разложения вещества. Очевидно
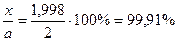 ,
,
т.е. при этих условиях N2O практически полностью разлагается.
 |
Пример 10. Для обратимой реакции первого порядка
Кравн = 8, а k1 = 0,4 с-1. Вычислите время, при котором концентрации веществ А и В станут равными, если начальная концентрация вещества В равна 0.
Решение. Из константы равновесия находим константу скорости обратной реакции:

Для того, чтобы найти время, за которое прореагирует ровно половина вещества А, надо подставить значение  в решение кинетического уравнения для обратимых реакций:
в решение кинетического уравнения для обратимых реакций:

Отсюда получим:

Примеры решения задач к разделу «Коллоидная химия»
Пример 1. Найти средний сдвиг 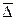 при броуновском движении шарообразных частиц табачного дыма радиусом r = 10-6 м при температуре 293 К за время 10 с. Вязкость воздуха
при броуновском движении шарообразных частиц табачного дыма радиусом r = 10-6 м при температуре 293 К за время 10 с. Вязкость воздуха 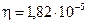 Па с.
Па с.
Решение. По уравнению Стокса – Энштейна находим коэффициент диффузии
 .
.
По уравнению Эйнштейна – Смолуховского определяем средний сдвиг частиц
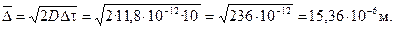
Пример 2. Найти скорость оседания космических частиц радиусом 4 10-5 м на поверхности Луны. Ускорение свободного падения на Луне g л = 1.608 м∙c-2; вязкость среды 10-7 Па с, плотность вещества частиц 3000 кг∙м-3.
Решение. Скорость оседания частиц находим по уравнению

Пример 3. На какой высоте h2 по сравнению с уровнем h1 число частиц в золе золота при температуре 27◦С уменьшается в два раза, если диаметр частиц составляет 2 нм, а плотность золота 19300 кг∙м-3, плотность гидрозоля принять за 1000 кг∙м-3?
Решение. Запишем уравнение, которое описывается гипсометрическим законом Лапласа-Перрена:
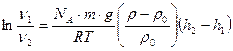
|
|
|
|
|
Дата добавления: 2014-11-16; Просмотров: 1218; Нарушение авторских прав?; Мы поможем в написании вашей работы!