
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Равновесия в растворах комплексных соединений
|
|
|
|
Комплексные соединения диссоциируют в растворах как сильные электролиты на внешнюю и внутреннюю сферы (комплексы): [Сu(NН3)4]SО4 ® [Сu(NН3)4]2+ + SО42-
Комплексы (комплексные ионы) диссоциируют как слабые электролиты.
Диссоциация - многоступенчатая:
[Cu(NH3)4]2+ Û [Cu(NH3)3]2+ + NH3 К 1
[Cu(NH3)3]2+ Û [Cu(NH3)2]2++ NH3 К 2
[Cu(NH3)2]2+ Û [Cu(NH3)]2+ + NH3 К3
[Cu(NH3)]2+ Û Cu2+ + NH3 К 4
_________________________________________
[Cu(NH3)4]2+ Û Cu2+ + 4 NH3 К Н
Константа суммарной реакции К Н - константа нестойкости равна произведению констант диссоциации по отдельным ступеням К Н = К 1 К 2 К 3 К 4.
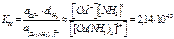 ( при 298К)
( при 298К)
В растворах прочных комплексов концентрация ионов комплексообразователя мала.
В общем виде для диссоциации комплекса [МХ n ] z Û М n + + y X m
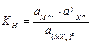 табличная величина
табличная величина
где z - заряд комплекса;
n + - заряд комплексообразователя;
m - заряд лиганда,
y – координационное число
Константа обратного процесса, т. е. процесса образования комплекса, называется константой устойчивости К У = 1/ К Н.
Чем ниже константа нестойкости комплекса и чем выше константа устойчивости, тем прочнее комплекс.
Константы нестойкости К Н и устойчивости К У зависят от природы лигандов и комплексообразователя, а также от значения координационного числа.
Основные учебники и учебные пособия
1. Н.В.Коровин. Общая химия
2. Н.В.Коровин и др. Лабораторные работы по химии
3. Задачи и упражнения по общей химии. Под ред. Н.В.Коровина
4. Общая химия. Теория и расчеты. Под ред. Н.В. Коровина
|
|
|
|
|
Дата добавления: 2014-11-18; Просмотров: 450; Нарушение авторских прав?; Мы поможем в написании вашей работы!