
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Зависимость скорости химической реакции от температуры
Скорость химической реакции при данной температуре пропорциональна произведению концентраций реагирующих веществ в степени, равной стехиометрическому коэффициенту, стоящему перед формулой данного вещества в уравнении реакции.
Зависимость скорости химической реакции от природы реагирующих веществ.
Говорить о скорости химической реакции имеет смысл, если природа реагирующих веществ позволяет им вступать в химическое взаимодействие. Например, природа реагирующих веществ позволяет протекать первой и второй реакции, но не позволяет третьей.
1. Mg + O2 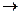 2MgО
2MgО
2. Zn + 2HCl 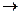 ZnCl2 + H2↑
ZnCl2 + H2↑
3. NaOH + KOH ≠ 
2. Зависимость скорости химической реакции от концентрации реагирующих веществ определяется законом действия масс, который был установлен в 1867г опытным путем Гульдбергом и Вааге.
Закон действия масс справедлив только для наиболее простых по своему механизму реакций взаимодействия, протекающих в газах или в разбавленных растворах.
Для гомогенных реакций:
1.aA(Ж) + bB(Ж) ↔ cC(Ж) + dD(Ж) ;  (T=const)
(T=const)
2. 3H2(Г) + N2(Г) ↔ 2NH3(Г); 
Для гетерогенных реакций:
1. aA(т) + bB(Г) = cC(Г) + dD(Г); 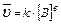 2. С (т)+О2(Г)=СО2(Г);
2. С (т)+О2(Г)=СО2(Г); 
В законе действия масс не учитываются концентрации веществ, находящихся в твердой фазе. Чем больше площадь поверхности твердой фазы, тем выше скорость химической реакции.
k – константа скорости химической реакции определяется природой реагирующих веществ и зависит от температуры, от присутствия в системе катализатора, но не зависит от концентрации реагирующих веществ. Константа скорости представляет собой скорость химической реакции (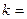
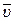 ), если концентрации реагирующих веществ
), если концентрации реагирующих веществ  .
.
3. Зависимость скорости химической реакции от давления. Для газообразных систем увеличение давления или уменьшение объема, равноценно увеличению концентрации и наоборот.
Задача: Как изменится скорость химической реакции 2SO2(г) + O2(г) 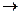 2SO3(г), если давление в системе увеличить в 4 раза?
2SO3(г), если давление в системе увеличить в 4 раза?
В соответствие с законом действия масс для прямой реакции, записываем выражение:
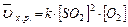 , пусть [SO2]=a моль/л, [O2]=b моль/л, тогда по закону действия масс
, пусть [SO2]=a моль/л, [O2]=b моль/л, тогда по закону действия масс 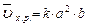
Уменьшение объема в 4 раза соответствует увеличению концентрации в системе в 4 раза, тогда
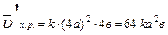 ;
;
 .
.
Влияние температуры на скорость химической реакции приближенно определяется правилом Вант-Гоффа. При повышении температуры на 100С скорость химической реакции возрастает в 2-4раза.
Математическая запись правила Вант-Гоффа: 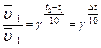 γ - температурный коэффициент скорости реакции или коэффициент Вант-Гоффа для большинства реакций лежит в пределах 2-4.
γ - температурный коэффициент скорости реакции или коэффициент Вант-Гоффа для большинства реакций лежит в пределах 2-4.
Задача. Во сколько раз изменится скорость химической реакции, протекающей в газовой фазе, если температура изменилась от 80 0С до 120 0С (γ = 3)?
В соответствии с правилом Вант-Гоффа записываем:
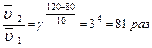
Увеличение скорости химической реакции при повышении температуры объясняется не только увеличением кинетической энергии взаимодействующих молекул. Например, число столкновений молекул растет пропорционально корню квадратному из абсолютной температуры  . При нагревании веществ от нуля до ста градусов по Цельсию, скорость движения молекул возрастает в 1,2 раза
. При нагревании веществ от нуля до ста градусов по Цельсию, скорость движения молекул возрастает в 1,2 раза 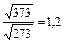 , а скорость химической реакции возрастает примерно в 59 тысяч раз. Такое резкое увеличение скорости реакции с ростом температуры объясняется долей активных молекул, столкновения которых приводит к химическому взаимодействию. Согласно теории активных столкновений в реакцию вступают только активные молекулы, энергия которых превышает среднюю энергию молекул данного вещества, т.е. молекулы, обладающие энергией активации.
, а скорость химической реакции возрастает примерно в 59 тысяч раз. Такое резкое увеличение скорости реакции с ростом температуры объясняется долей активных молекул, столкновения которых приводит к химическому взаимодействию. Согласно теории активных столкновений в реакцию вступают только активные молекулы, энергия которых превышает среднюю энергию молекул данного вещества, т.е. молекулы, обладающие энергией активации.
Энергия активации (EА) – это тот избыток энергии по сравнению со средним запасом, которым должны обладать молекулы для осуществления химической реакции. Если ЕА< 40 кДж/моль – реакции протекают быстро, если ЕА > 120 кДж/моль – реакции не идут, если ЕА = 40-120 кДж/моль – реакции протекают в обычных условиях. Повышение температуры снижает энергию активации, делает вещества более реакционно-способными, скорость взаимодействия при этом увеличивается.
Более точную зависимость скорости химической реакции от температуры установил C.Аррениус: константа скорости реакции пропорциональна основанию натурального логарифма, возведенного в степень (–ЕА/RT).  ,
,
А – предэкспоненциальный множитель, определяет число активных
соударений;
е – экспонента (основание натурального логарифма).
Логарифмируя выражение  , получим уравнение:
, получим уравнение:
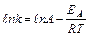 . Уравнение Аррениуса показывает, что скорость реакции тем выше, чем меньше энергия активации. Для снижения энергии активации используют катализаторы.
. Уравнение Аррениуса показывает, что скорость реакции тем выше, чем меньше энергия активации. Для снижения энергии активации используют катализаторы.
|
|
Дата добавления: 2014-11-29; Просмотров: 782; Нарушение авторских прав?; Мы поможем в написании вашей работы!