
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
ЛЕКЦИЯ. Реакторлар 8 страница
|
|
|
|
Кесте 5.8. Калий тыңайтқыштар ассортименті
| Тыңайтқыштар | Құрамы, | ГОСТ, ТУ | ||
| KCI | K2O | ылғал | ||
| Калий хлориді 1-сорт II-сорт | 95±1 91±1 | 60±0,6 57,5±0,6 | ГОСТ 4568-74 | |
| Ірі кристалды калий хлориді | 53,7±0,6 | ТУ 6-12-16-71 | ||
| Аралас калий тұзы (40%) | 63,3 | ТУ 6-12-16-71 | ||
| Калийхлорэлектролит марка А марка Б | 72,0 50,0 | 45,5 31,6 | ТУ 48-10-40-71 | |
| Калий сульфаты (ауыл шаруа) | - | 46±1 | ТУ 6-12-14-74 | |
| Калий сульфаты (техн.) | - | ТУ 48-5-30-72 | ||
| Калий сульфаты тыңайтқыш 1 сорт ІІ-сорт | - - | 50,0 46,0 | 0,3 0,3 | ТУ 6-12-45-73 |
| Калий магнезия (9±1%MgO) | - | 29±0,5 | ТУ 6-12-23-70 | |
| Каинит табиғи | - | 10±0,5 | ТУ 6-12-23-70 |
Минералды тыңайтқыш өндірісі дамуының
қысқаша тарихи очеркі.
Минералды тыңайтқыштарды қолдану жерді пайдаланудың ғылыми негізінде базаланады. Ж.Б. Буссенго, Ю. Либих, А.Н. Энгельгарт, Д.М. Менделеев, В.В. Докучаев, Д.Н. Прянишников және т.б. ғылымдар оның негізгі қалаған.
Ю. Либих 1840 жылы өсімдіктің минералды қоректену теориясын жасады, тұқымның ұрықтану негізіне және тұқымның тандалу негізіне ғылыми дәлел берді, өсімдіктің калийді, фосфорлы, күкіртті және басқа элементтерді тұтынуын дәлелдеді. Ол калийлі және еритін минералды тыңайтқышты табиғи фосфатты күкірт қышқылымен ыдырату арқылы алады.
Д.Н. Прянишников 1916 жылы өсімдіктің азотты қоректенуінің теориясын құрды, және фосфорлату, әктену және гипстену процесіне теориялық негізін қалады.
МТ-тың өнеркәсіптік негізі 30-шы жылдары орнатылды, осы уақытқа дейін калийлі және фосфорлы шикізаттардың негізінде және синтетикалық аммиактың өндірін ұйымдастыру негізінде. Осыған дейін азотты және калийлі МТ өндірілмеді десекте болады. Аммоний сульфатының өндірісінің кокс химиялық өндіріс аммиагының базасында 13000 тоннадан көтерілмеді, импортты фосфоритпен суперфосфат 65000 тонн. Барлығы 1913 ж. 17000 тонна минералды тыңайтқыштар алынды, сол уақытта тұтыну мөлшері 42500 тоннаны құрады.
|
|
|
Азотты тыңайтқыштар. Бобрикте, Горловкада, Березнякта аммоний нитратының өндірісі бойынша алғашқы жабдық күрделі және өнімділігі өте төмен болды. Онда аммиак нейтрализациясының жылуы қолданылмады, салқындататын суды көп қажет етті. Аммоний нитратының өндірісі 1737 жылы барлығы 270 мың тонна құрады.
1935-36 жылдары МТН аппаратымен аммоний нитратының өндірісі бойынша жабдықтың өнімділігіне енгізілді, Кемеровта, Днепродзержинскіде, Чирчикта. Жүйе бойынша бұл сызба іске асырылды және аммоний нитратының шығарылуы жер өнімінің қажеттілігін қамтамасыз етті, ал соғыс жылдарында- қорғаныс қажеттіліктері.
Соңғы жылдары аммоний нитратының өндірісі бойынша цехтар Кировоканде, Лисичанда, Руставиде іске қосылды. Жүйелі түрде қоспа іздеу бағытында жұмыстар жүргізілді, аппаратуралар іске қосылды. 1970-1972 жылдары 225 мың тонна өнімділікпен агрегат қатары Череповецте, Черкассте, Навоиде, 60-70%-дық азот қышқылын қолдана отырып енгізуі, және бір сатыға жүрді. 1972 жылдан бастап аммоний нитраты Ресей Федерациясында тек қана АС-67, АС-72 және АС-72 М агрегаттарында өндірілді, шынында 450 мың тонна біріңғай өнімділікпен бөлшектерімен және аппаратураны орналастыруымен ерекшеленеді. Нәтежесінде аммоний нитратының өндірісі бойынша қызмет жасайтын цехтардың саны елімізде 1940 жылы 6-дан 1980 жылы 31-ге дейін өсті.
|
|
|
Өнеркәсіптік масштабтарда карбамид өндірісі 20-30 жылдары Рессей Федерациясында басталды. Синтез процесінде фундаменталдық зерттелуі 30-шы жылдардың басында жүргізілді, 1935 жылы модельді жабдық орнатуға мүмкіндік берді және 1939 жылы тәулігіне 1т. өнімділікпен жартылай өнеркәсіптік цех ашылды. 1958 жылы Сталиногорлық және Лисичандық комбинаттарда ашық рециклімен карбамид өндіру бойынша цехтар іске қосылды. 70 және 105 мың тонна өнімділікпен жартылай рецикл сызба бойынша алғашқы цехтар 1961-1964 жылдары пайдалануға жіберілді. 1963-1965 жылдары Северодонецте және Чирчикта, Щекинода, жылына 190 мың тонна өнімділік пен толық сұйық рециклді сызба бойынша карбамид өндірісінің алғашқы цех қатары ашылды.
Фосфорлы тыңайтқыштар. Алғашқы фосфорлы тыңайтқыш ретінде топырақты фосфорлы ұн пайдаланылды. Оның өндірісі ХІХ ғасырдан басталады. Оны фосфатты шикізатты байыту арқылы алады. ХХ ғасырдың басталғанынша фосфорлы тыңайтқыш ретінде сүйек ұнын және тыңайтқыштарды қолданды, фосфат пен сүйектерді қышқылды өңдеу арқылы алады. Төменгі сапалы суперфосфот және преципитат түрінде алынады. ХХ ғасырдың басында Ресейде бұл әдіс бойынша 13 завот жұмыс жасап, жылына 129 мың тонна суперфосфат өндірді.
Фосфорлы МТ-тың технологиясының келешекте дамуы елдегі фосфатты кен қалдықтарының ашылуымен және енгізілуімен байланысты. 1928-1932 жылдар кезеңінде еліміздегі ауыл шаруашылық химизация тапсырмасын шешу үшін ірі суперфосфатты заводтар Константиновкада, Воскресеньскіде және Ленинградта ашылды, жылына 1,25 мың тонна өнімділікпен. 1930 жылдан бастап фосфорлы шикізат импорты тоқтатылды және өндіріс әйгілі фосфоритке ауысады, оның ішінде апатит концентратын, апатито – нефелинді флотациясын өндіріді. Осы жылдарда өте қарапайым суперфосфат өндірілді. Осы жылдарда экстракциялық фосфорлы қышқыл алу үшін әртүрлі қышқылдармен фосфатты шикізат ыдрату процесінің технологиялық режимін жасау және химия-физикалық негізін үйрену басталады, фосфор негізінде концентрацияланған және коплексті минералды тыңайтқыштар өндірілді: қос суперфосфотта, аммофосты, нитроаммфос және басқалар. 1934 жылы Воскресеньскіде және 1936 жылы Ақтөбеде концентрацияланған фосфорлы тыңайтқышты- преципитатты өндіру цехтары ашылды. Нәтежесінде 1940 жылы еліміздегі фосфорлы тыңайтқыш өндірісі 4,4 млн. тоннаны құрады, ал 1950 жылы 2,4 млн. тоннаға жетті.
|
|
|
1950-1960 жылдары қатары Самарқандағы, Сумақтағы, Чаржоудағы, Сумгайттегі суперфосфатты заводтар іске қосылды. Концентрацияланған және комплексті фосфорлы МТ өндірісі басталды. Фосфор негізіндегі МТ структурасына осы уақытта өзгерістер енгізілді: жай суперфосфаттың меншікті үлесі. 1962 жылы бірінші комплексті МТ- нитрофоска өндірісі қаланды. Ал 1963 жылы-аммофостың, және 1970 жылы - нитроаммофоскалар. Осының қатарында экстракциялықы фосфор қышқылы өндірісінің агрегаттың өнімділігі өсті және тыңайтқыш өндіретін жабдықтар дамыды.
Фосфорлы МТ өндірісі фосфор және фосфорлы қышқыл технологиясының дамуымен және құрылымымен тығыз байланысты. Әйгілі фосфор өнеркәсібінің бастапқы ХІХ ғасырдың 40-шы жылдарында болды. ХХ жүзжылдықтың басында Қазақстанда 10 фосфор заводы жұмыс жасады, фосфорлы қышқылы термиялық әдіспен жылына 180 мың тонна өнім өндірді.
Фосфор өнеркәсібінің әрі қарай дамуы электропештердің біріңғай күшін көтеру жолымен жүрді, пеш газының тиімді тазалануы, апативті концентратты шикізат ретінде пайдалану. 1969 жылы Жамбылда қос суперфосфат өндірісі бойынша 1970 жылы Жаңажамбылдың фосфор заводы ашылды.
Калийлі тыңайтқыш. Калийлі МТ-тың әйгілі өнеркәсібінің құрылуы Соликамскідегі, Предкарпаттағы, Старообнинскідегі калийлі тұздың ашылуымен тығыз байланысты. Ыстықтай шаймалау жолымен карналит өндірісі бойынша алғашқы фабрика 1937 жылы іске қосылған. Калий хлоридінің өндірісі галургиялық әдіспен ең алғаш рет 1933 жылы Солокамскіде алынды. 1954 жылы Брезняковтың калий комбинаты ашылды, ал 1963 жылы - бірінші кезекте Солигорск комбинат.
|
|
|
Хлорсыз калий тыңайтқыштың тұтынылуы мақтаның культивациясымен байланысты Калуш-Голынскдегі полиминералды кеннен калий сульфаты өндірістерін қажет етті. Оның негізінде 1975 жылы Калуштық фабрика ашылды, ондағы өнімнің 20%-ын калий сульфаты құрады.
Калий хлориді өндірісінің флотациялық әдісі бойынша зерттелуі 1952-1953 жылдары басталды. Олардың қорытындысы бойынша 1963-1964 жылдары Орал мен Солигорскідегі фабрика іске қосылды. Күрделі тұз жүйесі флотациясының физика-химиялық заңдылықтарын үйрену процесінде оптималды жарыстар табылды және флотация процесінің реагенті таңдаулы өндірістің технологиялық сызбалары құрылды. 1966-1973 жылдары пайдалануға жаңа флотациясы фабрикаға калий хлоридін алуы бойынша Солигорскіде ашылды. Калийлі минералды тыңайтқыштарда халық шаруашылығының қажеттілігін қамтамасыз етті.
Тұздар технологиясының типтік процестері.
Көптеген МТ құрамында әртүрлі минералды тұздар немесе қатты заттар бар. Минералды тыңайтқыш өндірісінің технологиялық сызбасы әртүрлі, бірақ көп жағдайда типтік процестердің біреуі қолданылады, тұз технологиясына сәйкес, оның мақсаты-күрделі жүйені бөлу, олар бірнеше тұз компонеттерінен тұрады.
Тұзда минералды шикізатты өндіру не оның жоғары температуралы өңделуімен не сұйық ортадағы және суспензиялық жолмен жүруі мүмкін. Осыған орай өңдеуге шикізатты даярлаудың қарапайым процесіне орай, тұз технологиясында процестің екі типі бар:
- термиялық немесе термохимиялық өңдеу, яғни, шикізатты күйдірудің әртүрлі түрі;
- еріту, қайта кристалдандыру процестері заттарды, химиялық өңдеумен, бөлумен, тазалаумен байланысты.
Күйдіру деп минералды термиялық өңдеуді айтады. Оларды қыздыру кезінде берілген температураға дейін ұстайды. Қыздыру кезіндегі процесс шартына байланысты, термиялық ыдрау реакциясы өтеді, қышқылдану немесе орнатылу, түзілу және минералдың полиморфлы түзілісі жүреді. Қыздыру кезіндегі химиялық түзіліске сәйкес ерекшеленеді.
- кальцинациялық күйдіру, мұның мақсаты - заттардан ұшатын копонентерді бөлу, көбінесе көміртегі оксидін (IV) және конституциялық суды. Мысалы, әкті өртеу:
СаСО3 = CaO + CO2
немесе алюминий гидроксидін оксидтелгенше дегидрациялау: 2 АІ(ОН)3 = АІ2О3 + 3Н2О
- тотықтыру күйдіру, мұның мақсаты- элементтің қышқылдану дәрежесін көрсету, мысалы: 6 ҒеО + О2 = 2Ғе3О4
немесе сульфидтың оксидке айналуы:
CuS + 1.5O2 = CuO + SO2
- тотықсыздандыру күйдіру, мұның мақсаты-элементтің тотығу дәрежесін түсіру. Мысалы, элементті фосфорды алу:
Са3 (РО4)2 + 5С + 3SіО2 = Р2 + 5СО + 3Са SіО3
Күйдірудің жеке жағдайы -шикізатты қандай-да бір реагенттермен еріткіш түзу мақсатында пісіру, өнім шикізатынан алынатын, мысалы: фторапатитті содамен қайнату:
Ca5(PO4)2F + 2Na2CO3 + SiO2 = 3CaNaPO4 + Ca2SiO4 +NaF +2CO2
Күйдіру мен жентектеу гетерогенді процестерден өтеді. Ондағы реакция мынадай жүйеде өтеді «Т+Т», «Т + Ж» және «Т + Г», мұндағы газ тәрізді және сұйық фазалар диссоциация және қатты заттың балқу есебінен түзіледі. Сондықтан, қыздыру мен қайнату процесінің жылдамдығы химиялық реакция жылдамдығына байланысты, осылайша айдау, балқыту және қаттыландыру диффузия, сұйық және газтәрізділердің фаза арқылы өтуі, әсер етуші копаненттермен және олардың өзара әрекеттесу өнімдерінен түзілгендері.
Процесс жылдамдығы лимитеуші стадия жылдамдығымен анықталады, ол нақты шартқа тәуелді және әртүрлі кинетикалық теңдеулермен беріледі. Мысалы, кинетикалық аймақта өтетін процесс үшін:
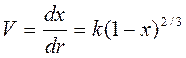 (5.3)
(5.3)
бұл жердегі: х – айналу дәрежесі;
k – реагент қасиетіне тәуелді және процесс шартына тәуелді коэффициент.
Күйдіру мен жентектеу процестер жылдамдығы температураны көтергенде, өртенген материал компонентін ұнтақтағанда, оның концентарциясын көтергенде көтерілуі мүкін, мұндай кезде компоненттің біреуі сұйық немесе газ тәрізді жағдайда болады.
Қатты денені еріту процесі деп қатты қиыршықты ертікіштің әсерімен бұзу процесін айтады. Еріткіш физикалық болуы мүмкін. Ерітілген заттың ерітіндіден мына үлгі бойынша қайтымды кристалдануы мүмкін болғанда: А + Р ↔ АР ↔ Р + А және химиялық, еріткіш немесе құрамындағы реагент, еритін затпен химиялық өзара әрекеттескенде және оның қайтымды кристалдануын мүмкін емес етеді, яғни мына үлгі бойынша:
А + Р = ВР + Р
мұндағы: А –ерітілген зат;
Р – еріткіш; В- еріту нәтижесінде түзілген жаңа зат.
Мұндағы химиялық еріту процесінің физикалық еріту процесінен ерекшелігі қайтымсыз. Гетерогенді каталитикалық емес еріту процесі де болады, «Т + Ж» жүйесінде диффузиялық аймақта өтеді, ауа гетерогенді процесс үшін ортақ теңдеу қолданады:
V = КМ · Ғ · ΔС (5.4)
Еріту процесі температураны көтеру, қатты фазаны ұсақтау (Ғ), концентрацияны ұлғайту (ΔС) және араластыру есебінен жеделдетіледі. Физикалық еріту процестің қозғаушы күшімен өзгерген жағдайда, концентрацияның ерекшілігі пайда болады ΔС = (СН-·С), сондықтан оның жылдамдығы мына теңдеумен анықталады:
VФ = КР · Ғ(СН- С), (5.5)
мұндағы: КР –еріту жылдамдығының коэффициенті;
Ғ - еріген зат кристалдарының бет алаңы; С – сұйық фазада еріген заттың концентрациясы; СН - берілген температурада қаныққан ертітінділердің концентрациясы.
Мұнда еру мөлшері бойынша концентрация төмендейді (СН- С), және еру процесі баяулай түседі. Ең қарапайым жағдайда, реакция тек қана қатты дене қабатында өткен кезде, химиялық еріту жылдамдығы мына теңдеумен бірілуі мүкін:
V = К · Ғ · СР
бұл жердегі: К- гидродинамикалық және басқа еру шартындағы
температураға байланысты коэффициент.
СР – еріткіштегі белсенді реагент концентрациясы.
Ерітіндіден кристалдау және басқа процестер.
Кристаллизация деп ерітіндідегі қатты фазаны бөлу процесін айтады. Тәсіліне байланысты, оның көмегімен еріткіштің артық қанығуына қол жеткізіледі, кристаллизацияның екі түрі болады; политермиялық және изотермиялық.
Политермиялық кристалдау кезінде артық қаныққан ерітінді жүйені салқындату есебінен түзіледі. Бұл процесс ауыспалы температурада өтеді. Заттарды кристалдау үшін қолданбалы әдіс, еру қасиеті температураны көтеру кезінде ұлғая түседі (сурет 5.2 қисық 1).
Изотермиялық кристалдау кезінде артық қаныққан ерітінді еріткіш бөлігін бұлау нәтежесінде түзіледі. Бұл әдіс үнемі бір температурада жүреді (T = const). Бұл әдіс заттарды кристалдау үшін қолданылады, олардың еру қасиеті температураға тәуелді (сурет 5.2 қисық 2). Кристаллизацияның бір түрі тұнбаға түсіру, яғни концентрлі ерітіндіге басқа затты қосқанда, еріген заттың ерігіштігі төмендейді де, тұнбаға түседі.

Сурет 5.2. Заттардың еруінің температураға тәуелділігі.
Бақылау сұрақтары
- Өсімдік ұлпаларының құрамына кіретін негізгі элементтерін атаңыз және олардың өсімдікте тіршілік етудегі маңыздылығын көрсетіңіз?
- Жер өңдеудің қазіргі сатысында минералды тыңайтқыштарды топыраққа енгізудің қажеттілігі неге байланысты?
- Қазіргі кездегі минералды тыңайтқыштардың жіктелуін анықтаңыз?
- Минералды тыңайтқыштардың құрамында қандай қоректі заттар бар?
- Минералды тыңайтқыштар өндірісінде қолданылатын тұз өндірудің негізгі типтік процесін атаңыз және мысал келтіріңіз?
- Физикалық ерумен химиялық ерудің айырмашылығы.
- Политермиялық кристаллизация мен изотермиялық кристаллизацияның айырмашылығы не, мысал келтіріңіз?
№13 ЛЕКЦИЯ. Органикалық қосылыстардың технологиясы
Негізгі органикалық синтез өнімдері.
Негізгі немесе ауыр органикалық синтез (НОС) деп салыстырмалы түрде құрылысы қарапайым, өте үлкен мөлшерде өндірілетін мақсатты өнім және органикалық технологияның басқа салаларындағы жартылай өнім ретінде пайдаланылатын органикалық заттар өндірісінің жиынтығы аталады.
НОС мақсатты өнімдеріне синтетикалық сұйық отын, майлайтын майлар, еріткіштер мен экстрагенттер, мономерлер, полимер материалдарының пластификаторлары, пестицидтер және өсімдіктерді қорғау құралдары және басқалар жатады. НОС жартылай өнімдері ретінде сәйкес қосылыстардың гомологтық қатарының қарапайым өкілдері: көмірсутектер (этилен, пропилен, бензол), галоген орнын басқан (дихлорэтан, винилхлорид), спирттер (метанол, этанол), альдегидтер мен кетондар (ацетальдегид, ацетон), органикалық қышқылдар (сірке қышқылы) және басқалар пайдаланылады. НОС жеңіл органикалық синтезден айырмашылығы (ЖОС) құрылысы күрделі, салыстырмалы түрде аз мөлшермен өндірілетін мақсатты соңғы өнім ретінде артықшылықпен пайдаланылатын органикалық заттар өндірісін біріктіреді. Оларға бояғыштар, фото және кинореактивтер, фармацевтикалық препараттар, жарылғыш заттар, парфюмериялық құралдар және т.б. жатады. Пайдалануына байланысты оларды екі топқа бөледі:
- аралық өнімдер, басқа заттар синтезінде пайдаланылады;
- мақсатты пайдаланылатын негізгі өнімдер.
Аралық өнімдер (парафиндер, олефиндер т.б.) үлкен масштабта өндіріледі, оларды мақсатты синтезде көп қолданады. Мономерді өндіру негізгі органикалық синтезде үлкен орын алады, оларды пластмассаны, синтетикалық каучукты, синтетикалық лактарды, кілейлерді, пленкалық материалдарды, талшықтарды өндіруде шикізат ретінде көп мөлшерде қолданады.
Барлық синтетикалық полимерлерді полимеризация жэәне поликонденсация арқылы алады. Полимеризация кезінде мономерлер жылу, жарық сәулелендіру немесе катализатор әсерінен бір-бірімен байланысады және керек қасиеті бар полимерлер алынады.
Пластификаторларды (жұмсартқыштар) полимерлерге (30-40%-ке дейін) қосу арқылы оларды пластикалық, эластикалық қасиеттерін реттейді. Пластификаторды қосқанда полимерді қалыптау, престеу, ию т.б. операцияларды жүргізу жеңілдейді. Пластификаторға қойылатын негізгі талап полимермен бірлесуі, ұшуының төмендігі. Пластификаторлар топтары: жоғары температурада қайнайтын күрделі эфирлер (дибутил –мен диоксидфталандар, жоғары қышқылдардың немесе спирттердің кейбір эфирлері. Каучук өндірісінде жұмсартқыш ретінде минералды майлар, алкилароматты көмірсутектер, төмен полиолефиндер т.б. қолданылады.
Синтетикалық БАЗ мен жуу заттары. Беттік активті заттардың қасиеттері гидрофобты және сумен сольваттарға бейім гидрофильдік (полярлық) топтары бар органикалық заттарға бөлінеді. Кәдімгі сабында стеарин немесе пальмитин қышқылының натрий тұзы RCOONa аталған топтардың ролін ұзын тізбекті көмірсутек және карбоксилатты топ атқарады.
БАЗ күйдің шекаралық бетіне шоғырланады, өзінің гидрофобтық тобымен жүйенің компонентіне, ал гидрофильдік топтар суға бағытталады. БАЗ және жуатын заттар ионогенді және ионогенсіз болады. Ионогенді заттар анионды және катионды активті болады. Олардың беттік активтілік қасиеті диссоциация кезінде пайда болатын анионмен немесе катионмен анықталады.
Анионды активті заттар(синтетикалық майлы қышқылдан алынатын сабын) сілтілі орта түзейді, матаны ыдыратады, Са, Мg тұздарымен ерімейтін қосылыстар құрайды, жуылу дәрежесін төмендетеді. Аталған кемшіліктерден құтылу үшін алкиларенсульфатты RC6H4SO2ONa, алкилсульфонатты RSO2ONa және алкилсульфатты RОSO2ONa (алкил тобымен С12-С18) қолданады. Катион активті жуатын заттар сирек пайдаланылады. Кейінгі кезде ионогенді емес жуатын заттар көбірек қолданылуда. Оларды этиленоксидты мен әртүрлі органикалық қосылыстар (карбонды қышқылдар, спирттер, аминдер т.б. активті сутек атомы бар заттар) синтезінен алады. Заттардың жуу қабілетін көтеру үшін БАЗ басқа қоспалармен араластырады. Мысалы, жуу ұнтағы құрамында фосфат, натрийдің пирофосфаты немесе гексаметафосфаты, силикат, натрий сульфаты мен карбонаты, пербораттар, карбометилцеллюлоза (Целл. – ОСН2СООNa) болады.
Синтетикалық отын, майлау майлары және оған қоспа. Синтетикалық моторлық және ракеталық отын, антифрендер, тормоздық және гидравликалық сұйықтарды алу негізгі органикалық синтезде үлкен орын алады. Көмірсутектің сұйық отынды көмірден алу, кейін іштен жанатын двигательдер үшін жоғары октанды отын өндіру үшін изопарафиндер синтезі, әсіресе, изооктанды (СН2)2СНСН2 С(СН3) өндіру іске асырылады. Мотор отынының жоғары октанды компоненті ретінде изопропилбензолды пайдаланады. Ал кейінгі кезде метанолды, үшіншілік-бутилметилді эфирді пайдалану перспективасы шешілуде.
Синтетикалық отынды ракеталық техникада метанол, этанол, этиламиндер, диметилгидразин, кейбір металорганикалық қосылыстарын пайдаланудың көмірсутек жанармайлығынан артықшылығы мәлім болды. Жағар майларын мұнайдан өндіреді, бірақ жаңа техниканың талабына бұлар сәйкес келмей жатыр. Мысалы, двигательдерді минус 300С температурада және жоғарыайналымда жұмыс істету үшін жаңа жағар майлар қажет. Олардың тұтқырлығы температураға аз байланысты, ұшпайтын, коррозия етпейтін, тотықпайтын және ыдырамайтын қасиеттері болуы керек.
Синтетикалық жағар майларға келесі органикалық қосылыстар топтарына жатады: синтетикалық көмірсутектер олефиндердің төмен полимерлері мен алкилденген ароматты көмірсутектер); екі негізді карбон қышқылдары мен жоғары біратомдық спирттердің және жоғары монокарбондық қышқылдар мен көп атомдық спирттердің күрделі эфирлері; жоғары температурада қайнайтын фторкөмірсутектер және фторхлоркөмірсутектер (оларда сутек атомдары толығымен галогенмен ауыстырылады); кремнийорганикалық полимерлер силоксандық байланыстағы Si – O – Si
Отын мен майлардың эксплуатациялық санасын көтеретін қоспалар өндірілуде. Тотығуды болдырмайтын қоспалар автототығудың тізбекті реакциясын тежейді (мысалы, алкилденген фенолдар), басқалары майдың қатаю температурасын төмендетеді (депрессорлар), коррозияны төмендетеді (ингибитор).
|
|
|
|
|
Дата добавления: 2014-12-10; Просмотров: 1502; Нарушение авторских прав?; Мы поможем в написании вашей работы!