
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчеты по формулам веществ
|
|
|
|
Стехиометрические расчеты
Химические реакции
Вычисляем атомную массу металла
Аr = Мэк∙Z = 32,6∙2 = 65,2
5) В периодической системе двухвалентный металл с близкой атомной массой – это цинк.
Химическими реакциями называются превращения одних веществ в другие при их взаимодействи. С помощью формул веществ химическую реакцию можно записать или в виде схемы, или в виде уравнения.
Схема химической реакции несет только качественную информацию: какие вещества (реагенты) взаимодействуют и какие вещества (продукты) при этом получаются:
C2H5OH + O2 ® CO2 + H2O
Закон сохранения массы в схеме реакции не соблюдается, поэтому между реагентами (исходными веществами) и продуктами ставится стрелка.
В уравнении реакции закон сохранения массы соблюдается, поэтому между реагентами и продуктами ставится знак равенства:
C2H5OH + 3O2 = 2CO2 + 3H2O
Химические реакции подробно рассматриваются на следующей лекции.
Напоминаем, что стехиометрией называется раздел химии, который изучает количественные соотношения между элементами в соединениях и между веществами в химических реакциях. Стехиометрические расчеты проводятся по формулам веществ, уравнениям реакций и по закону эквивалентов.
Формула вещества – это не только молекула или формульная единица вещества, но и один моль этого вещества. Поэтому по формуле можно вычислить количественный состав вещества (массовые доли элементов) и, наоборот, по известному количественному составу вещества определить его формулу.
Пример 13. Вычислить массовые доли натрия, углерода и кислорода в карбонате натрия.
Решение. Один моль карбоната натрия Na2CO3 содержит 2 моль атомов натрия, 1 моль атомов углерода и 3 моль атомов кислорода. Молярная масса Na2CO3 равна 106 г/моль, натрия – 23 г/моль, углерода – 12 г/моль, кислорода – 16 г/моль. В 106 г (1 моль) Na2CO3 содержится натрия – 46 г, углерода – 12 г и кислорода – 48 г. Вычисляем массовые доли элементов (ω):
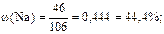
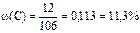
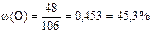
Пример 14. Определить формулу оксида железа, содержащего 69,9 % железа и 30,1 % кислорода.
Решение. Обозначим числа атомов железа и кислорода в формуле оксида символами х и у (FexOy). Молярная масса атомов железа равна 55,85 г/моль, а кислорода – 16,00 г/моль. Масса железа в оксиде составляет 55,85∙х, кислорода – 16,00∙у, а отношение этих масс по условию задачи равно 69,9: 30,1. Таким образом:
69,9: 30,1 = 55,8×x: 16,00×y, откуда x: y = 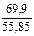 :
: 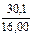 = 1,25: 1,88
= 1,25: 1,88
Чтобы выразить полученное отношение целыми числами, разделим оба его члена на меньший из них, а затем умножим на два:
x: y = 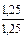 :
: 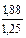 = 1: 1,5; x: y = 2: 3
= 1: 1,5; x: y = 2: 3
Таким образом, формула оксида железа – Fe2O3.
|
|
|
|
|
Дата добавления: 2014-12-16; Просмотров: 1147; Нарушение авторских прав?; Мы поможем в написании вашей работы!