
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Опыт 1. Взаимодействие меди с кислотами
|
|
|
|
Экспериментальная часть
Теоретические вопросы
ЭЛЕМЕНТЫ IВ И IIВ ГРУПП. МЕДЬ, ЦИНК
Задачи и упражнения
1. Вычислите потенциал водородного электрода, погруженного а) в раствор с рН=3,5; б) в раствор с рН=5; в) раствор с рН= 10,7; с) в раствор с рН=14.
2. Потенциал водородного электрода в некотором водном растворе равен – 118 мВ. Вычислите активность ионов Н+ в этом растворе.
3. Водородный электрод погружен в раствор с рН=0. Насколько изменится потенциал электрода, если раствор нейтрализовать до рН=7?
4. Вычислите электродный потенциал никеля, опущенного в раствор его соли концентрации: а) 0,01 моль/л; б) 0,1 моль/л; в) 0,5 моль/л; г) 1 моль/л.
5. Вычислите э.д.с. концентрационного гальванического элемента (в милливольтах), состоящего из цинковых электродов, опущенных в растворы сульфата цинка с активностью 2.10-2 и 3,2.10-3 моль/л.
6. Вычислите э.д.с. концентрационных элементов (растворы содержат по 0,1 моль/л KNO3): а) Ag/AgClнас.//AgIнас./Ag; б) Ag/Ag2Sнас..//.AgClнас./Ag.
7. При какой активности Pb2+ э.д.с. гальванического элемента Pb/ Pb2+//H+/H2 будет равна нулю? Возможна ли такая активность?
8. В каком направлении будут перемещаться электроны во внешней цепи гальванического элемента Mg/Mg2+//Fe3+/Fe, если концентрации электролитов равны 1 моль/л? Насколько изменится э.д.с. этого элемента, если растворы обеих солей разбавить до концентрации 0,03 моль/л?
9. Напишите уравнения коррозионных процессов луженого железа а) в кислой среде; б) в щелочной среде.
10. Напишите уравнения коррозионных процессов оцинкованного железа а) в кислой среде; б) в щелочной среде.
Лабораторная работа 14
1. Положение меди, серебра и цинка в периодической системе. Особенности их электронного строения меди.
2. Характерные степени окисления для меди, серебра и цинка. Примеры соединений в этих степенях окисления.
3. Природные соединения меди, серебра и цинка. Получение металлов.
4. Взаимодействие меди, серебра и цинка с с кислотами.
5. Амфотерные свойства гидроксида цинка.
6. Окислительные свойства соединений меди(II) и серебра(I).
7. Координационные соединения меди, серебра и цинка.
а) Поместите в пробирку немного стружек меди и прилейте 1-2 мл H2SO4 (2н). Отметьте отсутствие изменений. Прилейте в пробирку несколько капель пероксида водорода (H2O2) и слегка встряхните содержимое пробирки. Отметьте изменение окраски раствора и объясните происходящее явление. Напишите уравнение реакции.
Cu + H2SO4 разб. ¹
Cu + H2SO4 + H2O2 ® CuSO4 + H2O
б) Поместите в две пробирки немного медных стружек (опыт проводите под тягой). В первую пробирку налейте немного концентрированной серной кислоты и нагрейте. Что наблюдаете? Напишите уравнение реакции. Во вторую пробирку прилейте немного концентрированной азотной кислоты HNO3. Что наблюдаете? Напишите уравнение реакции.
Cu + H2SO4 конц. ® CuSO4 + SO2 + H2O
Cu + HNO3 конц. ® Cu(NO3)2 + NO2 + H2O
Cu + HNO3 разб. ® Cu(NO3)2 + NO + H2O
Опыт 2. Получение и свойства гидроксида меди(II)
Налейте в пробирку 5-6 капель раствора соли меди(II) и добавьте такой же объем щелочи NaOH (2н). Напишите уравнение реакции, отметив цвет осадка. Разделите осадок на три пробирки. В первую пробирку прилейте 1-2 мл раствора H2SO4 (2н), а во вторую - 1-2 мл раствора NaOH (2н). Что наблюдаете? Проявляет ли гидроксид меди в этих условиях кислотные свойства? Напишите уравнения реакций. Третью пробирку с гидроксидом меди(II) нагрейте на водяной бане. Что наблюдаете? Сделайте вывод о термической устойчивости гидроксида меди(II). Напишите уравнение реакции.
CuSO4 + NaOH ® Cu(OH)2 + Na2SO4
Cu(OH)2 + H2SO4 ® CuSO4 + H2O
Cu(OH)2 + NaOH ¹
Cu(OH)2 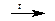 CuO + H2O
CuO + H2O
Опыт 3. Окислительные свойства иона меди(II)
Налейте в пробирку примерно 1 мл раствора сульфата меди(II) и добавьте немного раствора KI. Наблюдайте изменение в окраске раствора и выпадение белого осадка CuI. Добавьте несколько капель крахмала. Почему крахмал окрасился в синий цвет? Напишите уравнение реакции.
CuSO4 + KI ® CuI + + I2 K2SO4
Опыт 4. Получение аммиаката меди. Качественная реакция на ион Cu2+
Налейте в пробирку 2-3 капли раствора сульфата меди(II) и прилейте такое же количество раствора NH4OH (2н). Составьте уравнение реакции и отметьте цвет осадка сульфата гидроксомеди(II). По каплям добавляйте в пробирку концентрированный раствор NH4OH (25%). Наблюдайте за растворением осадка и изменением окраски раствора вследствие образования ионов [Cu(NH3)4]2+. Составьте уравнение реакции.
CuSO4 + NH4OH ® (CuOH)2SO4 + (NH4)2SO4
(CuOH)2SO4 + (NH4)2SO4 + NH4OH ® [Cu(NH3)4]SO4 + H2O
|
|
|
|
|
Дата добавления: 2015-01-03; Просмотров: 824; Нарушение авторских прав?; Мы поможем в написании вашей работы!