
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции 1-ого порядка
|
|
|
|
Тримолекулярные: 2NO + Cl2 ® 2NOCl
Бимолекулярные: H2 + I2 ® 2HI
Мономолекулярные: I2 ® 2I
Целое (+) число: 1,2, реже 3
а) H2 + I2 ® 2HI – простая (элементарная) реакция
n (Н2) = 1, n (I2) =1,т.е. равны стехиометрическим коэффициентам.
n = 1+1 =2 Þ 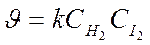
б) 2N2O5 ® O2 + 2N2 O4 - сложная реакция
протекает по стадиям:
1. N2O5 ® O2 + N2O3;
2. N2O3 ® NO + NO2;
3. 2NO2 ® N2O4.
и самая медленная стадия – (2) Þ она определяет порядок
кинетического уравнения:
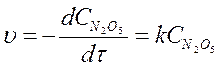
 Опыт: 5Na2SO3 + 2HJO3
Опыт: 5Na2SO3 + 2HJO3  J2 + 5Na2SO4 + H2O
J2 + 5Na2SO4 + H2O
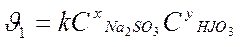 ;
; 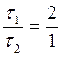 ;
; 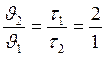
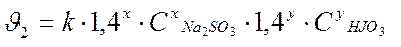
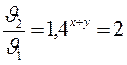 ; (x+y) lg 1,4 = lg 2; x+y =
; (x+y) lg 1,4 = lg 2; x+y = 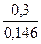 @ 2
@ 2
 Лаб.раб.: Na2S2O3 +H2SO4 = S + H2SO3 + Na2SO4
Лаб.раб.: Na2S2O3 +H2SO4 = S + H2SO3 + Na2SO4
Механизм: 1ст.: Na2S2O3 +H2SO4 = H2S2O3 + Na2SO4 быстро
2ст.: H2S2O3 = S + H2SO3 - медленно
 А В CH3OCH3® CH4 + H2 + CO
А В CH3OCH3® CH4 + H2 + CO
Кинетическое уравнение реакции первого порядка
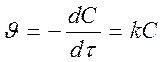 .
.
Разделим переменные и проинтегрируем

lnC – lnC0 = -kt Þ lnC = lnC0 - kt
С0 – исходная концентрация
С - концентрация в момент времени t
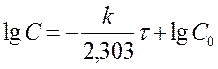
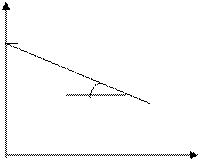
Кинетическая кривая реакций 1-ого порядка
 lg C
lg C
lg C o tga = - 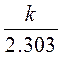
a
t, с
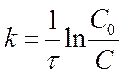 или
или 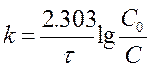 . [ k ] = [с-1]
. [ k ] = [с-1]
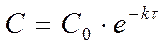 .
.
период полупревращения τ1/2:
|
C = 0,5C0 Þ 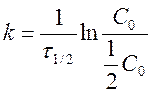
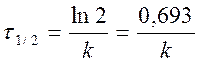 - не зависит от С о
- не зависит от С о
|
|
|
|
|
Дата добавления: 2014-12-24; Просмотров: 391; Нарушение авторских прав?; Мы поможем в написании вашей работы!